อันดับแรก โลหะอลูมิเนียมได้รับทางเคมีโดยนักเคมีชาวเยอรมัน F. Wöhler ในปี ค.ศ. 1821 (ลดการใช้อะลูมิเนียมคลอไรด์กับโพแทสเซียมของโลหะเมื่อถูกความร้อน) ในปี ค.ศ. 1854 นักวิทยาศาสตร์ชาวฝรั่งเศส Saint-Clair Deville ได้เสนอวิธีทางเคมีไฟฟ้าสำหรับการผลิตอะลูมิเนียมโดยการลดอะลูมิเนียม-โซเดียม ดับเบิ้ลคลอไรด์ด้วยโซเดียม
การผลิตและการผลิตอลูมิเนียม
อลูมิเนียมเมทัลลิกได้มาจากสามขั้นตอน:
- การรับอลูมินา (Al 2 O 3) จากแร่อะลูมิเนียม
- รับอลูมิเนียมจากอลูมินา
- การกลั่นอลูมิเนียม
รับอลูมินา
ประมาณ 95% ของอลูมินาทั้งหมดได้มาจากแร่บอกไซต์
อะลูมิเนียม(แร่อะลูมิเนียมฝรั่งเศส) (ตามชื่อพื้นที่ Baux ทางตอนใต้ของฝรั่งเศส) - แร่อะลูมิเนียมประกอบด้วยอะลูมิเนียมไฮดรอกไซด์ ออกไซด์ของเหล็กและซิลิกอน วัตถุดิบสำหรับการผลิตอลูมินาและวัสดุทนไฟที่มีส่วนผสมของอลูมินา เนื้อหาของอลูมินาในแร่บอกไซต์เชิงพาณิชย์มีตั้งแต่ 40% ถึง 60% และอีกมากมาย นอกจากนี้ยังใช้เป็นฟลักซ์ในโลหะผสมเหล็ก
ภาพที่ 1 - แร่อะลูมิเนียม
โดยทั่วไป บอกไซต์เป็นก้อนดิน คล้ายดินเหนียว ซึ่งอาจมีลักษณะเป็นแถบ พิโซไลต์ (คล้ายถั่ว) หรือเนื้อที่สม่ำเสมอ ภายใต้สภาวะอากาศปกติ เฟลด์สปาร์ (แร่ธาตุที่ประกอบเป็น ที่สุด เปลือกโลกและเนื่องจากเป็นอะลูมิโนซิลิเกต) สลายตัวด้วยการก่อตัวของดินเหนียว แต่ในสภาพอากาศร้อนและมีความชื้นสูง บอกไซต์อาจกลายเป็นผลิตภัณฑ์ขั้นสุดท้ายของการสลายตัว เนื่องจากสภาพแวดล้อมดังกล่าวเอื้อต่อการกำจัดด่างและซิลิกา โดยเฉพาะจากไซเอไนต์หรือแกบโบร อะลูมิเนียมจะถูกแปรรูปเป็นอะลูมิเนียมเป็นขั้นๆ ขั้นแรก ได้อะลูมิเนียมออกไซด์ (อลูมินา) และจากนั้นก็อะลูมิเนียมที่เป็นโลหะ
สิ่งเจือปนหลักในแร่บอกไซต์คือ Fe 2 O 3 , SiO 2 , TiO 2 สิ่งเจือปนเล็กน้อยของแร่บอกไซต์ ได้แก่ Na 2 O, K 2 O, CaO, MgO, ธาตุหายาก, Cr, P, V, F, สารอินทรีย์
โดยปกติแล้วแร่อะลูมิเนียมจะถูกจัดประเภท:
- ตามสี
- โดยแร่หลัก (มักผสมกัน);
- ตามวัย
เกณฑ์หลัก คุณสมบัติของแร่อะลูมิเนียมคือ:
- โมดูลซิลิคอน (Msi = Al 2 O 3 /SiO 2 (% wt.)) โมดูลซิลิกอนที่ใหญ่ขึ้น the คุณภาพที่ดีกว่า(MSI = 7);
- ปริมาณธาตุเหล็กในแง่ของ Fe 2 O 3 หากเนื้อหาของ Fe 2 O 3 อยู่ที่ประมาณ 18 % โดยน้ำหนัก อะลูมิเนียมก็ถือเป็นธาตุเหล็กสูง ยิ่งมีธาตุเหล็กมากเท่าไร การขุดแร่บอกไซต์ก็ยิ่งยากขึ้นเท่านั้น
- ปริมาณกำมะถัน การปรากฏตัวของกำมะถันจำนวนมากทำให้การประมวลผลของบอกไซต์ซับซ้อน
- เนื้อหาของคาร์บอเนตในแง่ของ CO 3 (2-) . การปรากฏตัวของคาร์บอเนตจำนวนมากทำให้การประมวลผลของบอกไซต์ซับซ้อน
ใช้อะลูมิเนียม:
- ในการผลิตอลูมินา
- ในการผลิตวัสดุที่มีฤทธิ์กัดกร่อน
- ในการผลิตวัสดุทนไฟ
- เป็นฟลักซ์สำหรับการถลุงเหล็กแบบเปิด
- สำหรับการอบแห้งก๊าซและน้ำมันทำความสะอาดจากกำมะถัน
- เป็นสีย้อม
จนถึงปัจจุบันซัพพลายเออร์หลักของอะลูมิเนียมคือ:
- ออสเตรเลีย - มีเงินฝากจำนวนมากเช่น Fe, Au, U, Ni, Co, Cu และอื่นๆ การซื้อวัตถุดิบจากออสเตรเลียมีกำไรมากกว่าการซื้อวัตถุดิบเอง
- กินี - รัสเซียซื้อที่นั่งหลายที่นั่ง
- อเมริกากลาง: กายอานา จาเมกา ซูริมาน
- บราซิล.
ในยุโรป เงินฝากทั้งหมดจะหมดลง บอกไซต์มาจากกรีซ แต่วัตถุดิบนี้มีคุณภาพต่ำ

รูปที่ 2 - ปริมาณสำรองของอะลูมิเนียมในโลก
ด้านล่างเป็นแหล่งแร่อะลูมิเนียมหลักในรัสเซีย
- เงินฝากครั้งแรกถูกค้นพบในปี 1914 ใกล้เซนต์ปีเตอร์สเบิร์ก ใกล้เมือง Tikhvin 6 โรงงานถูกสร้างขึ้นที่สนามนี้ ที่ใหญ่ที่สุดคือโรงงานอลูมิเนียม Volkhov จนถึงปัจจุบัน เขตข้อมูล Tikhvinskoye หมดลงแล้วและดำเนินการกับวัตถุดิบที่นำเข้าเป็นหลัก
- ในปี 1931 มีการค้นพบแหล่งแร่บอกไซต์คุณภาพสูง (SUBR) ของ Severo-Uralskoye เป็นพื้นฐานสำหรับการก่อสร้างโรงงานอะลูมิเนียม Ural (UAZ) ในปี 1939 และบนพื้นฐานของเหมืองบอกไซต์เซาท์อูราล (YUBR) โรงถลุงอะลูมิเนียม Bogoslovsky (BAZ) ก็ถูกสร้างขึ้น
- สนาม Severoonezhskoye ตั้งอยู่บนถนนสู่คาบสมุทร Kola อยู่ในแผน แต่ไม่ทราบวันที่สร้าง
- เงินฝาก Vislovskoe เป็นดินเหนียวบริสุทธิ์ประเภท kaolite ไม่ใช้สำหรับอลูมินา
- เขต Timanskoye (สาธารณรัฐ Komi, Varkuta) ชาวแคนาดามีความสนใจในสาขานี้ ดังนั้นพวกเขากำลังวางแผนที่จะสร้างโรงงาน (Komi Sual เป็นบริษัทโฮลดิ้ง)
การรับอลูมินาจากแร่บอกไซต์
เนื่องจากอะลูมิเนียมมีลักษณะเป็นแอมโฟเทอริก จึงผลิตอลูมินาได้สามวิธี:
- อัลคาไลน์,
- กรด;
- อิเล็กโทรไลต์
วิธีที่นิยมใช้กันมากที่สุดคือวิธีอัลคาไลน์ (วิธีของ K.I. ไบเออร์ ซึ่งพัฒนาขึ้นในรัสเซียเมื่อปลายศตวรรษก่อนที่ผ่านมา และใช้สำหรับการประมวลผลบอกไซต์คุณภาพสูงที่มีซิลิกาในปริมาณเล็กน้อย (มากถึง 5-6%)) เนื่องจาก การนำเทคนิคไปใช้มันได้รับการปรับปรุงอย่างมาก รูปแบบการผลิตอลูมินาโดยวิธีไบเออร์แสดงในรูปที่ 3
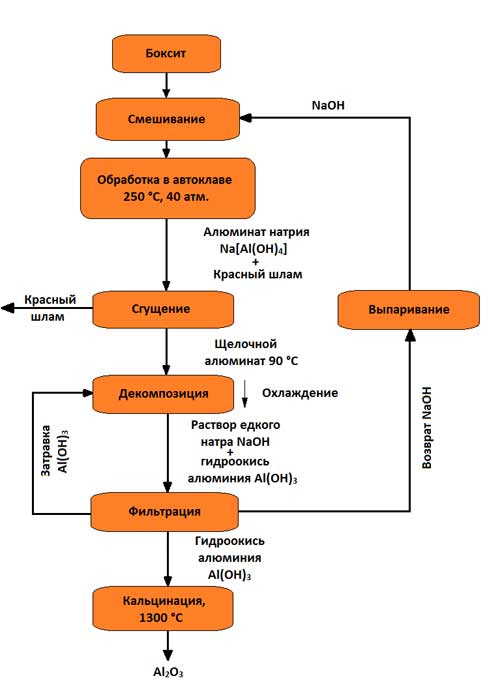
รูปที่ 3 - โครงการรับอลูมินาโดยวิธีไบเออร์
สาระสำคัญของวิธีการนี้คือ สารละลายอะลูมิเนียมจะสลายตัวอย่างรวดเร็วเมื่อใส่อะลูมิเนียมไฮดรอกไซด์เข้าไป และสารละลายที่เหลือจากการสลายตัวหลังจากการระเหยของสารละลายภายใต้สภาวะของการผสมแบบเข้มข้นที่ 169–170 °C สามารถละลายอลูมินาที่มีอยู่ในอะลูมิเนียมได้อีกครั้ง วิธีนี้ประกอบด้วยการดำเนินการหลักดังต่อไปนี้:
1. การเตรียมอะลูมิเนียมซึ่งประกอบด้วยการบดและบดในโรงสี โรงสีจะมาพร้อมกับบอกไซต์ ด่างกัดกร่อน และไม่ใช่ จำนวนมากของมะนาวซึ่งปรับปรุงการจัดสรร Al 2 O 3 ; เยื่อกระดาษที่ได้จะถูกป้อนเพื่อชะล้าง
2. การชะล้างอะลูมิเนียม (in ครั้งล่าสุดบล็อกหม้อนึ่งความดันรูปทรงกลมที่ใช้จนถึงขณะนี้ได้ถูกแทนที่บางส่วนด้วยหม้อนึ่งความดันแบบท่อซึ่งการชะล้างเกิดขึ้นที่อุณหภูมิ 230–250 ° C (500–520 K) ซึ่งประกอบด้วยการสลายตัวทางเคมีจากการมีปฏิสัมพันธ์กับ สารละลายน้ำด่าง; อะลูมิเนียมออกไซด์ไฮเดรตเมื่อทำปฏิกิริยากับด่างให้เข้าสู่สารละลายในรูปของโซเดียมอะลูมิเนต:
AlOOH+NaOH→NaAlO 2 +H 2 O
อัล(OH) 3 +NaOH→NaAlO 2 +2H 2 O;
SiO 2 +2NaOH→Na 2 SiO 3 +H2O;
ในสารละลายโซเดียมอะลูมิเนตและโซเดียมซิลิเกตเป็นโซเดียมอะลูมิโนซิลิเกตที่ไม่ละลายน้ำ ไททาเนียมและเหล็กออกไซด์ผ่านเข้าไปในสารตกค้างที่ไม่ละลายน้ำทำให้สารตกค้างเป็นสีแดง สารตกค้างนี้เรียกว่าโคลนแดง เมื่อละลายเสร็จแล้ว โซเดียมอะลูมิเนตที่ได้จะถูกเจือจางด้วยสารละลายด่างในขณะที่ลดอุณหภูมิลง 100 ° C
3. การแยกสารละลายอะลูมิเนตออกจากโคลนแดง มักล้างด้วยสารเพิ่มความข้นพิเศษ ด้วยเหตุนี้ โคลนสีแดงจึงตกลงมา และสารละลายอะลูมิเนตจะถูกระบายออกแล้วกรองออก (ชี้แจง) ในปริมาณที่จำกัด กากตะกอนจะถูกใช้ ตัวอย่างเช่น เป็นสารเติมแต่งสำหรับซีเมนต์ ขึ้นอยู่กับเกรดของแร่บอกไซต์ โคลนสีแดง 0.6 - 1.0 ตัน (สารตกค้างแห้ง) ตกลงบนอลูมินาที่ผลิตได้ 1 ตัน ขึ้นอยู่กับเกรดของอะลูมิเนียม
4. การสลายตัวของสารละลายอะลูมิเนต มันถูกกรองและสูบลงในภาชนะขนาดใหญ่ที่มีตัวกวน (ตัวย่อยสลาย) อะลูมิเนียมไฮดรอกไซด์ Al(OH) 3 ถูกสกัดจากสารละลายอิ่มตัวยิ่งยวดเมื่อเย็นลงจนถึง 60 °C (330 K) และกวนอย่างต่อเนื่อง เนื่องจากกระบวนการนี้ดำเนินไปอย่างช้าและไม่สม่ำเสมอ และการก่อตัวและการเติบโตของผลึกอะลูมิเนียมไฮดรอกไซด์จึงมี สำคัญมากในระหว่างการประมวลผลต่อไปจะมีการเติมไฮดรอกไซด์ที่เป็นของแข็งจำนวนมากลงในตัวย่อยสลาย - เมล็ด:
นา 2 O อัล 2 O 3 + 4H2O→Al(OH) 3 + 2NaOH;
5. การจัดสรรอะลูมิเนียมไฮดรอกไซด์และการจำแนกประเภท สิ่งนี้เกิดขึ้นในไฮโดรไซโคลนและตัวกรองสุญญากาศ ซึ่งตะกอนที่มีอนุภาค Al(OH) 3 50 - 60% แยกออกจากสารละลายอะลูมิเนต ส่วนสำคัญของไฮดรอกไซด์จะกลับสู่กระบวนการย่อยสลายเป็นวัสดุเมล็ด ซึ่งยังคงหมุนเวียนอยู่ในปริมาณที่ไม่เปลี่ยนแปลง สารตกค้างหลังจากล้างด้วยน้ำจะถูกเผา กรองก็กลับสู่การไหลเวียน (หลังจากความเข้มข้นในเครื่องระเหย - เพื่อชะล้างบอกไซต์ใหม่);
6. การคายน้ำของอะลูมิเนียมไฮดรอกไซด์ (การเผา); เป็นขั้นตอนสุดท้ายของการผลิตอลูมินา มันดำเนินการในเตาเผาแบบหมุนแบบท่อและเมื่อเร็ว ๆ นี้ในเตาเผาที่มีการเคลื่อนที่แบบปั่นป่วนของวัสดุที่อุณหภูมิ 1150 - 1300 ° C; อะลูมิเนียมไฮดรอกไซด์ดิบ ผ่านเตาโรตารี่ ทำให้แห้งและแห้ง เมื่อถูกความร้อน การเปลี่ยนแปลงโครงสร้างต่อไปนี้จะเกิดขึ้นตามลำดับ:
Al(OH) 3 → AlOOH → γ-Al 2 O 3 → α-Al 2 O 3
200 °C - 950 °C - 1200 °C.
อลูมินาที่ผ่านการเผาขั้นสุดท้ายมี 30 - 50% α-Al2O3 (คอรันดัม) ส่วนที่เหลือคือ γ-Al 2 O 2 .
วิธีนี้สกัดได้ 85 - 87% ของอลูมินาทั้งหมดที่ผลิต ส่งผลให้อลูมินามีความแข็งแรง สารประกอบเคมีด้วยจุดหลอมเหลว 2050 ° C
การได้มาซึ่งอะลูมิเนียมด้วยกระแสไฟฟ้า
การลดอิเล็กโทรไลต์ของอะลูมิเนียมออกไซด์ที่ละลายในตัวหลอมแบบไครโอไลต์จะดำเนินการที่อุณหภูมิ 950–970 °C ในเซลล์อิเล็กโทรไลต์ อิเล็กโทรไลเซอร์ประกอบด้วยอ่างที่บุด้วยบล็อกคาร์บอน ที่ด้านล่างของซึ่งมี a ไฟฟ้า. อะลูมิเนียมเหลวที่ปล่อยออกมาด้านล่างทำหน้าที่เป็นแคโทดที่หนักกว่าเกลืออิเล็กโทรไลต์ที่หลอมละลาย ดังนั้นจึงถูกรวบรวมไว้บนฐานถ่านหิน จากนั้นจึงสูบออกเป็นระยะ (รูปที่ 4) จากด้านบน คาร์บอนแอโนดจะแช่อยู่ในอิเล็กโทรไลต์ ซึ่งเผาไหม้ในบรรยากาศของออกซิเจนที่ปล่อยออกมาจากอะลูมิเนียมออกไซด์ ปล่อยคาร์บอนมอนอกไซด์ (CO) หรือคาร์บอนไดออกไซด์ (CO 2) ในทางปฏิบัติใช้แอโนดสองประเภท:
- แอโนด Zederberg ที่อบด้วยตัวเองซึ่งประกอบด้วยก้อนที่เรียกว่า "ขนมปัง" ของมวล Zederberg (ถ่านหินเถ้าต่ำที่มีน้ำมันดิน 25 - 35%) ยัดลงในเปลือกอลูมิเนียม ภายใต้การกระทำของอุณหภูมิสูงมวลขั้วบวกจะถูกเผา (เผา);
- ยิงหรือ "ต่อเนื่อง" แอโนดที่ทำจากบล็อกคาร์บอนขนาดใหญ่ (เช่น 1900 × 600 × 500 มม. น้ำหนักประมาณ 1.1 ตัน)

รูปที่ 4 - แผนผังของอิเล็กโทรไลเซอร์
ความแรงของกระแสไฟฟ้าบนอิเล็กโทรไลต์คือ 150,000 A. พวกมันเชื่อมต่อกับเครือข่ายแบบอนุกรมนั่นคือระบบ (อนุกรม) ได้มา - อิเล็กโทรไลเซอร์แถวยาว
แรงดันใช้งานบนอ่างซึ่งอยู่ที่ 4 - 5 V นั้นสูงกว่าแรงดันไฟฟ้าที่อะลูมิเนียมออกไซด์สลายตัวมาก เนื่องจากการสูญเสียแรงดันไฟฟ้าในกระบวนการนี้ย่อมหลีกเลี่ยงไม่ได้ ส่วนต่างๆระบบต่างๆ ความสมดุลของวัตถุดิบและพลังงานเมื่อได้รับอะลูมิเนียม 1 ตัน แสดงในภาพที่ 5
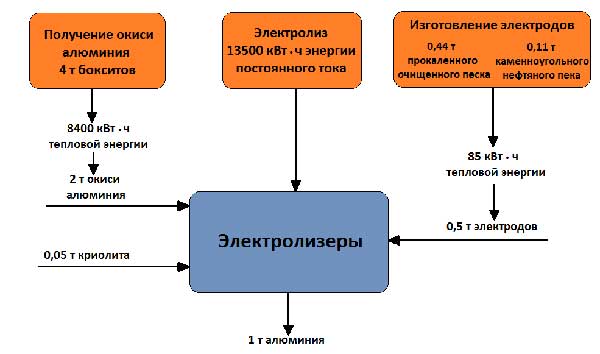
ภาพที่ 5 - ความสมดุลของวัตถุดิบและพลังงานในการผลิตอลูมิเนียม 1 ตัน
ในถังปฏิกิริยา อะลูมิเนียมออกไซด์จะถูกแปลงเป็นอะลูมิเนียมคลอไรด์ก่อน จากนั้นในอ่างที่หุ้มฉนวนอย่างแน่นหนา อิเล็กโทรไลซิสของ AlCl 3 จะถูกละลายในเกลือหลอมเหลวของ KCl หรือ NaCl คลอรีนที่ปล่อยออกมาในกระบวนการนี้จะถูกดูดออกและป้อนเพื่อรีไซเคิล อลูมิเนียมวางอยู่บนแคโทด
ข้อดีของวิธีนี้เหนืออิเล็กโทรไลซิสที่มีอยู่ของของเหลว cryolite-alumina ละลาย (Al 2 O 3 , Na 3 AlF 6 ที่ละลายใน cryolite) คือ: ประหยัดพลังงานได้มากถึง 30%; ความเป็นไปได้ของการใช้อะลูมิเนียมออกไซด์ซึ่งไม่เหมาะสำหรับอิเล็กโทรไลซิสแบบเดิม (เช่น Al 2 O 3 ที่มีปริมาณซิลิกอนสูง) แทนที่ไครโอไลต์ราคาแพงด้วยเกลือที่ถูกกว่า การกำจัดอันตรายจากการปล่อยฟลูออไรด์
รับอลูมิเนียมขัดเงา
สำหรับอะลูมิเนียม การกลั่นด้วยไฟฟ้าด้วยการสลายตัวของสารละลายเกลือในน้ำเป็นไปไม่ได้ เนื่องจากเพื่อวัตถุประสงค์บางอย่าง ระดับการทำให้อะลูมิเนียมอุตสาหกรรมบริสุทธิ์ (Al 99.5 - Al 99.8) ที่ได้จากอิเล็กโทรไลซิสของการหลอมของไครโอไลต์-อลูมินายังไม่เพียงพอ แม้แต่อะลูมิเนียมบริสุทธิ์ (Al 99.99 R) ก็ได้มาจากอะลูมิเนียมอุตสาหกรรมหรือเศษโลหะโดยการกลั่น . วิธีการกลั่นที่มีชื่อเสียงที่สุดคืออิเล็กโทรไลซิสสามชั้น
การกลั่นด้วยอิเล็กโทรไลซิสสามชั้น
ซับในด้วยแผ่นเหล็กที่ทำงานด้วยกระแสตรง (รูปที่ 6) อ่างกลั่นประกอบด้วยเตาถ่านที่มีตัวนำกระแสไฟและซับในแมกนีไซต์ที่ป้องกันความร้อน ตรงกันข้ามกับอิเล็กโทรไลซิสของไครโอไลต์-อลูมินาที่หลอมเหลว แอโนดที่นี่คือ ตามกฎแล้ว โลหะกลั่นที่หลอมเหลว (ชั้นแอโนดที่ต่ำกว่า) อิเล็กโทรไลต์ประกอบด้วยฟลูออไรด์บริสุทธิ์หรือส่วนผสมของแบเรียมคลอไรด์และอะลูมิเนียมและโซเดียมฟลูออไรด์ (ชั้นกลาง) อะลูมิเนียมที่ละลายจากชั้นแอโนดในอิเล็กโทรไลต์จะถูกปล่อยออกมาเหนืออิเล็กโทรไลต์ (ชั้นแคโทดด้านบน) โลหะบริสุทธิ์ทำหน้าที่เป็นแคโทด กระแสไฟฟ้าถูกส่งไปยังชั้นแคโทดโดยอิเล็กโทรดกราไฟท์

รูปที่ 6 - ไดอะแกรมของเซลล์อิเล็กโทรไลต์พร้อมเตาด้านหน้าสำหรับการกลั่นอลูมิเนียม (ตาม Fulda - Ginzberg)
1 - อลูมิเนียมละลาย; 2 – อิเล็กโทรไลต์; 3 - อลูมิเนียมกลั่นความถี่สูง 4 – แคโทดกราไฟท์; 5 - ผนังแมกนีไซต์; 6 - แตรหน้า; 7 - ชั้นฉนวน; 8 - ฉนวนด้านข้าง; 9 - เตาถ่าน; 10 – ตัวนำแอโนด; 11 - การแยกเตาไฟ; 12 - กล่องเหล็ก; 13 - ปก
อ่างทำงานที่ 750 - 800 ° C การใช้พลังงาน 20 kWh ต่อ 1 กก อลูมิเนียมบริสุทธิ์กล่าวคือค่อนข้างสูงกว่าอิเล็กโทรลิซิสอะลูมิเนียมทั่วไป
โลหะแอโนดประกอบด้วย 25-35% Cu; 7 – 12% สังกะสี; 6 – 9% ศรี; มากถึง 5% Fe และแมงกานีส นิกเกิล ตะกั่ว และดีบุกจำนวนเล็กน้อย ส่วนที่เหลือ (40 - 55%) เป็นอะลูมิเนียม โลหะหนักและซิลิกอนทั้งหมดยังคงอยู่ในชั้นแอโนดระหว่างการกลั่น การปรากฏตัวของแมกนีเซียมในอิเล็กโทรไลต์นำไปสู่การเปลี่ยนแปลงที่ไม่พึงประสงค์ในองค์ประกอบของอิเล็กโทรไลต์หรือทำให้เกิดตะกรันที่รุนแรง ในการกำจัดแมกนีเซียม ตะกรันที่มีแมกนีเซียมจะได้รับการบำบัดด้วยฟลักซ์หรือคลอรีนที่เป็นก๊าซ
ผลจากการกลั่นจะได้อะลูมิเนียมบริสุทธิ์ (99.99%) และผลิตภัณฑ์คัดแยก (ผลิตภัณฑ์ Ziger) ซึ่งประกอบด้วยโลหะหนักและซิลิกอน และถูกแยกออกในรูปของสารละลายอัลคาไลน์และกากผลึก สารละลายอัลคาไลน์เป็นของเสีย และกากที่เป็นของแข็งจะถูกใช้เพื่อขจัดความเป็นกรด
อลูมิเนียมกลั่นมักมีองค์ประกอบดังนี้ %: Fe 0.0005 - 0.002; ศรี 0.002 - 0.005; ลูกบาศ์ก 0.0005 - 0.002; สังกะสี 0.0005 - 0.002; ร่องรอยมิลลิกรัม; อัลพักผ่อน
อลูมิเนียมกลั่นถูกแปรรูปเป็นผลิตภัณฑ์กึ่งสำเร็จรูปในองค์ประกอบที่ระบุหรือผสมกับแมกนีเซียม (ตารางที่ 1)
ตารางที่ 1 - องค์ประกอบทางเคมีอะลูมิเนียมบริสุทธิ์สูงและอะลูมิเนียมขั้นต้นตามมาตรฐาน DIN 1712 แผ่น 1
|
สิ่งเจือปนที่อนุญาต*, % |
||||||||
|
รวมทั้ง |
||||||||
* เท่าที่เป็นไปได้ที่จะกำหนด วิธีการทั่วไปการวิจัย.
** อะลูมิเนียมบริสุทธิ์สำหรับงานวิศวกรรมไฟฟ้า (ตัวนำอะลูมิเนียม) มีจำหน่ายในรูปของอะลูมิเนียมปฐมภูมิ 99.5 ที่มีปริมาณไม่เกิน 0.03% (Ti + Cr + V + Mn) กำหนดในกรณีนี้เป็น E-A1 หมายเลขวัสดุ 3.0256 มิฉะนั้นจะเป็นไปตาม VDE-0202
การกลั่นด้วยสารประกอบเชิงซ้อนออร์กาโนอะลูมิเนียมและการหลอมโซน
อะลูมิเนียมที่มีความบริสุทธิ์สูงเกรด A1 99.99 R ได้จากการกลั่นอิเล็กโทรลิซิสของอะลูมิเนียมบริสุทธิ์หรืออะลูมิเนียมบริสุทธิ์เชิงพาณิชย์โดยใช้สารประกอบออร์กาโนอะลูมิเนียมที่ซับซ้อนของอะลูมิเนียมเป็นอิเล็กโทรไลต์ อิเล็กโทรลิซิสเกิดขึ้นที่อุณหภูมิประมาณ 1,000 องศาเซลเซียสระหว่างอิเล็กโทรดอะลูมิเนียมที่เป็นของแข็ง และหลักการคล้ายกับอิเล็กโทรไลซิสสำหรับการกลั่นของทองแดง ลักษณะของอิเล็กโทรไลต์กำหนดความจำเป็นในการทำงานโดยไม่มีอากาศและที่ความหนาแน่นกระแสไฟต่ำ
อิเล็กโทรไลซิสสำหรับการกลั่นชนิดนี้ ซึ่งใช้ในตอนแรกเฉพาะในห้องปฏิบัติการเท่านั้น ได้ดำเนินการในระดับอุตสาหกรรมขนาดเล็กแล้ว - ผลิตโลหะหลายตันต่อปี ระดับการทำให้บริสุทธิ์ของโลหะที่ได้คือ 99.999 -99.9999% ขอบเขตที่เป็นไปได้ในการใช้งานสำหรับโลหะที่มีความบริสุทธิ์นี้ ได้แก่ วิศวกรรมไฟฟ้าและอิเล็กทรอนิกส์ด้วยการแช่แข็ง
สามารถใช้วิธีการกลั่นที่พิจารณาแล้วในการชุบด้วยไฟฟ้า
มากไปกว่านั้น ความบริสุทธิ์สูง- ในนามสูงถึง A1 99.99999 - สามารถรับได้จากการหลอมโซนภายหลังของโลหะ เมื่อแปรรูปอะลูมิเนียมที่มีความบริสุทธิ์สูงให้เป็นผลิตภัณฑ์กึ่งสำเร็จรูป แผ่นหรือลวด จำเป็นต้องใช้ความระมัดระวังเป็นพิเศษเนื่องจากอุณหภูมิการตกผลึกใหม่ของโลหะ คุณสมบัติที่โดดเด่นของโลหะกลั่นคือการนำไฟฟ้าสูงในบริเวณที่มีอุณหภูมิในการแช่แข็ง
บทนำ
อลูมิเนียมเป็นโลหะที่สำคัญที่สุด โดยมีปริมาณการผลิตสูงกว่าโลหะอื่นๆ ที่ไม่ใช่โลหะมาก และเป็นอันดับสองรองจากการผลิตเหล็กเท่านั้น อัตราการเติบโตที่สูงของการผลิตอะลูมิเนียมเกิดจากเอกลักษณ์เฉพาะตัว คุณสมบัติทางกายภาพและทางเคมีเนื่องจากมีการใช้งานอย่างกว้างขวางในด้านวิศวกรรมไฟฟ้า อุตสาหกรรมอากาศยานและยานยนต์ การขนส่ง เครื่องใช้ในครัวเรือน การก่อสร้าง บรรจุภัณฑ์ ผลิตภัณฑ์อาหารเป็นต้น
อุตสาหกรรมอลูมิเนียมของรัสเซียสร้างขึ้นใน สมัยโซเวียตครองตำแหน่งที่โดดเด่นในการผลิตโลหะที่ไม่ใช่เหล็กในประเทศและอยู่ในอันดับที่สองของโลกในแง่ของการผลิตโลหะ ที่ ปีที่แล้ว, โดยอาศัยอำนาจตาม สาเหตุที่ทราบ, อุปกรณ์สำหรับการผลิตอลูมิเนียมในทางปฏิบัติไม่ได้รับการปรับปรุงให้ทันสมัย, เทคโนโลยีของอิเล็กโทรไลซิสไม่ได้รับการปรับปรุง, ปริมาณของการวิจัยทางวิทยาศาสตร์ลดลงอย่างไม่อาจยอมรับได้และล้าหลังอย่างเห็นได้ชัดหลังประเทศที่พัฒนาแล้ว ในขณะเดียวกัน อุปกรณ์ต่าง ๆ ก็กำลังได้รับการปรับปรุงให้ทันสมัยอย่างกว้างขวางในต่างประเทศ เทคโนโลยีกำลังได้รับการปรับปรุง ซึ่งทำให้สามารถเพิ่มขึ้นอย่างรวดเร็ว ประสิทธิภาพทางเศรษฐกิจและความปลอดภัยต่อสิ่งแวดล้อมในการผลิตอะลูมิเนียม
เมื่อเร็ว ๆ นี้ วิศวกรรมเครื่องกลต้องการโลหะเบาเพิ่มมากขึ้น โดยเฉพาะอย่างยิ่งในอุตสาหกรรมอากาศยานและการขนส่งทางรถไฟ ดังนั้นการพัฒนาวิธีการใหม่ที่ประหยัดกว่าในการรับอลูมิเนียมและการปรับปรุงวิธีการที่มีอยู่จึงมีความสำคัญอย่างยิ่ง
1. ประวัติความเป็นมาของการพัฒนาอุตสาหกรรมอลูมิเนียม
ปัจจุบันอะลูมิเนียมเป็นอันดับหนึ่งในกลุ่มโลหะที่ไม่ใช่เหล็กในแง่ของปริมาณการผลิต และการผลิตก็มีการขยายตัวอย่างต่อเนื่อง
ในอดีต การกล่าวถึงอะลูมิเนียมเป็นโลหะครั้งแรกเกิดขึ้นในงานเขียนของโรมันในศตวรรษแรก ที่ สารานุกรมที่มีชื่อเสียง"Historia naturalis" สามารถติดตามเรื่องราวต่อไปนี้ อยู่มาวันหนึ่ง นักอัญมณีชาวโรมันได้รับอนุญาตให้แสดงจานอาหารค่ำที่ทำด้วยโลหะใหม่ให้แก่จักรพรรดิทิเบเรียส จานนั้นเบามากและส่องประกายเหมือนเงิน ช่างอัญมณีบอกกับจักรพรรดิว่าเขาสกัดโลหะจากดินเหนียวธรรมดา เขายังยืนยันกับจักรพรรดิว่ามีเพียงเขาและเหล่าทวยเทพเท่านั้นที่รู้วิธีเอาโลหะจากดินเหนียว จักรพรรดิทรงสนใจอย่างมาก อย่างไรก็ตาม เขาตระหนักในทันทีว่าคลังสมบัติทั้งหมดของเขา ซึ่งประกอบด้วยทองคำและเงิน จะทรุดโทรมหากผู้คนเริ่มผลิตโลหะเบานี้จากดินเหนียว ดังนั้น แทนที่จะเป็นรางวัลที่นักอัญมณีคาดหวัง เขากลับถูกตัดศีรษะ
ไม่มีใครรู้ว่าเรื่องนี้จริงแค่ไหน แต่เหตุการณ์ที่อธิบายไว้เกิดขึ้น 2,000 ปีก่อนการค้นพบวิธีการผลิตอลูมิเนียมโดยมนุษย์ สิ่งนี้เกิดขึ้นในปี 1825 เมื่อนักฟิสิกส์ชาวเดนมาร์ก H. Oersted ได้รับอะลูมิเนียมโลหะหลายมิลลิกรัมโดยการลดความร้อนของอะลูมิเนียมคลอไรด์ด้วยโพแทสเซียมอะมัลกัม
ความยากลำบากในการรับอลูมิเนียมเกิดขึ้นจากปัจจัยดังต่อไปนี้:
อลูมิเนียมมีความสัมพันธ์สูงต่อออกซิเจน อะลูมิเนียมสามารถลดลงได้ด้วยคาร์บอนไดออกไซด์ที่อุณหภูมิประมาณ 2,000 องศาเซลเซียส อย่างไรก็ตาม ที่อุณหภูมิ 1200 องศาเซลเซียส คาร์บอนจะทำปฏิกิริยากับอะลูมิเนียม ทำให้เกิดคาร์ไบด์
ศักยภาพทางเคมีไฟฟ้าของอะลูมิเนียมสูง (-1.67V) เป็นไปไม่ได้ที่จะได้รับอะลูมิเนียมจากสารละลายที่เป็นน้ำ เนื่องจากกระบวนการวิวัฒนาการของไฮโดรเจน (การสลายตัวของน้ำ) จะดำเนินต่อไปที่ขั้วลบ
จุดหลอมเหลวสูงของอลูมินา (2050 องศาเซลเซียส) ซึ่งไม่รวมความเป็นไปได้ของการแยกอิเล็กโทรไลซิสของอลูมินาหลอมเหลว
อุตสาหกรรมการผลิตอลูมิเนียมมีความเกี่ยวข้องกับชื่อของ Henri Saint-Clair Deville ชาวฝรั่งเศส เขาตระหนักดีถึงการทดลองของ G. Oersted และนักวิทยาศาสตร์อีกคนหนึ่งคือ F. Wehler ซึ่งในปี 1827 สามารถแยกเม็ดอลูมิเนียมออกได้ สาเหตุของความล้มเหลวของ F. Wöhler คือเมล็ดพืชในอากาศเหล่านี้ถูกปกคลุมด้วยฟิล์มอะลูมิเนียมออกไซด์ที่บางที่สุดในทันที
ก่อนอื่น A.S.-K. ในกระบวนการรับโลหะ Deville แทนที่โพแทสเซียมด้วยโซเดียมที่ถูกกว่าและทำการทดลองในห้องปฏิบัติการในขนาดใหญ่ อะลูมิเนียมคลอไรด์ที่ได้นั้นถูกบรรจุลงในท่อเหล็กขนาดใหญ่ ซึ่งบรรจุในภาชนะด้วย โลหะโซเดียม. ในระหว่างการให้ความร้อน อะลูมิเนียมคลอไรด์ทำปฏิกิริยากับโซเดียมในเฟสของแก๊ส และอนุภาคอะลูมิเนียมจะตกลงไปที่ด้านล่างของท่อ ธัญพืชที่เกิดขึ้นจากปฏิกิริยาถูกเก็บรวบรวมอย่างระมัดระวัง หลอมเหลว และได้รับแท่งโลหะ
วิธีใหม่ในการผลิตอะลูมิเนียมได้รับการพิสูจน์แล้วว่าต้องใช้แรงงานมาก นอกจากนี้ ปฏิกิริยาระหว่างไออะลูมิเนียมคลอไรด์กับโซเดียมมักเกิดการระเบิดขึ้น ในสภาพห้องปฏิบัติการ สิ่งนี้ไม่ก่อให้เกิดอันตรายร้ายแรง แต่ในสภาพโรงงาน อาจทำให้เกิดภัยพิบัติได้ ถาม. Deville แทนที่อะลูมิเนียมคลอไรด์ด้วยส่วนผสมของ AlCl 3 กับ NaCl ตอนนี้ผู้เข้าร่วมปฏิกิริยาอยู่ในสถานะหลอมเหลว การระเบิดหยุดลง แต่ที่สำคัญที่สุด แทนที่จะต้องเก็บเม็ดโลหะเล็กๆ ด้วยมือ พวกเขาได้รับอะลูมิเนียมเหลวจำนวนมาก
การทดลองที่โรงงาน Javel ประสบความสำเร็จ ในปี พ.ศ. 2398 ได้โลหะแท่งแรกที่มีน้ำหนัก 6–8 กิโลกรัม
กระบองของการผลิตอลูมิเนียมโดยวิธีทางเคมียังคงดำเนินต่อไปโดยนักวิทยาศาสตร์ชาวรัสเซีย N. N. Beketov เขาทำปฏิกิริยาโต้ตอบระหว่างไครโอไลต์ (Na 3 AlF 6) และแมกนีเซียม วิธีการของ N. N. Beketov แตกต่างกันเล็กน้อยจากวิธีการของ A.S.-K. Deville แต่ง่ายกว่า ในเมือง Gmelingem ของเยอรมนี ในปี 1885 โรงงานแห่งนี้ถูกสร้างขึ้นโดยใช้วิธีการของ N. N. Beketov โดยได้รับอะลูมิเนียม 58 ตันในห้าปี คิดเป็นมากกว่าหนึ่งในสี่ของการผลิตโลหะทั้งโลกด้วยวิธีการทางเคมีในช่วงปี 1854 ถึง พ.ศ. 2433
การได้มาซึ่งอะลูมิเนียมด้วยวิธีการทางเคมีไม่สามารถให้โลหะราคาถูกแก่อุตสาหกรรมได้ มันไม่เกิดผลและไม่ให้อะลูมิเนียมบริสุทธิ์ที่ปราศจากสิ่งเจือปน สิ่งนี้ทำให้นักวิจัย ประเทศต่างๆให้โลกมองหาวิธีใหม่ในการผลิตอะลูมิเนียม
กระแสไฟฟ้ามาช่วยนักวิทยาศาสตร์ ย้อนกลับไปในปี 1808 G. Davy พยายามย่อยสลายอลูมินาโดยใช้แบตเตอรี่ไฟฟ้าอันทรงพลัง แต่ก็ไม่เป็นผล เกือบ 50 ปีต่อมา R. Bunsen และ A.S.-K. Deville ดำเนินการอิเล็กโทรไลซิสของส่วนผสมของอะลูมิเนียมและโซเดียมคลอไรด์อย่างอิสระ พวกเขาโชคดีกว่ารุ่นก่อนและสามารถหาอลูมิเนียมขนาดเล็กได้ อย่างไรก็ตามในสมัยนั้นยังไม่มีแหล่งไฟฟ้าราคาถูกและมีประสิทธิภาพเพียงพอ ดังนั้นอิเล็กโทรไลซิสของอะลูมิเนียมจึงเป็นเพียงความสนใจทางทฤษฎีเท่านั้น
ในปีพ.ศ. 2410 ไดนาโมถูกประดิษฐ์ขึ้น และในไม่ช้าพวกเขาก็เรียนรู้วิธีส่งกระแสไฟฟ้าในระยะทางไกล ไฟฟ้าเริ่มรุกอุตสาหกรรม
ในปี พ.ศ. 2429 P. Héroult ในฝรั่งเศสและ C. Hall ในสหรัฐอเมริกาเกือบจะพร้อมกันได้วางรากฐานสำหรับวิธีการผลิตอะลูมิเนียมสมัยใหม่ โดยเสนอให้ได้มาโดยวิธีอิเล็กโทรไลซิสของอลูมินาที่ละลายในไครโอไลต์หลอมเหลว (วิธี Hall-Hérault) จากนี้ไป วิธีการใหม่การผลิตอะลูมิเนียมเริ่มมีการพัฒนาอย่างรวดเร็ว ซึ่งอำนวยความสะดวกโดยการปรับปรุงวิศวกรรมไฟฟ้า ตลอดจนการพัฒนาวิธีการสกัดอลูมินาจากแร่อะลูมิเนียม นักวิทยาศาสตร์ชาวรัสเซีย K.I. Bayer, D. A. Penyakov, A. N. Kuznetsov, A. N. Kuznetsov, E. I. Zhukovsky, A. A. Yakovkin มีส่วนสนับสนุนอย่างมากในการพัฒนาการผลิตอลูมินา, A. A. Yakovkin และอื่น ๆ ซาร์รัสเซียไม่มีอุตสาหกรรมอลูมิเนียมเป็นของตัวเอง อย่างไรก็ตาม การวิจัยเชิงทฤษฎีครั้งแรกในสาขาอะลูมิเนียมอิเล็กโทรไลซิสนั้นเป็นของนักวิทยาศาสตร์ชาวรัสเซียผู้โดดเด่น ผู้ก่อตั้ง electrometallurgy ของโลหะนอกกลุ่มเหล็กในประเทศของเรา ศ. ป.ล. Fedotiev ในปี พ.ศ. 2455 ร่วมกับ V.P. Ilyinsky ตีพิมพ์ผลงาน "Experimental; Research on Electrometallurgy of Aluminium" ซึ่งได้รับการแปลเป็นหลายภาษาทันที ภาษาต่างประเทศและกลายเป็นหนังสืออ้างอิงสำหรับนักโลหะวิทยาทั่วโลก พีพี Fedoteev และ Ilyinsky ที่สถาบันโพลีเทคนิคเซนต์ปีเตอร์สเบิร์ก (มหาวิทยาลัยเทคนิคแห่งรัฐเซนต์ปีเตอร์สเบิร์ก) ได้ทำการวิจัยอย่างละเอียดเกี่ยวกับการเลือกองค์ประกอบที่เหมาะสมที่สุดของอิเล็กโทรไลต์ และยังพบว่าความสามารถในการละลายของอลูมินาในไครโอไลต์และอุณหภูมิการตกผลึกของการเติม ของโซเดียม อะลูมิเนียม และแคลเซียมฟลูออไรด์
เมื่อวันที่ 28 มีนาคม พ.ศ. 2472 บทความตีพิมพ์ในหนังสือพิมพ์ Leningradskaya Pravda ซึ่งมีรายงานว่าได้รับโลหะอลูมิเนียม 8 กิโลกรัมจากการอาบน้ำครั้งเดียวเป็นครั้งแรกที่โรงงานนำร่องของโรงงาน Krasny Vyborzhets นี่เป็นจุดเริ่มต้นของอุตสาหกรรมอลูมิเนียมของเรา
ในปี พ.ศ. 2474 สถาบันวิจัยอุตสาหกรรมอะลูมิเนียม-แมกนีเซียม (VAMI) ก่อตั้งขึ้นในปี 2475 Volkhovsky เปิดตัวและในปี 1933 - โรงงานอลูมิเนียม Dnipro เนื่องจาก อุตสาหกรรมอลูมิเนียมเริ่มเจริญงอกงามตามส่วนต่างๆ ของประเทศ
2. พื้นฐานของอิเล็กโทรไลซิสของไครโอไลต์-อลูมินาละลาย
อิเล็กโทรไลซิสของไครโอไลต์-อลูมินาหลอมละลายเป็นวิธีหลักในการรับอะลูมิเนียม แม้ว่าบางส่วนจะ โลหะผสมอลูมิเนียมผลิตโดยกระบวนการอิเล็กโทรเทอร์มอล
อิเล็กโทรไลเซอร์อุตสาหกรรมเครื่องแรกมีไว้สำหรับกระแสสูงถึง 0.6 kA และในอีก 100 ปีข้างหน้าจะเพิ่มขึ้นเป็น 300 kA อย่างไรก็ตาม สิ่งนี้ไม่ได้ทำให้เกิดการเปลี่ยนแปลงที่สำคัญกับพื้นฐานของกระบวนการผลิต
รูปแบบทั่วไปของการผลิตอลูมิเนียมแสดงในรูปที่ 2.1. หน่วยหลักคืออิเล็กโทรไลเซอร์ อิเล็กโทรไลต์เป็นไครโอไลต์ที่หลอมละลายด้วยอะลูมิเนียมฟลูออไรด์ส่วนเกินเล็กน้อย ซึ่งอลูมินาจะละลาย กระบวนการนี้ดำเนินการที่ความเข้มข้นแปรผันของอลูมินาตั้งแต่ประมาณ 1 ถึง 8% (น้ำหนัก) จากด้านบน คาร์บอนแอโนดถูกหย่อนลงไปในอ่าง จุ่มลงในอิเล็กโทรไลต์บางส่วน แอโนดบูชายัญมีสองประเภทหลัก: อบเองและอบล่วงหน้า อดีตใช้ความร้อนของอิเล็กโทรไลซิสสำหรับการคั่วมวลแอโนดซึ่งประกอบด้วยส่วนผสมของสารเติมโค้กและสารยึดเกาะ, ระยะห่าง แอโนดอบเป็นส่วนผสมของโค้กและพิตช์ที่เตรียมไว้ล่วงหน้า เทคโนโลยีสำหรับการผลิตมวลแอโนดและแอโนดที่อบได้อธิบายไว้โดยละเอียดในเอกสาร (ดูตัวอย่าง)
ข้าว. 2.1. โครงการผลิตอลูมิเนียมจากอลูมินา
อะลูมิเนียมหลอมเหลวที่อุณหภูมิอิเล็กโทรไลซิส (950–960°C) จะหนักกว่าอิเล็กโทรไลต์และอยู่ที่ด้านล่างของอิเล็กโทรไลเซอร์ การหลอมของไครโอไลต์-อลูมินานั้นรุนแรงมาก ซึ่งสามารถต้านทานได้ด้วยคาร์บอนและวัสดุใหม่บางชนิด ในจำนวนนี้ทำเยื่อบุด้านในของอิเล็กโทรไลเซอร์
ในการแปลง AC เป็น DC บน โรงงานสมัยใหม่ใช้วงจรเรียงกระแสเซมิคอนดักเตอร์ที่มีแรงดันไฟฟ้า 850V และอัตราส่วนการแปลง 98.5% ติดตั้งในสถานีย่อยตัวแปลงซิลิคอน (KPP) หนึ่งหน่วยเรียงกระแสให้กระแสสูงถึง 63 kA จำนวนหน่วยดังกล่าวขึ้นอยู่กับความแรงของกระแสที่ต้องการเนื่องจากเชื่อมต่อแบบขนานทั้งหมด
กระบวนการที่เกิดขึ้นในอิเล็กโทรไลเซอร์ประกอบด้วยการสลายตัวด้วยไฟฟ้าของอลูมินาที่ละลายในอิเล็กโทรไลต์ อลูมิเนียมถูกปล่อยออกมาบนแคโทดอลูมิเนียมเหลวซึ่งถูกเทออกเป็นระยะโดยใช้ทัพพีสูญญากาศและส่งไปยังแผนกหล่อเพื่อเทหรือเครื่องผสมซึ่งขึ้นอยู่กับวัตถุประสงค์ต่อไปของโลหะโลหะผสมที่มีซิลิกอนแมกนีเซียมแมงกานีสทองแดง มีการเตรียมหรือกลั่น ที่ขั้วบวก คาร์บอนจะถูกออกซิไดซ์โดยออกซิเจนที่ปล่อยออกมา ก๊าซแอโนดไอเสียเป็นส่วนผสมของ CO 2 และ CO
อิเล็กโทรไลเซอร์มักจะติดตั้งที่พักพิงที่กำจัดก๊าซไอเสียและระบบทำความสะอาด ซึ่งจะช่วยลดการปล่อยสารอันตรายสู่ชั้นบรรยากาศ กระบวนการทางเทคโนโลยีกำหนดให้ที่พักพิงต้องผนึกอย่างผนึกแน่นเพื่อให้แน่ใจว่าการดูดก๊าซเข้าสู่ตัวสะสมโดยใช้พัดลม ก๊าซที่ถูกกำจัดออกจากอิเล็กโทรไลเซอร์ถูกครอบงำโดยคาร์บอนไดออกไซด์ (คาร์บอนมอนอกไซด์ส่วนใหญ่ถูกเผาไหม้เหนืออิเล็กโทรไลต์หรือในเตาพิเศษหลังจากระฆังเก็บก๊าซ) ไนโตรเจน ออกซิเจน ฟลูออไรด์ที่เป็นก๊าซและของแข็ง และอนุภาคของฝุ่นอลูมินา มีการใช้แผนการทางเทคโนโลยีที่หลากหลายเพื่อลบออกและส่งคืนสู่กระบวนการ
อิเล็กโทรไลเซอร์สมัยใหม่ติดตั้งระบบจ่ายอลูมินาอัตโนมัติ (AAF) โดยมีระยะเวลาโหลด 10–30 นาที
ปฏิกิริยาโดยรวมที่เกิดขึ้นในอิเล็กโทรไลเซอร์สามารถแสดงได้โดยสมการ
ดังนั้นในทางทฤษฎีจะใช้อลูมินาและแอโนดคาร์บอนสำหรับกระบวนการอิเล็กโทรลิซิสเช่นเดียวกับพลังงานไฟฟ้าที่จำเป็นไม่เพียง แต่สำหรับการดำเนินการตามกระบวนการอิเล็กโทรไลต์เท่านั้น - การสลายตัวของอลูมินา แต่ยังเพื่อรักษาอุณหภูมิการทำงานที่สูง ในทางปฏิบัติยังมีการบริโภคเกลือฟลูออไรด์จำนวนหนึ่งซึ่งระเหยและถูกดูดซึมเข้าสู่เยื่อบุ ในการรับอลูมิเนียม 1 ตัน คุณต้อง:
การผลิตอะลูมิเนียมเป็นหนึ่งในกระบวนการที่ใช้พลังงานมากที่สุด ดังนั้นโรงถลุงอะลูมิเนียมจึงถูกสร้างขึ้นใกล้กับแหล่งพลังงาน
วัสดุทั้งหมดที่เข้าสู่อิเล็กโทรไลซิสต้องมี จำนวนเงินขั้นต่ำสิ่งเจือปนที่ให้ผลบวกทางไฟฟ้ามากกว่าอะลูมิเนียม (เหล็ก ซิลิกอน ทองแดง ฯลฯ) เนื่องจากสิ่งเจือปนเหล่านี้เกือบจะผ่านเข้าไปในโลหะระหว่างอิเล็กโทรลิซิสเกือบทั้งหมด
3. ทางเลือกอื่นในการรับอะลูมิเนียม
วิธีทางอุตสาหกรรมในการผลิตอะลูมิเนียมโดยอิเล็กโทรไลซิสของไครโอไลต์-อลูมินาที่หลอมเหลว แม้จะใช้งานเป็นเวลานานก็ตาม ข้อบกพร่องที่สำคัญ: การใช้พลังงานจำเพาะสูง การกำจัดโลหะจำเพาะต่ำและอายุการใช้งานของอิเล็กโทรไลเซอร์ ค่าแรงและต้นทุนทุนสูง การปล่อยสารอันตรายสู่บรรยากาศ และอื่นๆ อีกมากมาย ในการนี้เสนอวิธีอื่นในการผลิตอลูมิเนียม ลองพิจารณาบางส่วนของพวกเขา
3.1. การผลิตโลหะผสมอะลูมิเนียม-ซิลิกอนด้วยความร้อนด้วยไฟฟ้า
เป็นไปไม่ได้ที่จะได้อะลูมิเนียมบริสุทธิ์โดยการลดออกไซด์โดยตรง กระบวนการคาร์บอเทอร์มิกต้องใช้อุณหภูมิสูง (ประมาณ 2,000 องศาเซลเซียส) เพื่อลดอลูมินา และในกรณีที่ไม่มีส่วนประกอบที่เป็นโลหะผสม โลหะจะจับกับคาร์บอน ทำให้อะลูมิเนียมคาร์ไบด์ (A1 4 C 3) เป็นที่ทราบกันดีอยู่แล้วว่าอะลูมิเนียมคาร์ไบด์และอะลูมิเนียมสามารถละลายได้ซึ่งกันและกันและเกิดเป็นส่วนผสมที่ทนไฟได้มาก นอกจากนี้ A1 4 C 3 ละลายใน A1 2 O 3 ดังนั้นจากการลดลงของอะลูมิเนียมออกไซด์ด้วยคาร์บอน ส่วนผสมของอะลูมิเนียม คาร์ไบด์และออกไซด์จึงมีจุดหลอมเหลวสูง โดยปกติแล้วจะไม่สามารถปลดปล่อยมวลดังกล่าวออกจากเตาเผาได้ แม้ว่าจะสามารถทำได้ แต่ค่าใช้จ่ายในการแยกก็จะสูง
ในประเทศของเรา เป็นครั้งแรกในโลกที่วิธีการผลิตซิลิโคอะลูมิเนียม (โลหะผสมอะลูมิเนียม-ซิลิกอน) ได้รับการพัฒนาและดำเนินการในระดับอุตสาหกรรมด้วยตัวชี้วัดทางเทคนิคและเศรษฐกิจที่สูงเพียงพอ
รูปแบบเทคโนโลยีทั่วไปสำหรับการผลิตโลหะผสมอลูมิเนียม - ซิลิกอนแสดงในรูปที่ 3.1. นอกจากดินขาว (Al 2 O 3 × 2 SiO 2 × 2H 2 O), ไคยาไนต์ (Al 2 O 3 × SiO 2), distensillimanites (Al 2 O 3 × SiO 2) และแร่บอกไซต์เหล็กต่ำสามารถใช้เป็นวัตถุดิบได้
โลหะผสมหลังจากการถลุงด้วยไฟฟ้าถูกจ่ายให้เพื่อทำให้บริสุทธิ์จากสิ่งเจือปนที่ไม่ใช่โลหะ ในการทำเช่นนี้จะมีการจัดหาฟลักซ์ซึ่งประกอบด้วยส่วนผสมของไครโอไลต์และโซเดียมคลอไรด์ซึ่งทำให้สิ่งสกปรกเหล่านี้เปียกและ "รวบรวม" ซิลิโคอะลูมิเนียมกลั่นมีองค์ประกอบเฉลี่ย (%): A1 - 61; ศรี - 36; เฟ - 1.7; ที - 0.6; Zr - 0.5; แคลิฟอร์เนีย - 0.7. โลหะผสมนี้ไม่เหมาะสำหรับการผลิตซิลูมินและต้องการการทำให้บริสุทธิ์จากเหล็ก วิธีการทำให้บริสุทธิ์ที่พบมากที่สุดคือแมงกานีสซึ่งก่อให้เกิดสารประกอบระหว่างโลหะที่ทนไฟด้วยธาตุเหล็ก

ข้าว. 3.1. โครงการทั่วไปสำหรับการผลิตโลหะผสมอลูมิเนียม - ซิลิกอน
โลหะผสมที่ได้จะเจือจางด้วยอะลูมิเนียมอิเล็กโทรไลต์ทางเทคนิคหรืออะลูมิเนียมทุติยภูมิให้เป็นองค์ประกอบที่สอดคล้องกับเกรดต่างๆ ของซิลูมิน และหล่อเป็นแท่ง
ข้อดีของวิธีการนี้ได้ซิลูมินมากกว่าฟิวชั่น อะลูมิเนียมอิเล็กโทรไลต์ด้วยผลึกซิลิกอนมีดังนี้: กำลังสูงของหน่วยเดียว - เตาเผาที่ทันสมัยมีกำลัง 22.5 MB × A ซึ่งสูงกว่าพลังของอิเล็กโทรไลต์ประมาณ 30 เท่าโดย 160 kA และทำให้ปริมาณการขนส่งลดลง , ลดต้นทุนทุนและค่าแรง; การใช้วัตถุดิบที่มีโมดูลซิลิกอนต่ำซึ่งมีปริมาณสำรองค่อนข้างมาก
ในทางทฤษฎี อลูมิเนียมบริสุทธิ์สามารถแยกได้จากโลหะผสมอะลูมิเนียม-ซิลิกอนด้วยวิธีการต่างๆ อย่างไรก็ตาม เนื่องจากความซับซ้อนของฮาร์ดแวร์และการออกแบบเทคโนโลยีในอุตสาหกรรม วิธีการเหล่านี้จึงไม่ได้นำมาใช้ในปัจจุบัน
3.2. กระบวนการซับฮาโลเจน
เป็นที่ทราบกันดีว่าหากส่วนผสมของเฮไลด์และอะลูมิเนียมที่ปนเปื้อนถูกทำให้ร้อน อะลูมิเนียมบริสุทธิ์จะถูกปล่อยออกมาเมื่ออุณหภูมิลดลง การค้นพบนี้จุดประกายความสนใจในระบบอะลูมิเนียม-อะลูมิเนียมเฮไลด์ พบว่าอะลูมิเนียมโลหะทำปฏิกิริยากับ AlX 3 (โดยที่ X คือฮาโลเจน) ที่อุณหภูมิสูง ก่อตัวเป็นอะลูมิเนียมซับฮาไลด์:
![]()
เนื่องจากอะลูมิเนียมซับฮาไลด์เป็นผลิตภัณฑ์ที่เป็นก๊าซ สมดุลจะเปลี่ยนไปทางซ้ายเมื่ออุณหภูมิลดลง ตัวอย่างเช่น สามารถเตรียม A1C1(G) จาก Al และ AlC1 3 ในเขตปฏิกิริยาที่อุณหภูมิค่อนข้างสูง จากนั้นจึงถ่ายเทเป็นไอไปยังบริเวณที่เย็นกว่าซึ่งแปรผันเป็นอะลูมิเนียมบริสุทธิ์และอะลูมิเนียมคลอไรด์ ค่าคงที่สมดุลสำหรับระบบ A1 - A1C1 3 นั้นสูงกว่าสำหรับระบบ A1 - A1F 3 ดังนั้นจึงสามารถใช้ระบบคลอไรด์สำหรับกระบวนการทางอุตสาหกรรมได้ อุณหภูมิการก่อตัวของซับคลอไรด์อยู่ที่ประมาณ 1300 องศาเซลเซียสที่ความดันบรรยากาศ กระบวนการนี้น่าสนใจเป็นพิเศษสำหรับการแยกอะลูมิเนียมออกจากโลหะผสม เนื่องจากอะลูมิเนียมเฮไลด์ทำปฏิกิริยากับอะลูมิเนียมและแทบไม่เกิดปฏิกิริยากับโลหะอื่นๆ ส่วนใหญ่ ปัญหาเกิดขึ้นเฉพาะกับแอมโมเนียมเฮไลด์บางชนิดเท่านั้น เช่น FeCl 3 , MnCl 2 และอื่นๆ พวกเขาสามารถสร้างส่วนผสมด้วย AlCl 3 และปนเปื้อนอลูมิเนียมที่ได้
Alcan ได้พัฒนาเทคโนโลยีที่มีห้าขั้นตอน:
1. การผลิตโลหะผสมดิบ เช่น เหล็ก-ซิลิกอน-อะลูมิเนียม ในเตาหลอมลดอุณหภูมิคาร์บอเทอร์มอล
2. ปฏิกิริยาระหว่าง A1 และ AJC1 ในตัวแปลงที่อุณหภูมิ 1300 °C
3. การแยกไอระเหยเฮไลด์และซับฮาไลด์ในคอลัมน์กลั่น
4. ผลตอบแทน AICI สำหรับปฏิกิริยาระหว่างคลอไรด์และโลหะผสมเหลวที่อุดมด้วยอะลูมิเนียม
5. การสลายตัวของ A1C1 การผลิตอลูมิเนียมและการส่งคืน A1C1 3 เพื่อแก้ไข
วิธีการซับคลอไรด์เป็นที่สนใจมากที่สุดสำหรับการกลั่นอลูมิเนียมอัลลอยด์ทางอุตสาหกรรม
3.3. ที่กระบวนการ
รูปแบบการรับอลูมิเนียมโดยวิธี Thoth แสดงในรูปที่ 3.2. วัตถุดิบที่ประกอบด้วยอลูมิเนียมหลังจากการเตรียมที่เหมาะสมจะถูกคลอรีนในฟลูอิไดซ์เบดต่อหน้าโค้กและ SiCl 4 หลังใช้เพื่อระงับปฏิกิริยาคลอรีนของ SiO 2 เป็นผลมาจากคลอรีนในเตาหลอมฟลูอิไดซ์เบด (BF) ได้ส่วนผสมของก๊าซและไอ (VGM) ซึ่งรวมถึง AlCl 3 , FeCl 3 , TiCl 4 และ SiCl 4 ในคอนเดนเซอร์ตัวแรก ประมาณ 75% FeCl 3 ในสถานะของแข็งจะถูกปล่อยออกมาจาก PGM และส่งไปยังเครื่องปฏิกรณ์ตัวออกซิไดเซอร์ ซึ่งมันจะทำปฏิกิริยากับออกซิเจนในบรรยากาศ ส่งผลให้เกิด Fe 2 O 3 และ C1 2 . คลอรีนถูกส่งกลับเป็นคลอรีน ในคอนเดนเซอร์ตัวที่สอง FeCl 3 ที่เหลือจะถูกปล่อยออกมาและ A1C1 3 จะควบแน่น ไทเทเนียมและซิลิกอนคลอไรด์ควบแน่นในคอนเดนเซอร์ที่สาม การแยกคลอไรด์เหล่านี้ดำเนินการในคอลัมน์กลั่น
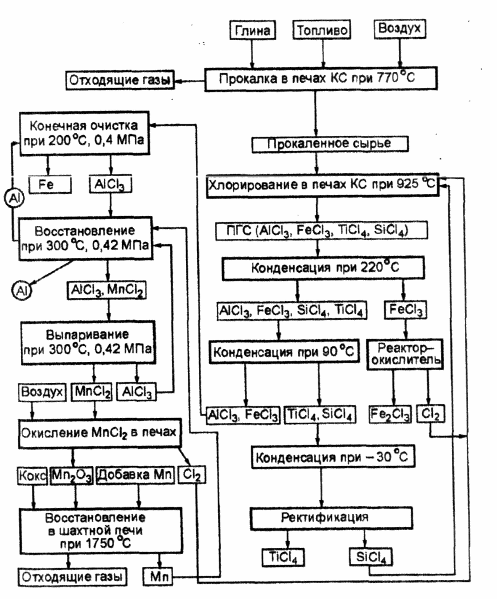
ข้าว. 3.2. โครงการรับอลูมิเนียมด้วยวิธี Thoth
คลอไรด์ของอะลูมิเนียมและเหล็กที่ถอดออกจากคอนเดนเซอร์ตัวที่สอง จะถูกให้ความร้อน สูบเข้าไปในตัวทำความสะอาดแบบสัมผัส โดยจะสัมผัสกันในกระแสทวนกับชั้นอนุภาคอะลูมิเนียมที่เป็นของแข็งที่เคลื่อนที่ได้ นี่คือที่ที่เกิดปฏิกิริยา:
อะลูมิเนียมคลอไรด์บริสุทธิ์ถูกป้อนเพื่อลดอุณหภูมิโลหะ สารรีดิวซ์ที่มีในทางเทคนิคซึ่งมีสัมพรรคภาพกับคลอรีนมากกว่าอะลูมิเนียมคือโซเดียม แมกนีเซียม และแมงกานีส อย่างไรก็ตาม สององค์ประกอบแรกของถนนและการผลิตนั้นใช้พลังงานมาก ดังนั้น ตามที่นักพัฒนาของกระบวนการ การใช้แมงกานีสมีข้อดีบางประการ ซึ่งสามารถงอกใหม่ได้จากคลอไรด์โดยวิธีคาร์บอเทอร์มิกโดยใช้พลังงานที่ต่ำกว่ามาก ในระหว่างการลดอะลูมิเนียมคลอไรด์ด้วยแมงกานีส ปฏิกิริยาต่อไปนี้จะเกิดขึ้น:
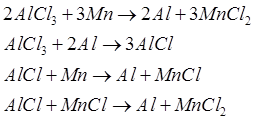
อลูมิเนียมจากส่วนผสมของ MnCl 2 กับ AlCl 3 ที่ไม่ทำปฏิกิริยาจะถูกแยกออกในตัวแยกแบบไซโคลน ในขณะที่แมงกานีสและอะลูมิเนียมคลอไรด์จะแยกจากกันในเครื่องระเหย อะลูมิเนียมคลอไรด์จะถูกส่งกลับไปยังเครื่องปฏิกรณ์เพื่อผลิตอะลูมิเนียม และแมงกานีสคลอไรด์จะทำปฏิกิริยากับออกซิเจนเพื่อสร้างออกไซด์ที่เป็นของแข็งของแมงกานีสและคลอรีน แมงกานีสออกไซด์ถูกลดขนาดให้เป็นโลหะโดยวิธีคาร์บอเทอร์มิกในเตาหลอมแบบเพลา ซึ่งบรรจุถ่านโค้กและหินปูน แมงกานีสถูกเติมลงในเตาเผาเพื่อชดเชยการสูญเสียระหว่างกระบวนการ
ต่อข้อเสีย กระบวนการนี้เช่นเดียวกับวิธีการทางความร้อนโลหะอื่นๆ รวมถึงการปนเปื้อนของผลิตภัณฑ์ที่เป็นผลลัพธ์ด้วยโลหะรีดิวซ์ ความจำเป็นในการจัดระบบการผลิตสำหรับการสร้างใหม่ของตัวรีดิวซ์ และการเพิ่มขึ้นของต้นทุนทุน
งานวิจัยเกี่ยวกับการผลิตอลูมิเนียมโดยการลดปริมาณแมงกานีสในห้องปฏิบัติการและขยายขนาดได้ดำเนินการในปี 2509-2516 ต่อมาไม่มีรายงานการพัฒนาอุตสาหกรรมในวรรณคดี ทิศทางนี้ซึ่งเห็นได้ชัดว่าเกิดจากปัญหาที่สำคัญในการดำเนินการทางเทคนิคของกระบวนการหลายขั้นตอนที่ซับซ้อนนี้
3.4. อิเล็กโทรไลซิสของคลอไรด์ละลาย
ในเดือนมกราคม พ.ศ. 2516 อัลโคได้ประกาศพัฒนาวิธีการผลิตอะลูมิเนียมแบบใหม่ บริษัทดำเนินการตามกระบวนการนี้เป็นเวลา 15 ปี และใช้เงินไป 23 ล้านดอลลาร์
วิธีนี้เกี่ยวข้องกับการผลิตอะลูมิเนียมคลอไรด์และอิเล็กโทรไลซิสที่ตามมา ในปี 1976 มีรายงานเกี่ยวกับการเปลี่ยนแปลงของบริษัท "Alcoa" ไปสู่การนำเทคโนโลยีคลอไรด์ไปใช้ในอุตสาหกรรมเพื่อผลิตอะลูมิเนียม ในเมืองปาเลสไตน์ (เท็กซัส สหรัฐอเมริกา) โรงงานที่มีกำลังการผลิตอลูมิเนียมออกแบบได้ 30,000 ตันต่อปีโดยใช้วิธีนี้ได้ดำเนินการอยู่
รูปแบบเทคโนโลยีพื้นฐานแสดงในรูปที่ 2.4.

ข้าว. 3.3. ระบบเทคโนโลยีได้อะลูมิเนียมจากคลอไรด์
อะลูมิเนียมคลอไรด์มีความสัมพันธ์กับน้ำสูงและมีแนวโน้มที่จะเกิดออกไซด์และไฮดรอกซีคลอไรด์ ในการนี้การรับมันใน รูปแบบบริสุทธิ์เป็นงานที่ยาก การปรากฏตัวของความชื้นทำให้เกิดการกัดกร่อน และการปรากฏตัวของสารประกอบที่ประกอบด้วยออกซิเจนนำไปสู่การตกตะกอนและการเกิดออกซิเดชันของแอโนด บริษัท "Alcoa" เสนอคลอรีนของอลูมินาบริสุทธิ์ซึ่งแก้ปัญหาเหล่านี้ได้บางส่วน อย่างไรก็ตาม จำเป็นต้องปฏิบัติตามข้อกำหนดที่เพิ่มขึ้นสำหรับความบริสุทธิ์ของคาร์บอนในระหว่างการทำคลอรีนในส่วนที่เกี่ยวข้องกับไฮโดรเจนหรือความชื้น
เมื่อเร็ว ๆ นี้มีรายงานว่า Toth Aluminium Corporation ประสบความสำเร็จในการผลิตอะลูมิเนียมคลอไรด์ที่มีส่วนประกอบหลักอย่างน้อย 99.97% ในระดับอุตสาหกรรมขนาดใหญ่
อะลูมิเนียมคลอไรด์ที่เป็นผลลัพธ์ในสถานะเป็นเม็ดหรือไอจะถูกป้อนเข้าสู่อิเล็กโทรลิซิส อิเล็กโทรไลเซอร์ที่ใช้ในเทคโนโลยีนี้ประกอบด้วยโครงเหล็กที่บุด้วยอิฐไฟร์เคลย์และอิฐดินเบาเพิ่มเติมในส่วนล่างเช่น วัสดุทนไฟที่ไม่เป็นสื่อนำความร้อนซึ่งทำปฏิกิริยากับคลอไรด์ละลายเล็กน้อย ที่ด้านล่างของอ่างมีช่องใส่กราไฟท์สำหรับเก็บอะลูมิเนียมเหลว ฝาปิดเซลล์อิเล็กโทรไลต์มีช่องสำหรับบรรจุอะลูมิเนียมคลอไรด์ การดูดอะลูมิเนียมเป็นระยะ และการจ่ายก๊าซคลอรีนที่ใช้ในการผลิตอะลูมิเนียมคลอไรด์อย่างต่อเนื่อง ผนังด้านข้างและฝาครอบอิเล็กโทรไลเซอร์ระบายความร้อนด้วยน้ำ
อิเล็กโทรไลซิสใช้อิเล็กโทรดที่ไม่สิ้นเปลืองกราไฟท์ ข้อได้เปรียบนี้ (เมื่อเทียบกับอิเล็กโทรไลซิสของไครโอไลต์-อลูมินาหลอมเหลว) ร่วมกับอุณหภูมิกระบวนการที่ค่อนข้างต่ำ (ประมาณ 700ºС) ทำให้สามารถผนึกอิเล็กโทรไลเซอร์ได้อย่างสมบูรณ์
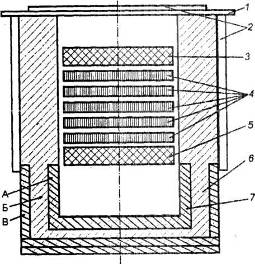
ข้าว. 2.5. แผนผังของเซลล์อิเล็กโทรไลต์ที่มีขั้วไฟฟ้าสองขั้วสำหรับการแยกอิเล็กโทรไลซิสของอะลูมิเนียมคลอไรด์
1 - ฝาครอบ: 2 - ระบายความร้อนด้วยน้ำ: 3 - แอโนด; 4 - อิเล็กโทรดสองขั้ว; 5 - แคโทด; 6 - ซับใน; 7 - ช่องสำหรับเก็บอลูมิเนียม วัสดุ: เอ - กราไฟท์; B - ไฟร์เคลย์; B - ไดอะตอม
การสลายตัวด้วยไฟฟ้าของอะลูมิเนียมคลอไรด์ในทางทฤษฎีต้องการแรงดันไฟฟ้าที่สูงกว่าอิเล็กโทรลิซิสของไครโอไลต์-อลูมินาที่หลอมเหลว เนื่องจากแรงดันการสลายตัวของอะลูมิเนียมคลอไรด์สูงกว่ามาก ดังนั้น ข้อเสียของกระบวนการอาจรวมถึงความจำเป็นในการจัดหาความร้อนจำนวนมากให้กับอิเล็กโทรไลเซอร์และการสูญเสียแรงดันไฟฟ้าที่สำคัญ อย่างไรก็ตาม การสูญเสียโอห์มมิกและความร้อนสูงจะลดลงอย่างมากเมื่อใช้ระบบอิเล็กโทรดสองขั้ว ในเซลล์ อิเล็กโทรดบนสุดคือแอโนด ด้านล่างคือแคโทด และระหว่างพวกมันคืออิเล็กโทรดกราไฟต์ ส่วนบนคือแคโทด และด้านล่างคือแอโนด ในเวลาเดียวกัน ผลการคำนวณแสดงให้เห็นว่าด้วยการเพิ่มจำนวนของอิเล็กโทรดสองขั้วและการลดลงของพื้นที่หน้าตัด กระแสไฟรั่วจะเพิ่มขึ้น กล่าวคือ ส่วนหนึ่งของกระแสไหลผ่านส่วนที่ชุบด้วยอิเล็กโทรไลต์ของเยื่อบุและช่องระหว่างเยื่อบุและไบโพลโดยไม่ต้องทำงานไฟฟ้าเคมี กระแสรั่วไหลเหล่านี้ส่งผลให้เอาต์พุตปัจจุบันลดลง
เนื่องจากอยู่ใกล้จุดหลอมเหลวและจุดเดือดที่ความดันบรรยากาศ อะลูมิเนียมคลอไรด์จึงระเหยได้จริงโดยไม่ละลาย อุณหภูมิการระเหิด 180.2 องศาเซลเซียส จุดสามจุดสอดคล้องกับอุณหภูมิ 192.6°C และความดันสัมบูรณ์ 0.23 MPa ในเรื่องนี้ ส่วนผสมที่หลอมเหลวของอะลูมิเนียมคลอไรด์ (5 ± 2% (มวล)) ลิเธียมคลอไรด์ (~28% (มวล)) และโซเดียมคลอไรด์ (67% (มวล)) ถูกใช้เป็นอิเล็กโทรไลต์ ในการหลอมเหลวเหล่านี้ กิจกรรมของ A1C1 3 จะลดลง สาเหตุส่วนใหญ่มาจากความจริงที่ว่าในส่วนผสมของคลอไรด์ที่หลอมละลาย A1C1 3 จะจับกับแอนไอออนเชิงซ้อน เป็นต้น
ระยะห่างระหว่างขั้วคือ 1.0 - 1.5 ซม. อุณหภูมิ 700 ±30ºСความหนาแน่นกระแสคือ -0.8 - 2.5 A / cm 2
บทสรุป
ข้อได้เปรียบหลักที่คาดการณ์และยืนยันระหว่างการดำเนินการทางอุตสาหกรรมในสหรัฐอเมริกาของวิธีการผลิตอะลูมิเนียมของ Alcoa โดยอิเล็กโทรไลซิสของคลอไรด์เมื่อเทียบกับอิเล็กโทรไลซิสของการหลอมของไครโอไลต์-อลูมินาคือความเป็นไปได้ของการใช้วัตถุดิบที่ประกอบด้วยอะลูมิเนียมคุณภาพต่ำ ช่วยลด การใช้พลังงานเฉพาะระหว่างอิเล็กโทรไลซิสประมาณ 30% และกำจัดการใช้วัสดุอิเล็กโทรดที่ประกอบด้วยคาร์บอนคุณภาพสูง การใช้คลอไรด์ที่หายากและก้าวร้าวแทนฟลูออไรด์ เพิ่มประสิทธิภาพแรงงาน ลดการลงทุน ลดค่าใช้จ่าย ต้นทุนของ ผลิตภัณฑ์ขั้นสุดท้ายและการปล่อยมลพิษสู่สิ่งแวดล้อม
เมื่อเร็ว ๆ นี้ ข้อดีของวิธีคลอไรด์ในการผลิตอะลูมิเนียมมีความชัดเจนมากขึ้นเนื่องจากการเพิ่มขึ้นของค่าไฟฟ้า วัตถุดิบสำหรับวิธีการผลิตอะลูมิเนียมทางอุตสาหกรรมที่มีอยู่ และข้อกำหนดในการป้องกันที่เพิ่มขึ้น สิ่งแวดล้อมและจนถึงขณะนี้ยังไม่มีผลลัพธ์เชิงบวกในการได้รับอลูมินาบริสุทธิ์จากวัตถุดิบที่ไม่ใช่อะลูมิเนียมคุณภาพต่ำ
ดังนั้นสิ่งที่มีแนวโน้มมากที่สุดของ ทางเลือกอื่นการผลิตอะลูมิเนียมคือการอิเล็กโทรไลซิสของอะลูมิเนียมคลอไรด์ในอิเล็กโทรไลเซอร์ที่มีอิเล็กโทรดสองขั้ว
บรรณานุกรม
1. Rozen B. M. , Rozen Ya. B. โลหะมีค่าพิเศษ - ม.: โลหะวิทยา, 2518. - 128 น.
2. Kolodin E. A. , Sverdlin V. A. , Svoboda R. V. การผลิตแอโนดที่ถูกเผาของอิเล็กโทรไลต์อลูมิเนียม - ม.: โลหะวิทยา, 1980, - 84 p.
3. Yankho E. A. , Vorobyov D. N. การผลิตมวลแอโนด - ม.: โลหะวิทยา, 2518. - 128 น.
4. M. M. Vetkzhov, A. M. Ts'shlakov และ S. N. Shkolnikov, Electrometallurgy ของอลูมิเนียมและแมกนีเซียม - ม.: โลหะวิทยา, 2530. - 320 น.
5. Shchenkov V.V. , Litvak S.N. การพัฒนาใหม่ กระบวนการทางเทคโนโลยีการผลิตอลูมิเนียม // Tsv. โลหะวิทยา: กระทิง NTI / ข้อมูลสี - พ.ศ. 2517 - ลำดับที่ 9 - ส. 38 - 41.
6. Sandler R. A. , Rapier A. Kh. Electrometallurgy ของอลูมิเนียมและแมกนีเซียม - L: LGI, 1983. - 94 น.
 อลูมิเนียมเป็นเรื่องธรรมดาที่สุด องค์ประกอบทางเคมีบนพื้น. อันดับที่สามรองจากออกซิเจนและซิลิกอน เนื้อหาของมันคือ 8.8 เปอร์เซ็นต์ของทรัพยากรธรรมชาติทั้งหมด
อลูมิเนียมเป็นเรื่องธรรมดาที่สุด องค์ประกอบทางเคมีบนพื้น. อันดับที่สามรองจากออกซิเจนและซิลิกอน เนื้อหาของมันคือ 8.8 เปอร์เซ็นต์ของทรัพยากรธรรมชาติทั้งหมด
อะลูมิเนียมบริสุทธิ์ได้มาอย่างไร?
แต่คุณรู้หรือไม่ว่าอะลูมิเนียมอิสระไม่พบในธรรมชาติ ไม่มีเหมืองอลูมิเนียม สกัดจากเหมืองที่มีบอกไซต์ อะลูไนต์ และเนฟิลีน เพื่อให้ได้อะลูมิเนียมในรูปแบบบริสุทธิ์ จำเป็นต้องแยกโลหะออกจากองค์ประกอบทางเคมีอื่นๆ
กระบวนการทางเทคโนโลยีในการรับอะลูมิเนียมประกอบด้วยสองขั้นตอน:
1 .แร่อะลูมิเนียมถูกบดขยี้ ได้อลูมินา
2 .การสกัดอะลูมิเนียมจากอลูมินา
อลูมินาเรียกว่าอลูมินาผลึก
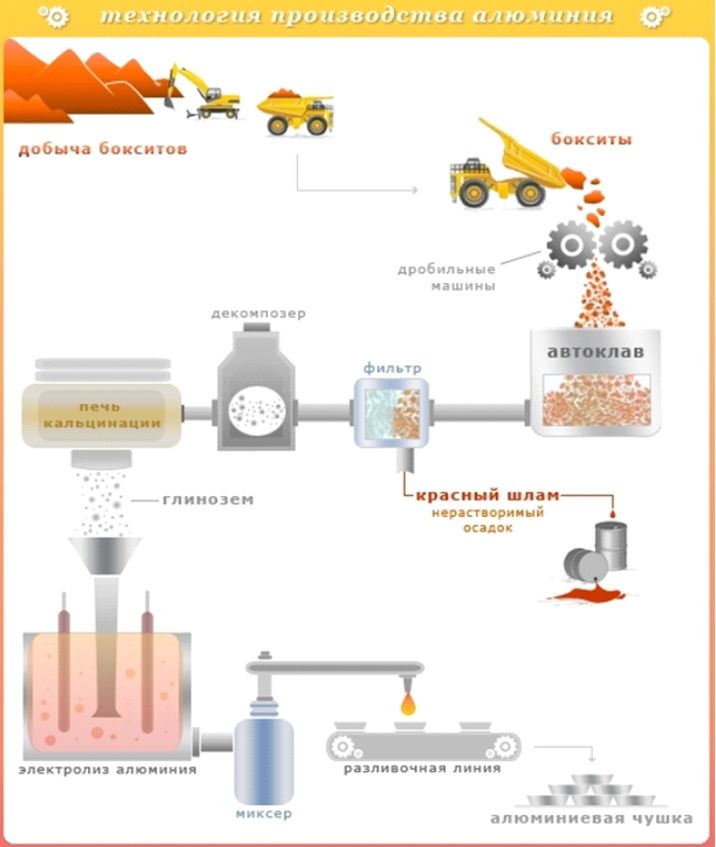
อลูมินาต้องผ่านกระบวนการอิเล็กโทรไลซิสในไครโอไลต์ ที่อุณหภูมิ 960-970 0 C แรงดันไฟฟ้าต่ำ 4.5 โวลต์ถูกเปิดใช้งานในอ่างพิเศษ แต่ที่มาก มีความแข็งแรงสูงปัจจุบัน 250,000 แอมแปร์ เป็นผลให้อลูมิเนียมเหลวเข้มข้นที่ด้านล่างของอ่างรอบ ๆ แคโทด ในขณะที่ออกซิเจนสะสมอยู่รอบขั้วบวก จากนั้นนำอะลูมิเนียมมากลั่นและเทลงในแม่พิมพ์ ต่อมาได้มีการผลิตผลิตภัณฑ์ต่างๆ
การผลิตอลูมิเนียมเป็นกระบวนการที่ใช้แรงงานมากซึ่งต้องใช้ไฟฟ้าร่วมกัน ดังนั้น ส่วนใหญ่มักจะพบโรงงานอลูมิเนียมใกล้กับโรงไฟฟ้าพลังน้ำขนาดใหญ่ เพื่อให้ได้ไฟฟ้าราคาถูก

อนาคตของอลูมิเนียมจะเป็นอย่างไร?
ในอดีตที่ผ่านมา:ตามคำสั่งของมีดนโปเลียนที่ 3 ทำจากอลูมิเนียม พวกเขาถูกเสิร์ฟในการเฉลิมฉลองให้กับจักรพรรดิและแขกผู้มีเกียรติที่สุด ที่เหลือก็พอใจกับเครื่องใช้ทองและเงิน
ในช่วงกลางศตวรรษที่สิบเก้า แฟชั่นนิสต้าชาวปารีสจำเป็นต้องมีอะลูมิเนียมอย่างน้อยหนึ่งชิ้นในชุดของพวกเขา
วันนี้:สิ่งที่ไม่ได้ทำจากอลูมิเนียม เครื่องบิน เชื้อเพลิงจรวด โปรไฟล์เรือนกระจก ผลิตภัณฑ์อิเล็กทรอนิกส์ การผลิตอะลูมิเนียมในโลหะวิทยาคิดเป็น 2% ของการผลิตโลหะ ในอนาคตตามการคาดการณ์จะเพิ่มขึ้นเป็น 4-5%
ต่อไปในอนาคต:ผู้ผลิตกำลังสร้างผ้าที่เคลือบด้วยชั้นบาง ๆ ของโลหะนี้แล้ว เรียกว่า "ผ้าอลูมิไนซ์" ตัวอย่างเช่น หากใช้ผ้าเป็นผ้าม่านในวันที่อากาศร้อน ผ้าจะทำงานได้ดีในสองวิธี: ความร้อนจะสะท้อนกลับมา และแสงจะเข้ามาในห้องได้ง่าย ดังนั้นอพาร์ทเมนท์จะเบาและเย็นในเวลาเดียวกัน
โลหะเบาสามารถพิชิตโลกได้เป็นเวลาสองศตวรรษและศตวรรษที่ 21 โดยทั้งหมด สัญญาว่าจะเป็นศตวรรษของอะลูมิเนียม
1. การนำอะลูมิเนียมออกไซด์กลับมาใช้ใหม่ด้วยไฮโดรเจน
2. อิเล็กโทรไลต์
3. โลหะความร้อน
4. Pyrometallurgical
5. Hydrometallurgical
181. วัสดุเริ่มต้นสำหรับการผลิตเหล็กสุกร ได้แก่
1. แร่เหล็ก
2. เศษเหล็ก ฟลักซ์
3. แร่เหล็ก ฟลักซ์ เชื้อเพลิง
4. แร่เหล็กโค้ก
5. อะลูมิเนียม
182. หลอมเหล็กหล่อใน:
1. เตาหลอม
3. เตาหลอมเพลา
4. เตาอุโมงค์
5. เตาห้อง
183. โลหะผสมของโลหะเหล็กคือ:
1. นิกเกิล
2. อิเล็กตรอน
5. เหล็กหล่อสีเทา
184. โลหะผสมเหล็กที่มีปริมาณคาร์บอน 0.2 ถึง 2% เรียกว่า:
5. ซีเมนต์
185. โลหะผสมเหล็กที่มีปริมาณคาร์บอนสูงกว่า 2% เรียกว่า:
5. นิกเกิล
186. อลูมิเนียมได้มาจากกระแสไฟฟ้า:
1. Boxtov
2. ส่วนผสมหลอมเหลวของอะลูมิเนียมออกไซด์กับไครโอไลต์
3. ศิษย์เก่า
4. อะลูมิเนียมไฮดรอกไซด์
5. เนฟีลีน
187. โลหะผสมของอลูมิเนียมกับซิลิกอนเรียกว่า:
1. ดูราลูมิน
3. Silumins
188. อลูมิเนียมอัลลอยด์ที่มีทองแดงแมกนีเซียมแมงกานีสเรียกว่า:
1. ดูราลูมิน
3. Silumins
189. โลหะผสมของเหล็กที่มีคาร์บอน (มากถึง 2%) ประกอบด้วย:
1. ออสเทนไนต์
2. ออสเทนไนต์และเลเดบิวไรท์
3. ซีเมนต์
4. ซีเมนต์และเลเดบิวไรท์
5. เลเดบุริตา
190. เหล็กหล่อที่มีปริมาณคาร์บอน (2-4%) ประกอบด้วย:
1. ออสเทนไนต์
2. ออสเทนไนต์และเลเดบิวไรท์
3. ซีเมนต์
4. ซีเมนต์และเลเดบิวไรท์
5. เลเดบุริตา
191. เหล็กหล่อที่มีปริมาณคาร์บอนมากกว่า 4% ประกอบด้วย:
1. ออสเทนไนต์
2. ออสเทนไนต์และเลเดบิวไรท์
3. ซีเมนต์
4. ซีเมนต์และเลเดบิวไรท์
5. เลเดบุริตา
192. นิกเกิลยึดติดกับเหล็ก:
193. แมงกานีสให้เหล็ก:
1. ความแข็งสีแดง ความแข็งแรง ทนต่อการกัดกร่อนที่อุณหภูมิสูง
2. ความแข็งแรง ความเหนียว ความต้านทานการกัดกร่อน
3. ความแข็งแกร่งภายใต้สภาวะปกติ
4. ความแข็งและความต้านทานการกัดกร่อน
5. ความแข็ง ทนต่อการสึกหรอ ทนต่อแรงกระแทก
194. ไนโอเบียมให้เหล็ก:
1. เพิ่มความเหนียวและความหนืด
2. ความทนทาน
3. ความแข็งและทนต่อการกัดกร่อน
4. ความต้านทานต่อกรด
5. ความแข็งแกร่งที่อุณหภูมิสูง
195. โมลิบดีนัมให้เหล็ก:
1. ความแข็งสีแดง ความแข็งแรง ทนต่อการกัดกร่อนที่อุณหภูมิสูง
2. ความแข็งแรง ความเหนียว ความต้านทานการกัดกร่อน
3. ความแข็งแกร่งภายใต้สภาวะปกติ
4. ความต้านทานต่อกรด
5. ความแข็ง ทนต่อการสึกหรอ ทนต่อแรงกระแทก
วัตถุดิบในการผลิตปิโตรเลียมโค้กคือ
2. ผลิตภัณฑ์น้ำมันหนัก
เป็นครั้งแรกที่นักเคมีชาวเยอรมัน F. Wöhler ได้รับอะลูมิเนียมที่เป็นโลหะในทางเคมีในปี 1821 (โดยการลดอะลูมิเนียมคลอไรด์ที่มีโพแทสเซียมของโลหะเมื่อถูกความร้อน) ในปี ค.ศ. 1854 นักวิทยาศาสตร์ชาวฝรั่งเศส Saint-Clair Deville ได้เสนอวิธีทางเคมีไฟฟ้าสำหรับการผลิตอะลูมิเนียมโดยการลดอะลูมิเนียม-โซเดียม ดับเบิ้ลคลอไรด์ด้วยโซเดียม
การผลิตและการผลิตอลูมิเนียม
อลูมิเนียมเมทัลลิกได้มาจากสามขั้นตอน:
- การรับอลูมินา (Al 2 O 3) จากแร่อะลูมิเนียม
- รับอลูมิเนียมจากอลูมินา
- การกลั่นอลูมิเนียม
รับอลูมินา
ประมาณ 95% ของอลูมินาทั้งหมดได้มาจากแร่บอกไซต์
อะลูมิเนียม(แร่อะลูมิเนียมฝรั่งเศส) (ตามชื่อพื้นที่ Baux ทางตอนใต้ของฝรั่งเศส) - แร่อะลูมิเนียมประกอบด้วยอะลูมิเนียมไฮดรอกไซด์ ออกไซด์ของเหล็กและซิลิกอน วัตถุดิบสำหรับการผลิตอลูมินาและวัสดุทนไฟที่มีส่วนผสมของอลูมินา เนื้อหาของอลูมินาในแร่บอกไซต์เชิงพาณิชย์มีตั้งแต่ 40% ถึง 60% และอีกมากมาย นอกจากนี้ยังใช้เป็นฟลักซ์ในโลหะผสมเหล็ก
ภาพที่ 1 - แร่อะลูมิเนียม
โดยทั่วไป บอกไซต์เป็นก้อนดิน คล้ายดินเหนียว ซึ่งอาจมีลักษณะเป็นแถบ พิโซไลต์ (คล้ายถั่ว) หรือเนื้อที่สม่ำเสมอ ภายใต้สภาพดินฟ้าอากาศปกติ เฟลด์สปาร์ (แร่ธาตุที่ประกอบขึ้นเป็นส่วนใหญ่ของเปลือกโลกและเป็นอะลูมิโนซิลิเกต) จะสลายตัวเป็นดินเหนียว แต่ในสภาพอากาศร้อนและมีความชื้นสูง บอกไซต์อาจเป็นผลิตภัณฑ์สุดท้ายจากการสลายตัว เนื่องจากสภาพแวดล้อมดังกล่าวสนับสนุนการกำจัด ของด่างและซิลิกา โดยเฉพาะจากไซไนต์หรือแกบโบร อะลูมิเนียมจะถูกแปรรูปเป็นอะลูมิเนียมเป็นขั้นๆ ขั้นแรก ได้อะลูมิเนียมออกไซด์ (อลูมินา) และจากนั้นก็อะลูมิเนียมที่เป็นโลหะ
สิ่งเจือปนหลักในแร่บอกไซต์คือ Fe 2 O 3 , SiO 2 , TiO 2 สิ่งเจือปนเล็กน้อยของแร่บอกไซต์ ได้แก่ Na 2 O, K 2 O, CaO, MgO, ธาตุหายาก, Cr, P, V, F, สารอินทรีย์
โดยปกติแล้วแร่อะลูมิเนียมจะถูกจัดประเภท:
- ตามสี
- โดยแร่หลัก (มักผสมกัน);
- ตามวัย
เกณฑ์หลัก คุณสมบัติของแร่อะลูมิเนียมคือ:
- โมดูลซิลิคอน (Msi = Al 2 O 3 /SiO 2 (% wt.)) โมดูลซิลิกอนที่ใหญ่ขึ้นคุณภาพก็จะยิ่งดีขึ้น (Msi = 7);
- ปริมาณธาตุเหล็กในแง่ของ Fe 2 O 3 หากเนื้อหาของ Fe 2 O 3 อยู่ที่ประมาณ 18 % โดยน้ำหนัก อะลูมิเนียมก็ถือเป็นธาตุเหล็กสูง ยิ่งมีธาตุเหล็กมากเท่าไร การขุดแร่บอกไซต์ก็ยิ่งยากขึ้นเท่านั้น
- ปริมาณกำมะถัน การปรากฏตัวของกำมะถันจำนวนมากทำให้การประมวลผลของบอกไซต์ซับซ้อน
- เนื้อหาของคาร์บอเนตในแง่ของ CO 3 (2-) . การปรากฏตัวของคาร์บอเนตจำนวนมากทำให้การประมวลผลของบอกไซต์ซับซ้อน
ใช้อะลูมิเนียม:
- ในการผลิตอลูมินา
- ในการผลิตวัสดุที่มีฤทธิ์กัดกร่อน
- ในการผลิตวัสดุทนไฟ
- เป็นฟลักซ์สำหรับการถลุงเหล็กแบบเปิด
- สำหรับการอบแห้งก๊าซและน้ำมันทำความสะอาดจากกำมะถัน
- เป็นสีย้อม
จนถึงปัจจุบันซัพพลายเออร์หลักของอะลูมิเนียมคือ:
- ออสเตรเลีย - มีเงินฝากจำนวนมากเช่น Fe, Au, U, Ni, Co, Cu และอื่นๆ การซื้อวัตถุดิบจากออสเตรเลียมีกำไรมากกว่าการซื้อวัตถุดิบเอง
- กินี - รัสเซียซื้อที่นั่งหลายที่นั่ง
- อเมริกากลาง: กายอานา จาเมกา ซูริมาน
- บราซิล.
ในยุโรป เงินฝากทั้งหมดจะหมดลง บอกไซต์มาจากกรีซ แต่วัตถุดิบนี้มีคุณภาพต่ำ

รูปที่ 2 - ปริมาณสำรองของอะลูมิเนียมในโลก
ด้านล่างเป็นแหล่งแร่อะลูมิเนียมหลักในรัสเซีย
- เงินฝากครั้งแรกถูกค้นพบในปี 1914 ใกล้เซนต์ปีเตอร์สเบิร์ก ใกล้เมือง Tikhvin 6 โรงงานถูกสร้างขึ้นที่สนามนี้ ที่ใหญ่ที่สุดคือโรงงานอลูมิเนียม Volkhov จนถึงปัจจุบัน เขตข้อมูล Tikhvinskoye หมดลงแล้วและดำเนินการกับวัตถุดิบที่นำเข้าเป็นหลัก
- ในปี 1931 มีการค้นพบแหล่งแร่บอกไซต์คุณภาพสูง (SUBR) ของ Severo-Uralskoye เป็นพื้นฐานสำหรับการก่อสร้างโรงงานอะลูมิเนียม Ural (UAZ) ในปี 1939 และบนพื้นฐานของเหมืองบอกไซต์เซาท์อูราล (YUBR) โรงถลุงอะลูมิเนียม Bogoslovsky (BAZ) ก็ถูกสร้างขึ้น
- สนาม Severoonezhskoye ตั้งอยู่บนถนนสู่คาบสมุทร Kola อยู่ในแผน แต่ไม่ทราบวันที่สร้าง
- เงินฝาก Vislovskoe เป็นดินเหนียวบริสุทธิ์ประเภท kaolite ไม่ใช้สำหรับอลูมินา
- เขต Timanskoye (สาธารณรัฐ Komi, Varkuta) ชาวแคนาดามีความสนใจในสาขานี้ ดังนั้นพวกเขากำลังวางแผนที่จะสร้างโรงงาน (Komi Sual เป็นบริษัทโฮลดิ้ง)
การรับอลูมินาจากแร่บอกไซต์
เนื่องจากอะลูมิเนียมมีลักษณะเป็นแอมโฟเทอริก จึงผลิตอลูมินาได้สามวิธี:
- อัลคาไลน์,
- กรด;
- อิเล็กโทรไลต์
วิธีที่นิยมใช้กันมากที่สุดคือวิธีอัลคาไลน์ (วิธีของ K.I. ไบเออร์ ซึ่งพัฒนาขึ้นในรัสเซียเมื่อปลายศตวรรษก่อนที่ผ่านมา และใช้สำหรับการประมวลผลบอกไซต์คุณภาพสูงที่มีซิลิกาในปริมาณเล็กน้อย (มากถึง 5-6%)) ตั้งแต่นั้นมา ประสิทธิภาพทางเทคนิคก็ได้รับการปรับปรุงอย่างมาก รูปแบบการผลิตอลูมินาโดยวิธีไบเออร์แสดงในรูปที่ 3

รูปที่ 3 - โครงการรับอลูมินาโดยวิธีไบเออร์
สาระสำคัญของวิธีการนี้คือ สารละลายอะลูมิเนียมจะสลายตัวอย่างรวดเร็วเมื่อใส่อะลูมิเนียมไฮดรอกไซด์เข้าไป และสารละลายที่เหลือจากการสลายตัวหลังจากการระเหยของสารละลายภายใต้สภาวะของการผสมแบบเข้มข้นที่ 169–170 °C สามารถละลายอลูมินาที่มีอยู่ในอะลูมิเนียมได้อีกครั้ง วิธีนี้ประกอบด้วยการดำเนินการหลักดังต่อไปนี้:
1. การเตรียมอะลูมิเนียมซึ่งประกอบด้วยการบดและบดในโรงสี โรงสีจะมาพร้อมกับบอกไซต์ ด่างกัดกร่อน และมะนาวจำนวนเล็กน้อย ซึ่งช่วยเพิ่มการปลดปล่อย Al 2 O 3 ; เยื่อกระดาษที่ได้จะถูกป้อนเพื่อชะล้าง
2. การชะชะอะลูมิเนียม (เมื่อเร็ว ๆ นี้บล็อกหม้อนึ่งความดันรูปทรงกลมที่ใช้จนถึงขณะนี้ได้ถูกแทนที่บางส่วนด้วยหม้อนึ่งความดันแบบท่อซึ่งการชะจะเกิดขึ้นที่อุณหภูมิ 230–250 ° C (500–520 K) ซึ่งประกอบด้วยการสลายตัวทางเคมีจาก ปฏิสัมพันธ์กับสารละลายด่าง อะลูมิเนียมออกไซด์ไฮเดรตเมื่อทำปฏิกิริยากับด่างให้เข้าสู่สารละลายในรูปของโซเดียมอะลูมิเนต:
AlOOH+NaOH→NaAlO 2 +H 2 O
อัล(OH) 3 +NaOH→NaAlO 2 +2H 2 O;
SiO 2 +2NaOH→Na 2 SiO 3 +H2O;
ในสารละลายโซเดียมอะลูมิเนตและโซเดียมซิลิเกตเป็นโซเดียมอะลูมิโนซิลิเกตที่ไม่ละลายน้ำ ไททาเนียมและเหล็กออกไซด์ผ่านเข้าไปในสารตกค้างที่ไม่ละลายน้ำทำให้สารตกค้างเป็นสีแดง สารตกค้างนี้เรียกว่าโคลนแดง เมื่อละลายเสร็จแล้ว โซเดียมอะลูมิเนตที่ได้จะถูกเจือจางด้วยสารละลายด่างในขณะที่ลดอุณหภูมิลง 100 ° C
3. การแยกสารละลายอะลูมิเนตออกจากโคลนแดง มักล้างด้วยสารเพิ่มความข้นพิเศษ ด้วยเหตุนี้ โคลนสีแดงจึงตกลงมา และสารละลายอะลูมิเนตจะถูกระบายออกแล้วกรองออก (ชี้แจง) ในปริมาณที่จำกัด กากตะกอนจะถูกใช้ ตัวอย่างเช่น เป็นสารเติมแต่งสำหรับซีเมนต์ ขึ้นอยู่กับเกรดของแร่บอกไซต์ โคลนสีแดง 0.6 - 1.0 ตัน (สารตกค้างแห้ง) ตกลงบนอลูมินาที่ผลิตได้ 1 ตัน ขึ้นอยู่กับเกรดของอะลูมิเนียม
4. การสลายตัวของสารละลายอะลูมิเนต มันถูกกรองและสูบลงในภาชนะขนาดใหญ่ที่มีตัวกวน (ตัวย่อยสลาย) อะลูมิเนียมไฮดรอกไซด์ Al(OH) 3 ถูกสกัดจากสารละลายอิ่มตัวยิ่งยวดเมื่อเย็นลงจนถึง 60 °C (330 K) และกวนอย่างต่อเนื่อง เนื่องจากกระบวนการนี้ดำเนินไปอย่างช้าๆและไม่สม่ำเสมอ และการก่อตัวและการเติบโตของผลึกอะลูมิเนียมไฮดรอกไซด์มีความสำคัญอย่างยิ่งในการประมวลผลต่อไป จึงมีการเพิ่มไฮดรอกไซด์ที่เป็นของแข็งจำนวนมากลงในตัวย่อยสลาย - เมล็ดพืช:
นา 2 O อัล 2 O 3 + 4H2O→Al(OH) 3 + 2NaOH;
5. การจัดสรรอะลูมิเนียมไฮดรอกไซด์และการจำแนกประเภท สิ่งนี้เกิดขึ้นในไฮโดรไซโคลนและตัวกรองสุญญากาศ ซึ่งตะกอนที่มีอนุภาค Al(OH) 3 50 - 60% แยกออกจากสารละลายอะลูมิเนต ส่วนสำคัญของไฮดรอกไซด์จะกลับสู่กระบวนการย่อยสลายเป็นวัสดุเมล็ด ซึ่งยังคงหมุนเวียนอยู่ในปริมาณที่ไม่เปลี่ยนแปลง สารตกค้างหลังจากล้างด้วยน้ำจะถูกเผา กรองก็กลับสู่การไหลเวียน (หลังจากความเข้มข้นในเครื่องระเหย - เพื่อชะล้างบอกไซต์ใหม่);
6. การคายน้ำของอะลูมิเนียมไฮดรอกไซด์ (การเผา); เป็นขั้นตอนสุดท้ายของการผลิตอลูมินา มันดำเนินการในเตาเผาแบบหมุนแบบท่อและเมื่อเร็ว ๆ นี้ในเตาเผาที่มีการเคลื่อนที่แบบปั่นป่วนของวัสดุที่อุณหภูมิ 1150 - 1300 ° C; อะลูมิเนียมไฮดรอกไซด์ดิบ ผ่านเตาโรตารี่ ทำให้แห้งและแห้ง เมื่อถูกความร้อน การเปลี่ยนแปลงโครงสร้างต่อไปนี้จะเกิดขึ้นตามลำดับ:
Al(OH) 3 → AlOOH → γ-Al 2 O 3 → α-Al 2 O 3
200 °C - 950 °C - 1200 °C.
อลูมินาที่ผ่านการเผาขั้นสุดท้ายมี 30 - 50% α-Al2O3 (คอรันดัม) ส่วนที่เหลือคือ γ-Al 2 O 2 .
วิธีนี้สกัดได้ 85 - 87% ของอลูมินาทั้งหมดที่ผลิต อลูมินาที่ได้นั้นเป็นสารประกอบทางเคมีที่มีจุดหลอมเหลวที่ 2050 ° C
การได้มาซึ่งอะลูมิเนียมด้วยกระแสไฟฟ้า
การลดอิเล็กโทรไลต์ของอะลูมิเนียมออกไซด์ที่ละลายในตัวหลอมแบบไครโอไลต์จะดำเนินการที่อุณหภูมิ 950–970 °C ในเซลล์อิเล็กโทรไลต์ เซลล์ประกอบด้วยอ่างที่ปูด้วยบล็อกคาร์บอนซึ่งอยู่ด้านล่างซึ่งมีการจ่ายกระแสไฟฟ้า อะลูมิเนียมเหลวที่ปล่อยออกมาด้านล่างทำหน้าที่เป็นแคโทดที่หนักกว่าเกลืออิเล็กโทรไลต์ที่หลอมละลาย ดังนั้นจึงถูกรวบรวมไว้บนฐานถ่านหิน จากนั้นจึงสูบออกเป็นระยะ (รูปที่ 4) จากด้านบน คาร์บอนแอโนดจะแช่อยู่ในอิเล็กโทรไลต์ ซึ่งเผาไหม้ในบรรยากาศของออกซิเจนที่ปล่อยออกมาจากอะลูมิเนียมออกไซด์ ปล่อยคาร์บอนมอนอกไซด์ (CO) หรือคาร์บอนไดออกไซด์ (CO 2) ในทางปฏิบัติใช้แอโนดสองประเภท:
- แอโนด Zederberg ที่อบด้วยตัวเองซึ่งประกอบด้วยก้อนที่เรียกว่า "ขนมปัง" ของมวล Zederberg (ถ่านหินเถ้าต่ำที่มีน้ำมันดิน 25 - 35%) ยัดลงในเปลือกอลูมิเนียม ภายใต้การกระทำของอุณหภูมิสูงมวลขั้วบวกจะถูกเผา (เผา);
- ยิงหรือ "ต่อเนื่อง" แอโนดที่ทำจากบล็อกคาร์บอนขนาดใหญ่ (เช่น 1900 × 600 × 500 มม. น้ำหนักประมาณ 1.1 ตัน)

รูปที่ 4 - แผนผังของอิเล็กโทรไลเซอร์
ความแรงของกระแสไฟฟ้าบนอิเล็กโทรไลต์คือ 150,000 A. พวกมันเชื่อมต่อกับเครือข่ายแบบอนุกรมนั่นคือระบบ (อนุกรม) ได้มา - อิเล็กโทรไลเซอร์แถวยาว
แรงดันใช้งานบนอ่างซึ่งอยู่ที่ 4 - 5 V นั้นสูงกว่าแรงดันที่อะลูมิเนียมออกไซด์สลายตัวมาก เนื่องจากการสูญเสียแรงดันไฟฟ้าในส่วนต่างๆ ของระบบเป็นสิ่งที่หลีกเลี่ยงไม่ได้ระหว่างการทำงาน ความสมดุลของวัตถุดิบและพลังงานเมื่อได้รับอะลูมิเนียม 1 ตัน แสดงในภาพที่ 5

ภาพที่ 5 - ความสมดุลของวัตถุดิบและพลังงานในการผลิตอลูมิเนียม 1 ตัน
ในถังปฏิกิริยา อะลูมิเนียมออกไซด์จะถูกแปลงเป็นอะลูมิเนียมคลอไรด์ก่อน จากนั้นในอ่างที่หุ้มฉนวนอย่างแน่นหนา อิเล็กโทรไลซิสของ AlCl 3 จะถูกละลายในเกลือหลอมเหลวของ KCl หรือ NaCl คลอรีนที่ปล่อยออกมาในกระบวนการนี้จะถูกดูดออกและป้อนเพื่อรีไซเคิล อลูมิเนียมวางอยู่บนแคโทด
ข้อดีของวิธีนี้เหนืออิเล็กโทรไลซิสที่มีอยู่ของของเหลว cryolite-alumina ละลาย (Al 2 O 3 , Na 3 AlF 6 ที่ละลายใน cryolite) คือ: ประหยัดพลังงานได้มากถึง 30%; ความเป็นไปได้ของการใช้อะลูมิเนียมออกไซด์ซึ่งไม่เหมาะสำหรับอิเล็กโทรไลซิสแบบเดิม (เช่น Al 2 O 3 ที่มีปริมาณซิลิกอนสูง) แทนที่ไครโอไลต์ราคาแพงด้วยเกลือที่ถูกกว่า การกำจัดอันตรายจากการปล่อยฟลูออไรด์
รับอลูมิเนียมขัดเงา
สำหรับอะลูมิเนียม การกลั่นด้วยไฟฟ้าด้วยการสลายตัวของสารละลายเกลือในน้ำเป็นไปไม่ได้ เนื่องจากเพื่อวัตถุประสงค์บางอย่าง ระดับการทำให้อะลูมิเนียมอุตสาหกรรมบริสุทธิ์ (Al 99.5 - Al 99.8) ที่ได้จากอิเล็กโทรไลซิสของการหลอมของไครโอไลต์-อลูมินายังไม่เพียงพอ แม้แต่อะลูมิเนียมบริสุทธิ์ (Al 99.99 R) ก็ได้มาจากอะลูมิเนียมอุตสาหกรรมหรือเศษโลหะโดยการกลั่น . วิธีการกลั่นที่มีชื่อเสียงที่สุดคืออิเล็กโทรไลซิสสามชั้น
การกลั่นด้วยอิเล็กโทรไลซิสสามชั้น
ซับในด้วยแผ่นเหล็กที่ทำงานด้วยกระแสตรง (รูปที่ 6) อ่างกลั่นประกอบด้วยเตาถ่านที่มีตัวนำกระแสไฟและซับในแมกนีไซต์ที่ป้องกันความร้อน ตรงกันข้ามกับอิเล็กโทรไลซิสของไครโอไลต์-อลูมินาที่หลอมเหลว แอโนดที่นี่คือ ตามกฎแล้ว โลหะกลั่นที่หลอมเหลว (ชั้นแอโนดที่ต่ำกว่า) อิเล็กโทรไลต์ประกอบด้วยฟลูออไรด์บริสุทธิ์หรือส่วนผสมของแบเรียมคลอไรด์และอะลูมิเนียมและโซเดียมฟลูออไรด์ (ชั้นกลาง) อะลูมิเนียมที่ละลายจากชั้นแอโนดในอิเล็กโทรไลต์จะถูกปล่อยออกมาเหนืออิเล็กโทรไลต์ (ชั้นแคโทดด้านบน) โลหะบริสุทธิ์ทำหน้าที่เป็นแคโทด กระแสไฟฟ้าถูกส่งไปยังชั้นแคโทดโดยอิเล็กโทรดกราไฟท์

รูปที่ 6 - ไดอะแกรมของเซลล์อิเล็กโทรไลต์พร้อมเตาด้านหน้าสำหรับการกลั่นอลูมิเนียม (ตาม Fulda - Ginzberg)
1 - อลูมิเนียมละลาย; 2 – อิเล็กโทรไลต์; 3 - อลูมิเนียมกลั่นความถี่สูง 4 – แคโทดกราไฟท์; 5 - ผนังแมกนีไซต์; 6 - แตรหน้า; 7 - ชั้นฉนวน; 8 - ฉนวนด้านข้าง; 9 - เตาถ่าน; 10 – ตัวนำแอโนด; 11 - การแยกเตาไฟ; 12 - กล่องเหล็ก; 13 - ปก
อ่างทำงานที่อุณหภูมิ 750 - 800 ° C ใช้พลังงาน 20 kWh ต่ออะลูมิเนียมบริสุทธิ์ 1 กิโลกรัม ซึ่งสูงกว่าการใช้ไฟฟ้าอิเล็กโทรไลซิสแบบอะลูมิเนียมทั่วไปเล็กน้อย
โลหะแอโนดประกอบด้วย 25-35% Cu; 7 – 12% สังกะสี; 6 – 9% ศรี; มากถึง 5% Fe และแมงกานีส นิกเกิล ตะกั่ว และดีบุกจำนวนเล็กน้อย ส่วนที่เหลือ (40 - 55%) เป็นอะลูมิเนียม โลหะหนักและซิลิกอนทั้งหมดยังคงอยู่ในชั้นแอโนดระหว่างการกลั่น การปรากฏตัวของแมกนีเซียมในอิเล็กโทรไลต์นำไปสู่การเปลี่ยนแปลงที่ไม่พึงประสงค์ในองค์ประกอบของอิเล็กโทรไลต์หรือทำให้เกิดตะกรันที่รุนแรง ในการกำจัดแมกนีเซียม ตะกรันที่มีแมกนีเซียมจะได้รับการบำบัดด้วยฟลักซ์หรือคลอรีนที่เป็นก๊าซ
ผลจากการกลั่นจะได้อะลูมิเนียมบริสุทธิ์ (99.99%) และผลิตภัณฑ์คัดแยก (ผลิตภัณฑ์ Ziger) ซึ่งประกอบด้วยโลหะหนักและซิลิกอน และถูกแยกออกในรูปของสารละลายอัลคาไลน์และกากผลึก สารละลายอัลคาไลน์เป็นของเสีย และกากที่เป็นของแข็งจะถูกใช้เพื่อขจัดความเป็นกรด
อลูมิเนียมกลั่นมักมีองค์ประกอบดังนี้ %: Fe 0.0005 - 0.002; ศรี 0.002 - 0.005; ลูกบาศ์ก 0.0005 - 0.002; สังกะสี 0.0005 - 0.002; ร่องรอยมิลลิกรัม; อัลพักผ่อน
อลูมิเนียมกลั่นถูกแปรรูปเป็นผลิตภัณฑ์กึ่งสำเร็จรูปในองค์ประกอบที่ระบุหรือผสมกับแมกนีเซียม (ตารางที่ 1)
ตารางที่ 1 - องค์ประกอบทางเคมีของอะลูมิเนียมบริสุทธิ์สูงและอะลูมิเนียมขั้นต้นตาม DIN 1712 แผ่น 1
|
สิ่งเจือปนที่อนุญาต*, % |
||||||||
|
รวมทั้ง |
||||||||
* เท่าที่เป็นไปได้ที่จะกำหนดโดยวิธีการวิจัยทั่วไป
** อะลูมิเนียมบริสุทธิ์สำหรับงานวิศวกรรมไฟฟ้า (ตัวนำอะลูมิเนียม) มีจำหน่ายในรูปของอะลูมิเนียมปฐมภูมิ 99.5 ที่มีปริมาณไม่เกิน 0.03% (Ti + Cr + V + Mn) กำหนดในกรณีนี้เป็น E-A1 หมายเลขวัสดุ 3.0256 มิฉะนั้นจะเป็นไปตาม VDE-0202
การกลั่นด้วยสารประกอบเชิงซ้อนออร์กาโนอะลูมิเนียมและการหลอมโซน
อะลูมิเนียมที่มีความบริสุทธิ์สูงเกรด A1 99.99 R ได้จากการกลั่นอิเล็กโทรลิซิสของอะลูมิเนียมบริสุทธิ์หรืออะลูมิเนียมบริสุทธิ์เชิงพาณิชย์โดยใช้สารประกอบออร์กาโนอะลูมิเนียมที่ซับซ้อนของอะลูมิเนียมเป็นอิเล็กโทรไลต์ อิเล็กโทรลิซิสเกิดขึ้นที่อุณหภูมิประมาณ 1,000 องศาเซลเซียสระหว่างอิเล็กโทรดอะลูมิเนียมที่เป็นของแข็ง และหลักการคล้ายกับอิเล็กโทรไลซิสสำหรับการกลั่นของทองแดง ลักษณะของอิเล็กโทรไลต์กำหนดความจำเป็นในการทำงานโดยไม่มีอากาศและที่ความหนาแน่นกระแสไฟต่ำ
อิเล็กโทรไลซิสสำหรับการกลั่นชนิดนี้ ซึ่งใช้ในตอนแรกเฉพาะในห้องปฏิบัติการเท่านั้น ได้ดำเนินการในระดับอุตสาหกรรมขนาดเล็กแล้ว - ผลิตโลหะหลายตันต่อปี ระดับการทำให้บริสุทธิ์ของโลหะที่ได้คือ 99.999 -99.9999% ขอบเขตที่เป็นไปได้ในการใช้งานสำหรับโลหะที่มีความบริสุทธิ์นี้ ได้แก่ วิศวกรรมไฟฟ้าและอิเล็กทรอนิกส์ด้วยการแช่แข็ง
สามารถใช้วิธีการกลั่นที่พิจารณาแล้วในการชุบด้วยไฟฟ้า
ความบริสุทธิ์ที่สูงกว่า - ในนามสูงถึง A1 99.99999 - สามารถรับได้จากการหลอมโลหะในโซนที่ตามมา เมื่อแปรรูปอะลูมิเนียมที่มีความบริสุทธิ์สูงให้เป็นผลิตภัณฑ์กึ่งสำเร็จรูป แผ่นหรือลวด จำเป็นต้องใช้ความระมัดระวังเป็นพิเศษเนื่องจากอุณหภูมิการตกผลึกใหม่ของโลหะ คุณสมบัติที่โดดเด่นของโลหะกลั่นคือการนำไฟฟ้าสูงในบริเวณที่มีอุณหภูมิในการแช่แข็ง


