Wstęp
Aluminium jest najważniejszym metalem, wielkość jego produkcji znacznie przewyższa produkcję wszystkich innych metali nieżelaznych i ustępuje jedynie produkcji stali. Wysokie tempo wzrostu produkcji aluminium wynika z jego unikalnych właściwości fizykochemicznych, dzięki którym znalazło szerokie zastosowanie w elektrotechnice, lotnictwie i motoryzacji, transporcie, AGD, budownictwie i opakowaniach. produkty żywieniowe itp.
Ale aluminium nie występuje naturalnie w postaci pierwiastkowej. Znane sposoby otrzymujący metalowe aluminium były drogie i nieefektywne, dlatego od dawna uważany jest za metal rzadki. W tym procesie przemysłowym głównym surowcem jest ruda utworzona głównie z uwodnionego tlenku glinu i niektórych zanieczyszczeń. Do wyprodukowania dwóch ton tlenku glinu potrzeba od czterech do pięciu ton boksytu.
Ta wartość zwykle generuje jedną tonę aluminium jako produktu. Aby rozwiązać ten problem, tlenek glinu miesza się ze strumieniem, to znaczy z substancją, która ma na celu obniżenie temperatury topnienia innych substancji. Po stopieniu w cieczy jony tlenku glinu są wolne.
Przemysł aluminiowy Rosji, stworzony w czas sowiecki, zajmuje dominującą pozycję w produkcji metali nieżelaznych w kraju i zajmuje drugie miejsce na świecie pod względem produkcji metali. W ostatnie lata, z racji znane przyczyny, sprzęt do produkcji aluminium praktycznie nie jest modernizowany, technologia elektrolizy nie jest ulepszana, ilość badań naukowych jest niedopuszczalnie zmniejszona i wyraźnie pozostaje w tyle za krajami rozwiniętymi. Jednocześnie za granicą sprzęt jest intensywnie modernizowany, doskonalona jest technologia, co pozwoliło na gwałtowny wzrost wydajność ekonomiczna i bezpieczeństwa ekologicznego produkcji aluminium.
Następnie w stalowym naczyniu przeprowadza się elektrolizę magmową tej mieszaniny tlenku glinu ze stopionym kriolitem. Dodatnim biegunem tej elektrolizy są elektrody grafitowe zanurzone w cieczy. Utleniają tlen. Dlatego mamy globalne równanie dla tego procesu.
Należy pamiętać, że powstałe metaliczne aluminium jest w stanie ciekłym. Dlatego pozostaje w stanie płynnym. Ponieważ aluminium jest gęstsze niż mieszanina, pozostaje na dnie naczynia i okresowo wycieka. Następnie umieszcza się go w formach zgodnie z pożądanym przeznaczeniem.
W ostatnie czasy Inżynieria mechaniczna coraz częściej wymaga metali lekkich, zwłaszcza w przemyśle lotniczym i transporcie kolejowym. Dlatego duże znaczenie ma rozwój nowych i bardziej ekonomicznych metod pozyskiwania aluminium oraz doskonalenie istniejących metod.
1. Historia rozwoju przemysłu aluminiowego
Obecnie aluminium zajmuje pierwsze miejsce wśród metali nieżelaznych pod względem wielkości produkcji, a jego produkcja stale się rozwija.
Przemysł aluminiowy jest jednym z najbardziej konkurencyjnych sektorów w kraju, stanowiąc prawie 10% bilansu handlowego Brazylii. Tylko pięć firm konkuruje o rynek krajowy, a około 90% brazylijskiego eksportu pochodzi z metali pierwotnych. Ekspansja tej branży na rynku międzynarodowym nastąpiła w obliczu niedoborów energii w krajach uprzemysłowionych, co zbiega się z okresem gwałtownego kurczenia się brazylijskiej gospodarki. Po przeanalizowaniu determinant krajowej przewagi komparatywnej wyjaśniono przyczyny wysokiego stopnia konkurencyjności międzynarodowej osiąganej przez ten sektor przemysłu.
Historycznie pierwsze wzmianki o metalicznym aluminium miały miejsce w pismach rzymskich z pierwszego wieku. W słynna encyklopedia„Historia naturalis” można znaleźć w następującej historii. Pewnego dnia rzymski jubiler mógł pokazać cesarzowi Tyberiuszowi talerz obiadowy wykonany z nowego metalu. Talerz był bardzo lekki i lśnił jak srebro. Jubiler powiedział cesarzowi, że wydobył metal ze zwykłej gliny. Zapewnił też cesarza, że tylko on i bogowie wiedzą, jak wydobyć metal z gliny. Cesarz był bardzo zainteresowany. Jednak natychmiast zdał sobie sprawę, że cały jego skarbiec, składający się ze złota i srebra, popadnie w ruinę, jeśli ludzie zaczną wytwarzać ten lekki metal z gliny. Dlatego zamiast nagrody oczekiwanej przez jubilera został ścięty.
Określa również kilka ważnych czynników, które mogą zagrozić konkurencyjności Brazylii firmy aluminiowe w przyszłości. Słowa kluczowe Słowa kluczowe: aluminium, konkurencyjność, sektor aluminiowy, przewaga konkurencyjna, struktura sektorowa, konkurencja międzynarodowa.
Przemysł aluminiowy jest jedną z najbardziej konkurencyjnych branż w Brazylii. Odpowiada za około 10% bilansu handlowego Brazylii. Ekspansja tej branży na rynku międzynarodowym odbywała się w obliczu niedoborów energii w krajach rozwiniętych oraz w czasie recesji gospodarczej w Brazylii. Analiza uwarunkowań przewagi konkurencyjnej kraju. pozwala ci zrozumieć wysoki poziom konkurencyjność tego sektora przemysłu. Zwrócono również uwagę na kilka ważnych czynników, które mogą wpłynąć na pozycję konkurencyjną brazylijskich firm aluminiowych.
Nie wiadomo na ile prawdziwa jest ta historia, ale opisywane wydarzenia miały miejsce 2000 lat przed odkryciem przez ludzkość metody produkcji aluminium. Stało się to w 1825 roku, kiedy duński fizyk G. Oersted uzyskał kilka miligramów metalicznego glinu w wyniku termicznej redukcji chlorku glinu amalgamatem potasu.
Znaczne trudności w pozyskaniu aluminium powstały ze względu na następujące czynniki:
Słowa kluczowe: aluminium, konkurencyjność, przemysł aluminiowy, przewaga konkurencyjna, struktura przemysłu, Międzynarodowy Konkurs. Brazylijski przemysł aluminium pierwotnego bardzo intensywnie eksportuje, co w znacznym stopniu przyczynia się do nadwyżki handlowej Brazylii. Wkład sektora aluminium w nadwyżkę handlową Brazylii wyniósł 1,06 mld USD, czyli 9,6% całości. W skali globalnej sektor aluminium pierwotnego charakteryzuje się dojrzałym przemysłem, charakteryzującym się słabnącym wzrostem, nadwyżką mocy zainstalowanej i dużymi wahaniami międzynarodowych cen towarów.
Wysokie powinowactwo aluminium do tlenu. Aluminium można redukować tlenkiem węgla w temperaturze około 2000°C. Jednak już w 1200°C węgiel oddziałuje z aluminium, dając węglik;
Wysoki potencjał elektrochemiczny aluminium (-1,67V). Od roztwory wodne uzyskanie aluminium jest niemożliwe, ponieważ proces wydzielania wodoru (rozkład wody) praktycznie zachodzi na katodzie;
Wysoki stopień wewnętrznej rywalizacji, charakterystyczny dla dojrzewającego sektora, doprowadził do wycofania się wielu ważnych konkurentów, którzy kiedyś rywalizowali o ten rynek. Z drugiej strony, szczególne warunki czynników produkcji przyczyniły się do pojawienia się nowych konkurentów, w tym firm brazylijskich.
Aluminium pierwotne jest towarem notowanym na rynku głównym giełdy towarowe pokój. Producenci konkurują ze sobą o racjonalizację kosztów produkcji w celu maksymalizacji zysku w przedsiębiorstwie, ponieważ cena produktu jest wynikiem równowagi między podażą a popytem na świecie.
Wysoka temperatura topnienia tlenku glinu (2050°C), co wyklucza możliwość elektrolizy stopionego tlenku glinu.
Przemysłowa produkcja aluminium kojarzy się z nazwiskiem Francuza Henri Saint-Clair Deville. Doskonale zdawał sobie sprawę z eksperymentów G. Oersteda i innego naukowca, F. Wehlera, któremu w 1827 roku udało się wyizolować ziarna aluminium. Powodem niepowodzenia F. Wöhlera było to, że ziarna te w powietrzu zostały natychmiast pokryte najcieńszą warstwą tlenku glinu.
Głównym źródłem produkcji aluminium jest energia elektryczna, której w Brazylii wciąż nie brakuje, ale ze względu na rosnący popyt krajowy i brak inwestycji w sektorze wytwarzania energii coraz mniej. Ponieważ przemysł aluminiowy jest bardzo energochłonny, oczekuje się, że jego międzynarodowa pozycja konkurencyjna znacznie spadnie wraz z pojawieniem się scenariusza niedoboru energii.
W artykule dokonano analizy brazylijskiego przemysłu aluminiowego w celu zidentyfikowania i oceny determinant międzynarodowej konkurencyjności tego sektora. W tym celu korzystamy z ramowej pracy zaproponowanej przez Portera 1, pochodzącej z badania przewag komparatywnych dziesięciu krajów uprzemysłowionych, które są liderami na światowym rynku produktów uprzemysłowionych.
Przede wszystkim A.S.-K. Deville w procesie pozyskiwania metalu zastępuje potas tańszym sodem i przeprowadza na dużą skalę eksperymenty laboratoryjne. Powstały chlorek glinu został załadowany do dużej stalowej rury, w której naczynia wypełnione metaliczny sód. Podczas ogrzewania chlorek glinu oddziaływał z sodem w fazie gazowej i cząstki glinu osadzały się na dnie probówki. Ziarna powstałe w wyniku reakcji starannie zebrano, przetopiono i otrzymano wlewki metalowe.
Całkowity obrót przemysłu aluminium pierwotnego wyniósł 35,1 miliarda dolarów. Wielkość produkcji sięgnęła 980 tys. ton, czyli o 2,1% więcej niż rok wcześniej. 3. Ta branża ma wszystko cechy charakterystyczneświatowy przemysł. Firmy produkcyjne działają na arenie międzynarodowej, wydobywając rudy, przetwarzając tlenek glinu, wytwarzając aluminium i komercjalizując metal w postaci pierwotnej lub półprzekształconej, w krajach stwarzających dogodne warunki lokalne lub ze względu na dostępność zasoby naturalne lub w związku z dotacjami i strukturami zachęt dla organizacji pozarządowych.
Nowy sposób produkcji aluminium okazał się bardzo pracochłonny. Ponadto oddziaływanie par chlorku glinu z sodem często przebiega z wybuchem. W warunkach laboratoryjnych nie stanowiło to poważnego zagrożenia, ale w warunkach fabrycznych mogło spowodować katastrofę. ZAPYTAĆ. Deville zastąpił chlorek glinu mieszaniną AlCl3 z NaCl. Teraz uczestnicy reakcji byli w stanie stopionym. Eksplozje ustały, ale co najważniejsze, zamiast małych metalowych kulek, które trzeba było zbierać ręcznie, dostały znaczną ilość płynnego aluminium.
Po krzemie aluminium jest najpowszechniejszym metalem w skorupa Ziemska. Oprócz tego, że występuje w dużej ilości, aluminium można uzyskać w niezwykle prostym i dobrze znanym procesie chemicznym: elektrolitycznej redukcji tlenku glinu, który jest rafinowany z zanieczyszczonego uwodnionego tlenku glinu, który występuje w rudzie boksytu. 4 Wadą tego procesu jest jednak konsumpcja duża liczba energii elektrycznej, która jest jedną z głównych przyczyn stosunkowo wysokiej ceny tego metalu.
Dzięki ich właściwości fizyczne aluminium jest metalem szeroko stosowanym jako surowiec do wielu produktów przemysłowych. Zasadniczo aluminium jest plastycznym, ciągliwym, odpornym na korozję materiałem o wysokiej przewodności cieplnej i elektrycznej i jest bardzo lekki. Takie cechy uzasadniają zastosowanie tego materiału w kilku ważnych segmentach przemysłu, takich jak: silniki, samoloty, przewody elektryczne, ramy metalowe, pojemniki i opakowania, elementy mechaniczne i konstrukcyjne maszyn i pojazdów itp.
Eksperymenty w zakładzie Javel zakończyły się sukcesem. W 1855 r. uzyskano pierwszy wlewek metalu o wadze 6–8 kg.
Pałeczkę produkcji aluminium metodami chemicznymi kontynuował rosyjski naukowiec N. N. Beketov. Przeprowadził reakcję interakcji między kriolitem (Na 3 AlF 6) a magnezem. Metoda N. N. Beketova niewiele różniła się od metody A.S.-K. Deville, ale było łatwiej. W niemieckim mieście Gmelingem w 1885 r. wybudowano fabrykę metodą N. N. Beketowa, w której w ciągu pięciu lat uzyskano 58 ton aluminium - ponad jedną czwartą całej światowej produkcji metali środkami chemicznymi w okresie od 1854 r. do 1890 roku.
Pomimo szerokiego zakresu zastosowań i zastosowań tego metalu, przemysł aluminiowy charakteryzuje się dużą koncentracją. Sześciu największych producentów aluminium pierwotnego zajmuje około 50% światowego rynku. Są to Alcoa, Alean, Kaiser, Reynolds, Alussiusse i Peshine. Jednak pierwszy szok naftowy uruchomił głęboki proces restrukturyzacji sektorowej, który m.in. ograniczył koncentrację tego przemysłu. 5 Nowy poziom cen energii to nie tylko znaczny wzrost kosztów produkcji i stopniowy wzrost cen produktów, ale także gwałtowne zmniejszenie światowego popytu.
Pozyskiwanie aluminium środkami chemicznymi nie mogło zapewnić przemysłowi taniego metalu. Był nieproduktywny i nie dawał czystego aluminium bez zanieczyszczeń. To sprawiło, że badacze różnych krajówświat w poszukiwaniu nowych sposobów produkcji aluminium.
Przyszedł z pomocą naukowcom Elektryczność. W 1808 roku G. Davy próbował rozłożyć tlenek glinu za pomocą potężnej baterii elektrycznej, ale bezskutecznie. Prawie 50 lat później R. Bunsen i A.S.-K. Deville niezależnie przeprowadził elektrolizę mieszaniny chlorków glinu i sodu. Mieli więcej szczęścia niż ich poprzednicy i udało im się uzyskać małe kropelki aluminium. Jednak w tamtych czasach wciąż nie było tanich i wystarczająco mocnych źródeł energii elektrycznej. Dlatego elektroliza aluminium miała jedynie znaczenie teoretyczne.
Zmiany kursów walut i stopy procentowe doprowadziło do spadku handlu międzynarodowego i ogólnej działalności przemysłowej. Ponieważ aluminium jest surowcem o szerokim zastosowaniu przemysłowym, naturalne jest, że ograniczenie działalności gospodarczej w krajach uprzemysłowionych doprowadzi do zmniejszenia jego zużycia. Ten odwrót przerósł jednak wszelkie oczekiwania sektora. Po tym można zaobserwować spadek światowego zużycia aluminium pierwotnego.
Zwłaszcza Brazylia posiadała nie tylko zamożnych zasoby wodne, ale także duże zapasy boksytu o wysokiej zawartości glinu. W tym kontekście brazylijski przemysł aluminiowy rozwinął się i osiągnął znaczącą pozycję wśród krajów eksportujących ten produkt.
W 1867 wynaleziono dynamo i wkrótce nauczyli się przesyłać prąd na duże odległości. Elektryczność zaczęła atakować przemysł.
W 1886 roku P. Héroult we Francji i C. Hall w USA niemal równocześnie położyły podwaliny pod nowoczesną metodę produkcji aluminium, proponując otrzymanie go przez elektrolizę tlenku glinu rozpuszczonego w stopionym kriolicie (metoda Halla-Héraulta). Od teraz nowy sposób produkcja aluminium zaczyna się szybko rozwijać, czemu sprzyjała poprawa elektrotechniki, a także opracowanie metod pozyskiwania tlenku glinu z rud aluminium. Znaczący wkład w rozwój produkcji tlenku glinu wnieśli rosyjscy naukowcy K. I. Bayer, D. A. Penyakov, A. N. Kuznetsov, E. I. Zhukovsky, A. A. Yakovkin i inni Carska Rosja nie miała własnego przemysłu aluminiowego. Jednak pierwsze badania teoretyczne w dziedzinie elektrolizy aluminium należały do wybitnego rosyjskiego naukowca, twórcy elektrometalurgii metali nieżelaznych w naszym kraju, prof. P.P. Fedotiew. W 1912 wraz z V.P. Ilyinsky opublikował pracę „Experimental; Research on the Electrometalurgia of Aluminium”, która została natychmiast przetłumaczona na wiele języków. języki obce i stał się podręcznikiem dla metalurgów na całym świecie. P.P. Fedotiew i Ilyinsky w St. Petersburg Polytechnic Institute (St. Petersburg State Technical University) przeprowadzili dokładne badania nad wyborem optymalnego składu elektrolitu, a także dowiedzieli się, jak rozpuszczalność tlenku glinu w kriolicie i temperatura krystalizacji dodatku fluorków sodu, glinu i wapnia.
Po szoku naftowym utrzymanie cen aluminium na stabilnym poziomie stało się prawie niemożliwe. Widać, że rynek charakteryzuje się częstą nierównowagą między podażą a popytem, a ceny produktów odzwierciedlają tę nierównowagę. Biorąc pod uwagę względną obfitość rudy aluminium na powierzchni Ziemi, elektryczność jest rzadkim źródłem aluminium.
Jest to sektor głęboko niejednorodny, z bardzo starymi obiektami współistniejącymi z fabrykami o wysokim stopniu zaawansowania technologicznego na całym świecie. Kilka czynników wpływa na eksploatację zacofanych technologicznie fabryk, w tym: dotacje rządowe, dostępność preferowanych źródeł energii elektrycznej, długi okres eksploatacji urządzeń oraz duży kapitał wymagany przez urządzenia do produkcji aluminium.
28 marca 1929 r. W gazecie Leningradskaja Prawda opublikowano artykuł, w którym podano, że z jednej kąpieli po raz pierwszy uzyskano 8 kg metalicznego aluminium w zakładzie pilotażowym zakładu Krasny Wyborżec. To był początek naszej branży aluminiowej.
W 1931 Instytut Badawczy Przemysłu Aluminium-Magnez (VAMI) został zorganizowany w 1932 roku. Wołchowski został uruchomiony, aw 1933 roku. - Zakłady aluminiowe Dnipro. Od tego czasu przemysł aluminiowy zaczął się dynamicznie rozwijać w różnych częściach kraju.
Strukturę średnich kosztów produkcji zaawansowanej technologicznie instalacji aluminium pierwotnego przedstawia tabela 1. 9 Sprawdzono, że 33,9% do 38,2% kosztów produkcji jest związanych z amortyzacją kapitału. Działania są zatem zwykle kapitałochłonne.
Produkcja aluminium została wprowadzona do Brazylii wkrótce po II wojnie światowej w ramach szerokiego procesu substytucji importu, który charakteryzował brazylijską gospodarkę w tym okresie. Produkcja wróciła głównie na rynek krajowy. Systematycznie wybierana jako najlepsza w tym roku w branży metalurgicznej, która obejmuje przedsiębiorstwa produkujące metale nieżelazne.
2. Podstawy elektrolizy stopów kriolit-tlenek glinu
Elektroliza stopów kriolit-tlenek glinu jest główną metodą otrzymywania aluminium, chociaż niektóre stopy aluminium wytwarzany w procesie elektrotermicznym.
Pierwsze elektrolizery przemysłowe były przystosowane do prądów do 0,6 kA, aw ciągu następnych 100 lat wzrosła do 300 kA. Nie przyniosło to jednak istotnych zmian w podstawach procesu produkcyjnego.
W sektorze panuje duża niestabilność dotycząca rentowności firm. handel międzynarodowy w coraz większym stopniu oparte na ekonomii skali, przywództwie technologicznym i zróżnicowanych produktach. W tym kontekście tylko firmy zdolne do produkcji w tych warunkach będą konkurencyjne na rynku światowym. Porter 13, analizując przewagi komparatywne krajów uprzemysłowionych, stwierdził, że wzorce konkurencji, a także źródła przewag komparatywnych różnią się znacznie w zależności od sektorów przemysłu, a nawet branych pod uwagę segmentów przemysłu.
Ogólny schemat produkcji aluminium pokazano na ryc. 2.1. Główną jednostką jest elektrolizer. Elektrolit to stopiony kriolit z niewielkim nadmiarem fluorku glinu, w którym rozpuszcza się tlenek glinu. Proces prowadzi się przy różnych stężeniach tlenku glinu od około 1 do 8% (wag.). Od góry anoda węglowa jest opuszczana do kąpieli, częściowo zanurzona w elektrolicie. Istnieją dwa główne rodzaje anod protektorowych: samopieczone i wstępnie wypiekane. Te pierwsze wykorzystują ciepło elektrolizy do prażenia masy anodowej, która składa się z mieszaniny koksu wypełniacza i spoiwa, paku. Wypiekane anody są wstępnie upieczoną mieszanką koksu i spoiwa smołowego. Technologia produkcji masy anodowej i anod wypalanych jest szczegółowo opisana w literaturze (patrz np.).
Ryż. 2.1. Schemat produkcji aluminium z tlenku glinu.
Stopione aluminium w temperaturze elektrolizy (950-960°C) jest cięższe od elektrolitu i znajduje się na dnie elektrolizera. Stopiony kriolit-tlenek glinu jest bardzo agresywny, czemu mogą przeciwdziałać materiały węglowe i niektóre nowe materiały. Z nich wykonana jest wewnętrzna wyściółka elektrolizera.
Aby przekonwertować AC na DC włączone nowoczesne fabryki stosowane są prostowniki półprzewodnikowe o napięciu 850V i współczynniku konwersji 98,5%, instalowane w krzemowej podstacji przekształtnikowej (KPP). Jedna jednostka prostownikowa daje prąd do 63 kA. Liczba takich jednostek zależy od wymaganej siły prądu, ponieważ wszystkie są połączone równolegle.
Proces zachodzący w elektrolizerze polega na elektrolitycznym rozkładzie tlenku glinu rozpuszczonego w elektrolicie. Aluminium jest uwalniane na płynnej katodzie aluminiowej, która jest okresowo wylewana za pomocą kadzi próżniowej i przesyłana do odlewni w celu zalania lub mieszalnika, gdzie w zależności od dalszego przeznaczenia metalu, stopy z krzemem, magnezem, manganem, miedzią są przygotowywane lub przeprowadzana jest rafinacja. Na anodzie węgiel jest utleniany przez uwolniony tlen. Gaz anodowy jest mieszaniną CO 2 i CO.
Elektrolizery są zwykle wyposażone w schrony usuwające spaliny oraz system czyszczenia. Zmniejsza to uwalnianie szkodliwych substancji do atmosfery. Proces technologiczny wymaga, aby schron był hermetyczny, aby umożliwić zasysanie gazu do kolektora za pomocą wentylatorów. W gazach usuwanych z elektrolizerów dominuje dwutlenek węgla (większość tlenku węgla spalana jest albo nad elektrolitem, albo w specjalnych palnikach za dzwonem zbiorczym gazu), azot, tlen, fluorki gazowe i stałe oraz cząstki pyłu glinowego. Do ich usuwania i przywracania do procesu wykorzystywane są różne schematy technologiczne.
Nowoczesne elektrolizery wyposażone są w automatyczny system podawania tlenku glinu (AAF) z czasem ładowania 10–30 min.
Całą reakcję zachodzącą w elektrolizerze można przedstawić równaniem
Tak więc teoretycznie do procesu elektrolizy zużywany jest tlenek glinu i węgiel anodowy, a także energia elektryczna niezbędna nie tylko do realizacji procesu elektrolitycznego - rozkładu tlenku glinu, ale także do utrzymania wysokiej temperatury pracy. W praktyce zużywana jest również pewna ilość soli fluorkowych, które odparowują i są wchłaniane przez wyściółkę. Aby uzyskać 1 tonę aluminium potrzebujesz:
Produkcja aluminium jest jednym z najbardziej energochłonnych procesów, dlatego huty aluminium budowane są blisko źródeł energii.
Wszystkie materiały wchodzące do elektrolizy muszą mieć: minimalna ilość zanieczyszczenia bardziej elektrododatnie niż aluminium (żelazo, krzem, miedź itp.), ponieważ zanieczyszczenia te prawie całkowicie przechodzą do metalu podczas elektrolizy.
3. Alternatywne sposoby pozyskiwania aluminium
Przemysłowa metoda wytwarzania aluminium przez elektrolizę stopów kriolit-tlenek glinu, pomimo jej długotrwałego stosowania, ma szereg znaczące niedociągnięcia: wysokie jednostkowe zużycie energii, niskie jednostkowe usuwanie metalu i żywotność elektrolizerów, wysokie koszty pracy i kapitału, uwalnianie szkodliwych substancji do atmosfery i wiele innych. W związku z tym proponuje się inne metody wytwarzania aluminium. Rozważmy niektóre z nich.
3.1. Produkcja elektrotermiczna stopów aluminium z krzemem.
Otrzymać czyste aluminium bezpośrednia redukcja jego tlenku jest niemożliwa. Procesy karbotermiczne wymagają wysokich temperatur (około 2000°C), aby zredukować tlenek glinu, a przy braku składników tworzących stop metal wiąże się z węglem, dając węglik glinu (A1 4 C 3). Wiadomo, że węglik glinu i aluminium są wzajemnie rozpuszczalne i tworzą bardzo ogniotrwałe mieszaniny. Ponadto A1 4 C 3 rozpuszcza się w A1 2 O 3, dlatego w wyniku redukcji tlenku glinu węglem otrzymuje się mieszaniny glinu, węglika i tlenku o wysokich temperaturach topnienia. Zwykle nie jest możliwe uwolnienie takiej masy z pieca. Nawet jeśli można to zrobić, koszt separacji będzie wysoki.
W naszym kraju po raz pierwszy na świecie opracowano i wdrożono na skalę przemysłową metodę wytwarzania krzemoglinu (stopów glinowo-krzemowych) o odpowiednio wysokich wskaźnikach technicznych i ekonomicznych.
Ogólny schemat technologiczny produkcji stopów aluminiowo-krzemowych przedstawiono na ryc. 3.1. Oprócz kaolinów (Al 2 O 3 × 2 SiO 2 × 2H 2 O) jako wsad można stosować cyjanity (Al 2 O 3 × SiO 2), distensilimanity (Al 2 O 3 × SiO 2) oraz boksyty o niskiej zawartości żelaza.
Stop po wytopie elektrycznym dostarczany jest do oczyszczania z zanieczyszczeń niemetalicznych. W tym celu dostarczany jest topnik składający się z mieszaniny kriolitu i chlorku sodu, który zwilża te zanieczyszczenia i „zbiera” je. Rafinowany glinokrzemian ma średni skład (%): A1 - 61; Si - 36; Fe - 1,7; Ti - 0,6; Zr - 0,5; Ca - 0,7. Stop ten nie nadaje się do produkcji siluminu i wymaga oczyszczenia z żelaza. Najpopularniejszą metodą oczyszczania jest mangan, który tworzy z żelazem ogniotrwałe związki międzymetaliczne.

Ryż. 3.1. Ogólny schemat produkcji stopów aluminiowo-krzemowych.
Powstały stop jest rozcieńczany technicznym aluminium elektrolitycznym lub aluminium wtórnym do składu odpowiadającego różnym gatunkom siluminu i odlewany we wlewki.
Zalety tej metody otrzymywania siluminu nad fuzją aluminium elektrolityczne z krzemem krystalicznym są następujące: duża moc pojedynczej jednostki – nowoczesne piece mają moc 22,5 MB×A, czyli około 30 razy większą od mocy elektrolizera o 160 kA, a co za tym idzie zmniejszenie ruchu towarowego , spadek kosztów kapitałowych i kosztów pracy; zastosowanie surowców o niskim module krzemowym, których zapasy są dość duże.
Teoretycznie czyste aluminium można wyizolować ze stopu aluminium i krzemu różnymi metodami. Jednak ze względu na złożoność projektowania sprzętowego i technologicznego w przemyśle metody te nie są obecnie wdrażane.
3.2. Proces subhalogenowy
Wiadomo, że jeśli ogrzewa się mieszaninę halogenku i zanieczyszczonego aluminium, to czyste aluminium jest uwalniane po obniżeniu temperatury. Odkrycie to wywołało zainteresowanie systemami aluminium-halogenek glinu. Stwierdzono, że metaliczne aluminium reaguje z AlX 3 (gdzie X oznacza halogen) w wysokiej temperaturze, tworząc podhalogenek glinu:
![]()
Ponieważ podhalogenek glinu jest produktem gazowym, równowaga przesuwa się w lewo wraz ze spadkiem temperatury. Na przykład, A1C1(G) można wytworzyć z Al i AlCl3 w strefie reakcyjnej w stosunkowo wysokich temperaturach, a następnie przenieść jako parę do zimniejszej strefy, gdzie dysproporcjonuje do czystego glinu i chlorku glinu. Stała równowagi dla systemu A1 - A1C1 3 jest wyższa niż dla systemu A1 - A1F 3, dlatego system chlorkowy może być stosowany w procesach przemysłowych. Temperatura tworzenia podchlorku wynosi około 1300°C pod ciśnieniem atmosferycznym. Proces ten jest szczególnie atrakcyjny w przypadku oddzielania aluminium od stopów, ponieważ halogenek glinu reaguje z aluminium i praktycznie nie wchodzi w interakcje z większością innych metali. Trudności pojawiają się tylko w przypadku niektórych lotnych halogenków amonu, takich jak FeCl 3 , MnCl 2 i niektórych innych. Mogą tworzyć mieszaniny z AlCl3 i zanieczyszczać powstały glin.
Alcan opracował technologię, która obejmuje pięć etapów:
1. Wytwarzanie surowego stopu, takiego jak żelazo-krzem-aluminium, w karbotermicznym piecu redukcyjnym.
2. Oddziaływanie między A1 i AJC1 w konwerterze w temperaturze 1300 °C.
3. Rozdzielanie lotnych halogenków i subhalogenków w kolumnach destylacyjnych.
4. Powrót AICI, do reakcji między chlorkiem a ciekłym stopem bogatym w aluminium.
5. Rozkład A1C1, produkcja aluminium i zwrot A1C1 3 do rektyfikacji.
Metoda podchlorkowa cieszy się największym zainteresowaniem w przemysłowej rafinacji stopów aluminium.
3.3. Ten proces
Schemat otrzymywania aluminium metodą Thota pokazano na ryc. 3.2. Surowce zawierające glin po odpowiednim przygotowaniu są chlorowane w złożu fluidalnym w obecności koksu i SiCl 4 . Ten ostatni służy do tłumienia reakcji chlorowania SiO 2 . W wyniku chlorowania w piecach fluidyzacyjnych (BF) powstaje mieszanina gazowo-parowa (VGM), w skład której wchodzą AlCl 3 , FeCl 3 , TiCl 4 i SiCl 4 . W pierwszym skraplaczu około 75% FeCl 3 w stanie stałym jest uwalniane z PGM i przesyłane do reaktora utleniacza, gdzie oddziałuje z tlenem atmosferycznym, w wyniku czego powstają Fe 2 O 3 i C1 2 . Chlor jest zwracany do chlorowania. W drugim skraplaczu uwalniany jest pozostały FeCl 3 i skrapla się A1C1 3 . W trzecim kondensatorze kondensują chlorki tytanu i krzemu. Oddzielanie tych chlorków odbywa się w kolumnie destylacyjnej.
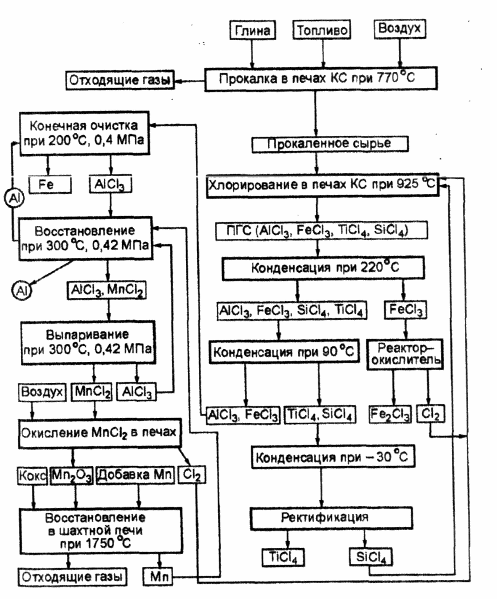
Ryż. 3.2. Schemat otrzymywania aluminium metodą Thotha.
Chlorki glinu i żelaza wyładowane z drugiego skraplacza są podgrzewane, pompowane do urządzenia do czyszczenia styków, gdzie stykają się w przeciwprądzie z ruchomą warstwą stałych cząstek aluminium. Tu zachodzi reakcja:
Oczyszczony chlorek glinu jest podawany do redukcji metalotermicznej. Dostępne technicznie środki redukujące, które mają większe powinowactwo do chloru niż aluminium, to sód, magnez i mangan. Jednak dwa pierwsze elementy drogi i ich produkcja są bardzo energochłonne. Dlatego, zdaniem twórców procesu, zastosowanie manganu ma pewne zalety, które można regenerować z chlorków metodą karbotermiczną przy znacznie mniejszym zużyciu energii. Podczas redukcji chlorku glinu manganem zachodzą następujące reakcje:
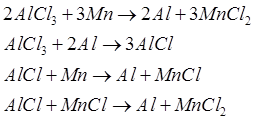
Glin z mieszaniny MnCl2 z nieprzereagowanym AlCl3 jest rozdzielany w separatorach cyklonowych, natomiast chlorki manganu i glinu są rozdzielane w wyparce. Chlorek glinu jest zawracany do reaktora w celu wytworzenia glinu, a chlorek manganu reaguje z tlenem, tworząc stałe tlenki manganu i chloru. Tlenek manganu jest redukowany do metalu metodą karbotermiczną w piecach szybowych, w których ładowany jest koks i wapień. Do pieca dodawany jest mangan, aby zrekompensować jego straty w trakcie procesu.
Wady tego procesu, jak również innych metod metalotermicznych, obejmują zanieczyszczenie powstałego produktu metalem redukującym, konieczność zorganizowania produkcji w celu regeneracji środka redukującego oraz wzrost kosztów kapitałowych.
Prace badawcze nad wytwarzaniem aluminium metodą redukcji manganem w skali laboratoryjnej i powiększonej prowadzono w latach 1966-1973. Następnie w literaturze nie było doniesień o rozwoju przemysłowym ten kierunek, co najwyraźniej wynika ze znacznych trudności w technicznej realizacji tego złożonego, wieloetapowego procesu.
3.4. Elektroliza stopionych chlorków
W styczniu 1973 roku firma Alcoa ogłosiła opracowanie nowej metody produkcji aluminium. Firma pracowała nad tym procesem przez 15 lat i wydała 23 miliony dolarów.
Metoda ta polega na produkcji chlorku glinu i jego późniejszej elektrolizie. W 1976 roku pojawiły się doniesienia o przejściu firmy "Alcoa" do przemysłowego wdrożenia technologii chlorkowej do produkcji aluminium. W mieście Palestyna (Teksas, USA) działał zakład o zdolności projektowej 30 tys. ton produkcji aluminium rocznie tą metodą.
Podstawowy schemat technologiczny pokazano na ryc. 2.4.

Ryż. 3.3. System technologii otrzymywanie aluminium z chlorku.
Chlorek glinu ma duże powinowactwo do wody oraz tendencję do tworzenia tlenków i chlorowodorków. W związku z tym uzyskanie go w czystej postaci jest trudnym zadaniem. Obecność wilgoci powoduje korozję, a obecność związków zawierających tlen prowadzi do wytrącania i utleniania anod. Firma „Alcoa” zaproponowała chlorowanie oczyszczonego tlenku glinu, co częściowo rozwiązuje te problemy. Jednak konieczne jest spełnienie zwiększonych wymagań dotyczących czystości węgla podczas chlorowania w stosunku do wodoru lub wilgoci.
Ostatnio pojawiły się doniesienia, że firmie Toth Aluminium Corporation udało się wyprodukować chlorek glinu zawierający co najmniej 99,97% głównego składnika na dużą skalę przemysłową.
Powstały chlorek glinu w postaci granulek lub pary jest poddawany elektrolizie. Elektrolizer zastosowany w tej technologii składa się ze stalowej obudowy wyłożonej cegłami szamotowymi oraz dodatkowo cegłami okrzemkowymi w dolnej części tj. termoizolacyjny nieprzewodzący materiał ogniotrwały, który słabo oddziałuje z roztopionymi chlorkami. Na dnie wanny znajduje się grafitowa komora do zbierania płynnego aluminium. W pokrywie ogniwa znajdują się otwory do ładowania chlorku glinu, okresowego odsysania glinu oraz ciągłego wyprowadzania gazowego chloru stosowanego do produkcji chlorku glinu. Ściany boczne i pokrywa elektrolizera są chłodzone wodą.
Elektroliza wykorzystuje grafitowe nie zużywające się elektrody. Ta zaleta (w porównaniu do elektrolizy stopów kriolit-tlenek glinu) wraz ze stosunkowo niską temperaturą procesu (około 700ºС) umożliwia całkowite uszczelnienie elektrolizerów.
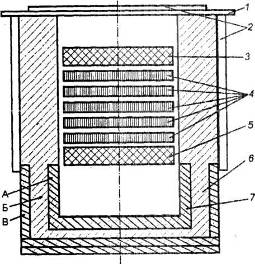
Ryż. 2.5. Schemat ogniwa elektrolitycznego z elektrodami bipolarnymi do elektrolizy chlorku glinu.
1 - osłona: 2 - chłodzenie wodne: 3 - anoda; 4 - elektrody bipolarne; 5 - katoda; 6 - podszewka; 7 - komora do zbierania aluminium. Materiał: A - grafit; B - szamot; B - okrzemka.
Elektrolityczny rozkład chlorku glinu teoretycznie wymaga wyższego napięcia niż elektroliza stopionego kriolit-tlenek glinu, ponieważ napięcie rozkładu chlorku glinu jest znacznie wyższe. Do wad procesu można więc zaliczyć konieczność dostarczenia dużej ilości ciepła do elektrolizera oraz znaczne straty napięcia. Jednak wysokie straty omowe i termiczne są znacznie zmniejszone, gdy stosuje się system elektrod bipolarnych. W ogniwie górna elektroda to anoda, dolna katoda, a pomiędzy nimi elektrody grafitowe, których górna część to katoda, a dolna to anoda. Jednocześnie wyniki obliczeń pokazują, że wraz ze wzrostem liczby elektrod bipolarnych i zmniejszeniem ich pola przekroju, prądy upływu rosną, tj. część prądu przepływa przez impregnowaną elektrolitem część okładziny oraz kanały między okładziną a dwubiegunami, bez wykonywania prac elektrochemicznych. Te prądy upływowe powodują zmniejszenie prądu wyjściowego.
Ze względu na bliskość temperatur topnienia i wrzenia pod ciśnieniem atmosferycznym chlorek glinu sublimuje praktycznie bez topienia. Temperatura sublimacji 180,2°C. Punkt potrójny odpowiada temperaturze 192,6°C i ciśnieniu bezwzględnemu 0,23 MPa. W związku z tym jako elektrolit stosuje się stopioną mieszaninę chlorku glinu (5 ± 2% (masa)), chlorku litu (~28% (masa)) i chlorku sodu (67% (masa)). W tych wytopach aktywność A1C1 3 spada. Wynika to w dużej mierze z faktu, że w stopionych mieszaninach chlorków A1C1 3 wiąże się na przykład z anionami złożonymi.
Odległość międzypolowa wynosi 1,0 - 1,5 cm, temperatura 700 ± 30ºС, gęstość prądu -0,8 - 2,5 A / cm2.
Wyniki.
Głównymi zaletami przewidzianymi i potwierdzonymi podczas przemysłowego wdrożenia w Stanach Zjednoczonych metody Alcoa wytwarzania aluminium metodą elektrolizy jego chlorków w porównaniu z elektrolizą stopów kriolit-tlenek glinu jest możliwość stosowania niskiej jakości surowców zawierających aluminium, zmniejszająca jednostkowy pobór mocy podczas elektrolizy o około 30% oraz eliminacja zużycia wysokiej jakości materiałów elektrodowych zawierających węgiel, stosowanie mniej rzadkich i agresywnych chlorków zamiast fluorków, zwiększenie wydajności pracy, zmniejszenie nakładów inwestycyjnych, zmniejszenie kosztów, kosztów produkty końcowe i szkodliwe emisje do środowiska.
Ostatnio zalety metody chlorkowej do produkcji aluminium stały się bardziej namacalne ze względu na wzrost kosztów energii elektrycznej, surowców do istniejącej przemysłowej metody produkcji aluminium oraz zwiększone wymagania dotyczące ochrony. środowisko oraz dotychczasowy brak pozytywnych wyników w otrzymywaniu czystego tlenku glinu z niskiej jakości surowców nieboksytowych.
Tak więc najbardziej obiecujący z alternatywne sposoby produkcja aluminium polega na elektrolizie chlorku glinu w elektrolizerach z elektrodami bipolarnymi.
Bibliografia
1. Rozen B. M., Rozen Ya B. Metal o szczególnej wartości. - M.: Metalurgia, 1975. - 128 s.
2. Kolodin E. A., Sverdlin V. A., Svoboda R. V. Produkcja wypalonych anod elektrolizerów aluminiowych. - M.: Metalurgia, 1980, - 84 s.
3. Yankho E. A., Vorobyov D. N. Produkcja masy anodowej. - M.: Metalurgia, 1975. - 128 s.
4. M. M. Vetkzhov, A. M. Ts’shlakov i S. N. Shkolnikov, Elektrometalurgia aluminium i magnezu. - M.: Metalurgia, 1987. - 320 s.
5. Shchenkov V.V., Litwak S.N. Rozwój nowych procesów technologicznych do produkcji aluminium Tsv. metalurgia: Bull. NTI / Informacje o kolorze. - 1974. - nr 9. - S. 38 - 41.
6. Sandler R. A., Rapier A. Kh. Elektrometalurgia aluminium i magnezu. - L: LGI, 1983. - 94 s.
UAB „Kazachstan elektroliza” (KEP), która jest częścią ENRC (Eurasian Natural Resources Corporation) – jedynej w Kazachstanie fabryki produkującej aluminium pierwotne. Zakład znajduje się w Pawłodarze. Otwarty w 2007 roku. W jego skład wchodzi wydział elektrolizy, odlewnia, wydział produkcji anod oraz inne wydziały pomocnicze. Na jego podstawie utworzono klaster hutniczy z pełny cykl produkcja: wydobycie boksytu, produkcja tlenku glinu, produkcja "skrzydlatego metalu". W ten moment zdolność produkcyjna zakładu wynosi 125 000 ton rocznie. Aluminium produkowane jest w dwudziestokilogramowych wlewkach w gatunku A-85 (zawiera 99,85% aluminium).
W międzyczasie zaczniemy studiować na zdjęciach technologię produkcji aluminium.
informacje ogólne
Aluminium - pierwiastek chemiczny trzecia grupa układ okresowy elementy D. I. Mendelejewa. Pod względem zawartości w skorupie ziemskiej aluminium zajmuje pierwsze miejsce wśród metali i trzecie wśród innych pierwiastków (po tlenie i krzemie). Skorupa ziemska to 8,8% aluminium (dla porównania zawartość żelaza w skorupie ziemskiej wynosi 4,2%, miedź - 0,003, złoto - 0,000005%). W naturze aluminium występuje tylko w postaci różnych i bardzo zróżnicowanych związków. Większość z nich to tlenek glinu - w życiu codziennym nazywa się go tlenkiem glinu, czyli po prostu gliną. Glina stanowi około jednej trzeciej tlenku glinu i jest potencjalnym surowcem do jej produkcji.
Aluminium posiada szereg właściwości, które odróżniają go od innych metali. Jest to niska gęstość aluminium, dobra ciągliwość i wystarczająca wytrzymałość mechaniczna, wysoka przewodność cieplna i elektryczna. Aluminium jest nietoksyczne, niemagnetyczne i odporne na korozję na wiele substancje chemiczne.
Najważniejszymi odbiorcami aluminium i jego stopów są przemysł lotniczy i motoryzacyjny, transport kolejowy i wodny, inżynieria mechaniczna, przemysł elektrotechniczny i oprzyrządowania, inżynieria przemysłowa i lądowa, przemysł chemiczny oraz produkcja dóbr konsumpcyjnych.
Produkcja aluminium
Istotą procesu produkcji aluminium jest otrzymanie bezwodnego, wolnego od zanieczyszczeń tlenku glinu (tlenku glinu), a następnie produkcja aluminium metalicznego poprzez elektrolizę rozpuszczonego w kriolicie tlenku glinu.
Proces technologiczny otrzymywania aluminium składa się z dwóch głównych etapów:
Otrzymywanie tlenku glinu (Al 2 O 3) z rud aluminium;
Elektroliza i rafinacja aluminium z tlenku glinu;
Tlenek glinu otrzymuje się z boksytów przez traktowanie ich alkaliami. Powstały glinian sodu poddaje się hydrolizie. W rezultacie wytrącają się kryształy wodorotlenku glinu. Wodorotlenek glinu jest odwadniany przez ogrzewanie w piecach obrotowych w celu uzyskania odwodnionego tlenku glinu.
Do produkcji kriolitu najpierw otrzymuje się fluorowodór z fluorytu, a następnie kwas fluorowodorowy. Do roztworu kwasu fluorowodorowego wprowadza się wodorotlenek glinu, w wyniku czego powstaje kwas fluoroglinowy, który neutralizuje się sodą i uzyskuje się kriolit, który wytrąca się. Jest filtrowany i suszony w bębnach suszących.
W ten sposób uzyskuje się tlenek glinu, który jest szarym proszkiem. Kolejnym zadaniem jest wyizolowanie z niego czystego aluminium za pomocą elektrolizy. Teraz zaczyna się zabawa:
Warsztat do produkcji anod
2. Przemysł aluminiowy jest głównym konsumentem elektrod węglowych, które służą do dostarczania prądu do elektrolitu w elektrolizerach.
3. Tutaj produkowane są prasowane, wstępnie wypalone elektrody.
4. Anoda jest blokiem pryzmatycznym, na którego górnej płaszczyźnie znajduje się kilka gniazd smoczkowych (wgłębień).
5. Bloki anodowe produkowane są z niskopopiołowego i niskosiarkowego koksu.
6. Do doprowadzenia prądu do anody stosuje się złączki stalowe, które wkłada się w kielichy złączki i wypełnia roztopionym żelazem lub uszczelnia pastą węglową.
7. Do produkcji wyrobów zawierających węgiel stosuje się stałe materiały zawierające węgiel, które stanowią podstawę elektrody oraz spoiwa substancji zawierających węgiel, które wypełniają szczeliny między ziarnami stałych materiałów zawierających węgiel. Podczas wypalania produktów spoiwa koksują i mocno wiążą ze sobą ziarna stałych materiałów węglowych.
Sklep elektrolizy
10. Nowoczesna elektroliza to wyodrębniona terytorialnie i administracyjnie samonośna jednostka z pełnym cyklem produkcyjnym - od magazynów odbiorczych surowców po magazyny produktów handlowych, których podstawą jest jedna lub więcej serii połączonych szeregowo wanien elektrolizy.
11. Elektrolizer jest kąpielą stopionego kriolitu, podwójnego fluorku sodu i glinu, w której rozpuszcza się 3–5% tlenku glinu, pływającego na złożu stopionego aluminium. Pręty stalowe przechodzące przez palenisko z płyt węglowych są wykorzystywane do zasilania katody, natomiast pręty węglowe zawieszone w stopionym kriolicie służą jako anody. Temperatura robocza procesu jest bliska 950°C, czyli znacznie wyższa niż temperatura topnienia aluminium. Temperatura w kąpieli elektrolitycznej jest kontrolowana przez zmianę szczeliny między anodami a metalowym odbiornikiem katody, na którym osadza się roztopione aluminium.
14. Ciekłe aluminium uwolnione na dnie, które służy jako katoda, jest cięższe od stopionej soli elektrolitu, dlatego jest gromadzone na podłożu węglowym, skąd jest okresowo wypompowywane. Od góry w elektrolicie zanurzone są anody węglowe, które spalają się w atmosferze tlenu uwalnianego z tlenku glinu, z wydzielaniem się tlenku węgla CO i dwutlenku węgla CO 2 .
15. Prąd na elektrolizerach wynosi 150 000 A. Napięcie robocze na kąpieli wynosi 4-5 V. W pobliżu elektrolizerów występuje silne pole elektromagnetyczne.
16. Specjalna maszyna do transportu palet anodowych. Służą do transportu świeżych anod i żużli anodowych pomiędzy wydziałem montażu anod (AMO) a budynkiem elektrolizy.
17. Gabaryty warsztatu robią wrażenie. Za tym samym rzędem doniczek, a obok niego drugi warsztat podobnej wielkości.
18. Dla produkcji tlenku glinu, soli fluorkowych i produktów węglowych typowy jest wymóg maksymalnego stopnia czystości tych materiałów.
19. Skład elektrolitu przemysłowych elektrolizerów aluminium, oprócz głównych składników - kriolitu, fluorku glinu i tlenku glinu, zawiera niewielkie ilości (łącznie do 8-9%) niektórych innych soli, które poprawiają niektóre właściwości fizykochemiczne elektrolitu, a tym samym zwiększyć wydajność elektrolizerów.
20. Gdy elektrolit wyczerpuje się z tlenku glinu, wprowadzana jest do niego kolejna porcja tlenku glinu.
odlewnia
21. Odlewnia zlokalizowana jest na terenie wydziału elektrolizy w taki sposób, aby drogi transportu ciekłego metalu z budynków elektrolizy do wydziału odlewni były minimalne. Głównym wyposażeniem tego wydziału są piece obrotowe (miksery) z ogrzewaniem elektrycznym.
22. Zwykle w celu poprawy jakości produktów instaluje się szeregowo dwa sparowane piece płomienne, z których jeden (osadnik) jest przeznaczony do odbioru, osiadania, uśredniania temperatury i składu metalu, a drugi (odlewania) do odlewania z tego różnego rodzaju produkty. System pieców stacjonarnych, w przeciwieństwie do obrotowych, umożliwia prowadzenie procesu ciągłego odlewania.
23. Płynne aluminium trzyma się w piecu elektrycznym przez 30-45 minut w temperaturze 690-730 ° C, aby wtrącenia niemetaliczne unosiły się i uwalniały gazy z metalu.
24. Zanieczyszczenia są usuwane przez rafinację, w której przedmuchiwany jest chlor
stop aluminium. Powstały parowy chlorek glinu, przechodząc przez stopiony metal, otacza cząsteczki zanieczyszczeń, które unoszą się na powierzchni metalu, gdzie są usuwane. Chlorowanie glinu pomaga również usunąć Na, Ca, Mg i gazy rozpuszczone w aluminium. Po rafinacji czystość aluminium pierwotnego wynosi 99,5-99,85%.
25. Zalewanie wlewków małogabarytowych do form odbywa się na napełniarce przenośnikowej wyposażonej w urządzenie do mechanicznego znakowania wlewków oraz w układ chłodzenia form powietrzem lub wodą.
26. Wlewanie metalu do form odbywa się krótkim, równomiernym strumieniem. Po napełnieniu form warstewka tlenków jest usuwana z powierzchni metalu.
27. Urządzenie do mechanicznego znakowania wlewków.
28. Odlane wlewki są układane w stosy za pomocą układarki wlewków zainstalowanej na końcu maszyny przenośnikowej.
29. Potem produkt końcowy pakowane w palety po 1000 kg i wysyłane do magazynu.
30. Produkcja jednej tony aluminium wymaga około 14 000 kilowatogodzin energii elektrycznej i około dwóch ton tlenku glinu. Jednocześnie do wyprodukowania jednej tony tlenku glinu potrzeba około 5 ton rudy boksytu. Obecnie cena aluminium na Londyńskiej Giełdzie Metali wynosi 2600 USD za tonę.
Wideo z zakładu elektrolizy. Popełniłem mały błąd, próbując jednocześnie zrobić zdjęcie i film, w wyniku czego film zatrzymuje się w momencie naświetlania.
Książka do samodzielnej nauki.


