Производство на алуминий
Подобни резюмета:
електролиза на алуминий. Определяне на размерите на анода. Размери на структурните елементи на сглобяемото катодно устройство. Материално, електрическо и енергийно изчисление на електролизера, неговата производителност и разход на суровини за производство на алуминий.
Промишлено значение на цветните метали: алуминий, мед, магнезий, олово, цинк, калай, титан. Технологични процеси на производство и обработка на метали, механизация и автоматизация на процесите. Производство на мед, алуминий, магнезий, титан и техните сплави.
Споменавания на нефт в писанията на древни историци и географи. Нефтът през 20 век като основна суровина за производството на гориво и много органични съединения. Технологични процеси на дестилация на нефт: термичен, каталитичен крекинг, риформинг.
AT последните годиниВъв връзка с развитието на нови специални области на технологията широко се използват топлоустойчиви сплави, които са способни да издържат на малки пластични деформации при високи температури без разрушаване за дълго време.
Суровини за топене на желязо. Устройство за доменна пещ. Топене на стомана в кислородни конвертори, мартенови, електрически пещи. Продукти от доменни пещи. Производство на мед, алуминий. Термична и химико-термична обработка на стомана.
Ремонт на автомобил след удар с алуминиев тиган в твърд предмет. Основните трудности при заваряването на алуминий и неговите сплави. Заваряване с волфрамов електрод с променлив симетричен ток. Ремонтна техника, оборудване за заваряване. Контрол на заварките.
Цветната металургия като най-конкурентната индустрия в Русия, инвестиционна политика. Цветни метали и сплави: мед, алуминий, цинк, магнезий; техните технологични и механични свойства, приложение в промишлеността и строителството.
основни характеристикимокри и сухи методи за пречистване на газови емисии по време на електролиза на алуминий. Химия на процесите на мокро и сухо газоочистване, тяхната ефективност в зависимост от режима на работа. Характеристики на обработката и обезвреждането на получените разтвори.
Пластмасите (пластмасите) като основен вид неметални материали. Основни технологични и експлоатационни свойства на пластмасите. Термопластични и термореактивни материали. Класификация на пластмасите в зависимост от основното им предназначение.
Метод за извършване на металографски анализ на месингова сплав LA77–2. Скица на микроструктурата на тази сплав на медна основа. Привеждане на необходимата диаграма на състоянието. Пристрастяване механични свойствас концентрация на мед в месингова сплав LA77–2.
Методи за получаване на алуминиево-силициеви сплави. Процес на карботермична редукция на оксиди на силиций и алуминий. Механизъм и кинетика на процеса на редукция на алумосиликатни смеси в гамата от алуминиеви силиконови състави с използване на редуциращ агент.
Име и история на откритието. Общи характеристики на алуминия. Намиране в природата. алуминиеви сплави. Получаване на отливки от алуминиеви сплави. Контрол на качеството на отливките и корекция на дефекти.
Стокова характеристика на цветните метали и изделията от тях. Изисквания за цветни метали и сплави в съответствие с GOST. Физични свойстваосновни (мед, олово, цинк, калай, никел, титан, магнезий), легиращи, благородни и разпръснати метали.
Въведение. Преди около 100 години Николай Гаврилович Чернишевски каза за алуминия, че този метал е предопределен за голямо бъдеще, че алуминият е металът на социализма. Оказва се визионер: през 20в. елемент № 13 алуминият стана основата на много структурни материали. Елемент от 3-ти период и IIIA-група Пери...
Характеристики на алуминия и неговите сплави. Технологичен процеспроизводството на алуминий и използването на "ишлеме" в производството. състояние алуминиева индустрияи световния пазар на алуминий в края на 2007 г. - началото на 2008 г. Използването на алуминий и неговите сплави.
Състав, свойства на електролита. Структура на криолитно-алуминиевите стопилки. Плътност на алуминиевия електролит. Повърхностно напрежение, налягане на наситени пари. Аноден ефект: положителни и отрицателни действия. Напрежение на разлагане. механизъм на електролизата.
Класификация на цветни метали, характеристики на тяхната обработка и обхват. Производство на алуминий и неговите свойства. Класификация на електрическите материали. Енергийна разлика между метални проводници и полупроводници и диелектрици.
Сравнителен анализсвойства на материалите за производство на нишки и термодвойки. Характеристики на волфрама и устройството на термодвойка като система от различни проводници. Свойства и обхват на термодвойка тел: алуминий, хромел, копел.
КАК СЕ ПРОИЗВЕДЕ
АЛУМИНИЕВ
Въпреки факта, че алуминият е най-разпространеният метал на нашата планета, в чистода не се намери на земята. Поради високата химическа активност алуминиевите атоми лесно образуват съединения с други вещества. В същото време "крилатият метал" не може да бъде получен чрез топене на руда в пещ, както се случва например с желязото. Процесът на получаване на алуминий е много по-сложен и се основава на използването на електричество с голяма мощност. Затова алуминиевите заводи винаги се изграждат в близост до големи източници на електроенергия - най-често водноелектрически централи, които не замърсяват околен свят. Но на първо място.
 Добив на боксит
Добив на боксит
Производството на метали е разделено на три основни етапа: извличане на боксит - алуминиева руда, преработката им в алуминиев оксид - алуминиев оксид и накрая производството на чист метал чрез електролиза - разграждането на алуминиевия оксид на неговите съставни части под въздействието на електрически ток. От 4-5 тона боксит се получават 2 тона алуминий, от които се произвежда 1 тон алуминий.
В света има няколко вида алуминиеви руди, но бокситът е основната суровина за производството на този метал. Това е скала, състояща се главно от алуминиев оксид с примес на други минерали. Бокситът се счита за висококачествен, ако съдържа повече от 50% алуминиев оксид.
Бокситите могат да бъдат много различни един от друг. По структура те са твърди и плътни или рохкави и ронливи. На цвят - като правило, тухленочервено, червеникаво или кафяво поради примеса на железен оксид. С ниско съдържание на желязо, бокситите са бели или сиви на цвят. Но понякога има жълти руди, тъмнозеленои дори пъстър - със сини, червено-виолетови или черни ивици.
Около 90% от световните запаси на боксит са съсредоточени в страните от тропическия и субтропичния пояс - 73% от тях са в пет държави: Гвинея, Бразилия, Ямайка, Австралия и Индия. Най-много боксит има в Гвинея – 5,3 млрд. тона (28,4%), докато те Високо качество, съдържат минимално количествопримеси и лежат почти на повърхността.
Най-често се добива боксит отворен път- със специално оборудване рудата се "отрязва" слой по слой от повърхността на земята и се транспортира за по-нататъшна обработка. Въпреки това, има места в света, където алуминиевата руда лежи много дълбоко и за нейното извличане е необходимо да се изградят мини - една от най-дълбоките мини в света "Черемуховская-Глубокая" се намира в Русия, в Урал, дълб. е 1550 метра.
 Производство на алуминий
Производство на алуминий
Следващата стъпка в производствената верига е преработката на боксита в алуминиев оксид - алуминиев оксид Al2O3, който е бял ронлив прах. Основният начин за получаване на алуминиев оксид в света е методът на Байер, открит преди повече от сто години, но все още актуален - около 90% от алуминиевия оксид в света се произвежда по този начин. Този метод е много икономичен, но може да се използва само при обработка на висококачествени боксити със сравнително ниско съдържание на примеси - предимно силициев диоксид.
Методът на Байер се основава на следното: кристалният алуминиев хидроксид, който е част от боксита, се разтваря добре при висока температура в разтвор сода каустик(каустик алкали, NaOH) с висока концентрация и когато температурата и концентрацията на разтвора се понижат, той кристализира отново. Външните вещества, които са част от боксита (така наречения баласт), не преминават в разтворима форма или прекристализират и се утаяват преди кристализацията на алуминиев хидроксид. Следователно, след разтварянето на алуминиевия хидроксид, баластът може лесно да се отдели - нарича се червена кал.
Големите частици алуминиев хидроксид лесно се отделят от разтвора чрез филтриране, измиват се с вода, сушат се и се калцинират - т.е. нагряват се, за да се отстрани водата. Така се получава двуалуминиев оксид.
Двуалуминиевият оксид няма срок на годност, но не е лесно да го съхранявате, тъй като при най-малката възможност той активно абсорбира влагата - затова производителите предпочитат да го изпращат на производство на алуминий. Първо, алуминиевият оксид се подрежда на купчини с тегло до 30 хиляди тона - получава се един вид бутер торта с височина до 10-12 метра. След това тортата се „нарязва“ и се зарежда за изпращане до железопътни вагони - средно от 60 до 75 тона на вагон (в зависимост от вида на самия вагон).
Има и друг, много по-рядко срещан начин за получаване на алуминиев оксид - методът на синтероване. Същността му е да се получи твърди материалиот прах при повишена температура. Бокситите се синтероват със сода и варовик - те свързват силициевия диоксид във водонеразтворими силикати, които лесно се отделят от алуминиевия оксид. Този метод е по-скъп от метода на Байер, но в същото време дава възможност за обработка на боксит с високо съдържание на вредни примеси от силициев диоксид.
![]() Криолит
Криолит
Алуминиевият оксид е директен източник на метала в процеса на производство на алуминий. Но за да се създаде среда, в която ще протича този процес, е необходим още един компонент - криолит.
Това е рядък минерал от групата на естествените флуориди със състав Na3AlF6. Обикновено образува безцветни, бели или опушеносиви кристални агрегати със стъкловиден блясък, понякога почти черни или червеникавокафяви. Криолитът е крехък и лесно се топи.
Има много малко естествени находища на този минерал, така че изкуственият криолит се използва в промишлеността. В съвременната металургия се получава чрез взаимодействие на флуороводородна киселина с алуминиев хидроксид и сода.
Производство на алуминий
И така, добихме боксит, получихме алуминиев оксид от него, запасихме се с криолит. Всичко е готово за последния етап - електролиза на алуминий. Цехът за електролиза е сърцето на алуминиев завод и не е като цеховете на други металургични предприятия, произвеждащи например желязо или стомана. Състои се от няколко правоъгълни сгради, чиято дължина често надхвърля 1 км. Стотици електролизни клетки са инсталирани в редове вътре, свързани последователно с масивни проводници към електричество. Постоянно наляганена електродите на всяка баня е в диапазона само 4-6 волта, докато силата на тока е 300 kA, 400 kA и повече. Електрическият ток е основната производствена сила тук - в този цех има много малко хора, всички процеси са механизирани.
Във всяка вана протича процесът на електролиза на алуминий. Резервоарът за баня е пълен с разтопен криолит, който създава електролитна (проводима) среда при температура 950°C. Ролята на катод се изпълнява от дъното на ваната, а анодът е въглищни блокове, потопени в криолит с дължина около 1,5 метра и ширина 0,5 метра, отстрани изглеждат като впечатляващ чук.
На всеки половин час нова порция суровини се зарежда във ваната с помощта на автоматична система за подаване на алуминиев оксид. Под въздействието на електрически ток връзката между алуминия и кислорода се прекъсва - алуминият се отлага на дъното на ваната, образувайки слой от 10-15 cm, а кислородът се свързва с въглерода, който е част от анодните блокове, и образува въглероден диоксид.
Приблизително веднъж на всеки 2-4 дни алуминият се отстранява от ваната с помощта на вакуумни черпаци. В замръзналата върху повърхността на ваната електролитна кора се пробива дупка, в която се спуска тръбата. През него в черпака се засмуква течен алуминий, от който предварително е изпомпван въздух. Средно около 1 тон метал се изпомпва от една баня, а около 4 тона разтопен алуминий могат да бъдат поставени в един коф. След това този черпак се изпраща в леярната.
При производството на всеки тон алуминий се отделят 280 000 m3 газове. Следователно всеки електролизер, независимо от конструкцията си, е оборудван със система за събиране на газ, която улавя газовете, отделени по време на електролизата, и ги изпраща към системата за очистване на газ. Съвременните системи за „сухо“ пречистване на газ не използват нищо повече от двуалуминиев оксид за улавяне на вредни флуорни съединения. Следователно, преди да се използва за производство на алуминий, алуминиевият оксид всъщност първо участва в пречистването на газове, които са се образували по-рано в процеса на производство на метал. Ето такъв порочен кръг.
Процесът на електролиза на алуминий изисква голяма сумаелектричество, затова е важно да се използват възобновяеми и незамърсяващи източници на тази енергия. Най-често за това се използват водноелектрически централи - те имат достатъчна мощност и нямат емисии в атмосферата. Например в Русия 95% от алуминиевия капацитет се осигурява от водно производство. Въпреки това, има места в света, където производството на въглища все още доминира - по-специално в Китай, то представлява 93% от производството на алуминий. В резултат на това за производството на 1 тон алуминий с помощта на хидрогенерация в атмосферата се отделят малко повече от 4 тона въглероден диоксид, а при използване на производство на въглища - пет пъти повече - 21,6 тона.
 Леярна
Леярна
Разтопеният алуминий в кофи се доставя в леярния цех на завода за алуминий. На този етап металът все още съдържа малко количество примеси от желязо, силиций, мед и други елементи. Но дори части от процента, дължащи се на примеси, могат да променят свойствата на алуминия, така че тук те се отстраняват чрез претопяване в специална пещ при температура от 800 ° C. Полученият чист алуминий се излива в специални форми, в които металът придобива своята твърда форма.
Най-малките алуминиеви блокове се наричат блокове, те имат тегло от 6 до 22,5 кг. След като са получили алуминий на слитъци, потребителите го разтопяват отново и му придават състава и формата, необходими за техните цели.
Най-големите слитъци са 30-тонни паралелепипеди с дължина 11,5 метра. Изработват се в специални форми, навлизащи в земята на около 13 метра. Горещ алуминий се излива в него за два часа - слитъкът "расте" във формата като ледена висулка, само че в обратната посока. В същото време се охлажда с вода и до приключване на изливането вече е готов за по-нататъшно транспортиране. Правоъгълните блокове се наричат слябове (от английски slabs) - те се използват за валцуване на тънки листове и производство алуминиево фолио, кутии за напитки или например каросерии.
Алуминият под формата на цилиндрични блокове достига дължина от 7 метра - те се използват за екструзия, тоест екструзия през отвор с необходимата форма. По този начин се правят повечето алуминиеви продукти.
В леярната алуминият се дава не само различни формино и състав. Факт е, че в чист вид този метал се използва много по-рядко, отколкото под формата на сплави.
Сплавите се получават чрез въвеждане на различни метали (т.нар. легиращи добавки) в алуминия - едни увеличават неговата твърдост, други увеличават плътността му, трети водят до промяна в неговата топлопроводимост и т.н. Като добавки се използват бор, желязо, силиций, магнезий, манган, мед, никел, олово, титан, хром, цинк, цирконий, литий, скандий, сребро и др.В допълнение към тези елементи могат да се използват още дузина легиращи добавки присъстват в алуминиеви сплави като стронций, фосфор и други, което значително увеличава възможния брой сплави. Към днешна дата в промишлеността се използват над 100 вида алуминиеви сплави.
 Нови технологии
Нови технологии
Производителите на алуминий непрекъснато подобряват технологиите си, за да се научат как да произвеждат метал най-добро качествона най-ниска цена и най-малко въздействие върху околната среда. Вече са проектирани и работят електролизатори с токов капацитет 400 и 500 kA, модернизират се електролизатори от минали поколения.
Едно от водещите световни разработки е производството на метал с помощта на инертен анод. Тази уникална революционна технология ще позволи на производителите на алуминий да спрат да използват въглеродни аноди. Инертният анод, най-просто казано, е вечен, но най-важното - когато се използва, в атмосферата не се отделя въглероден диоксид, а най-чистият кислород. Освен това, 1 електролизна вана ще може да произведе толкова кислород, колкото 70 хектара гора. Засега тази технология е секретна и се подлага на индустриални тестове, но кой знае - може би в бъдеще тя ще превърне алуминиевата индустрия в още един бял дроб на нашата планета.
 Рециклиране
Рециклиране
Алуминият има полезно свойство- не губят свойствата си по време на употреба, така че продуктите от него могат да бъдат претопени и рециклирани в нови продукти. Това ви позволява да спестите колосалната енергия, изразходвана за производството на алуминий за първи път.
Според изчисленията на Международния институт за алуминий от 1880 г. в света са произведени почти 1 милиард тона алуминий и три четвърти от това количество все още се използва. Около 35% в сгради и съоръжения, 30% в електрически кабели и оборудване и 30% в транспорт.
Алуминиевите отпадъци се събират по целия свят - в ежедневието това са предимно алуминиеви кутии от напитки. Изчислено е, че 1 кг събрани и рециклирани кутии спестява 8 кг боксит, 4 кг различни флуориди и 14 kWh електроенергия. Освен това ви позволява значително да намалите щетите върху околната среда от непрекъснато нарастващите сметища. Развитието на екологичната отговорност прави идеята за разделно събиране на отпадъци все по-популярна по света.
Алуминият има редица ценни свойства:
1. ниска плътност ρ=2.7g/cm3
2. висока топлопроводимост и електрическа проводимост (по-ниска от среброто и медта)
3. Добра пластичност
4. Достатъчна механична якост
В разтопено състояние (t топи Al=660°C) алуминият е течен и добре запълва кухината на формата, а в твърдо състояние е добре деформиран и лесно се поддава на рязане, запояване и заваряване.
Алуминият се използва най-широко под формата на ковани дуралуминиеви сплави.
Лятите алуминиеви сплави се използват в тракторостроенето и машиностроенето (палети, картери), приборостроенето и хранително-вкусовата промишленост (кутии, колби, чинии).
Алуминиевите руди включват боксити, нефелини, алунити и каолини. Редукцията на алуминий с въглерод е свързана с големи трудности, основната от които е високата температура t=2100°C. В този случай не се образува алуминий, а алуминиев карбид. Следователно алуминият се получава чрез електролиза. Особеността на електролизата е, че тя се извършва не от воден разтвор, а от стопилка. Не е възможно да се изолира алуминий от воден разтвор, т.к водородът с по-висок положителен потенциал от алуминия се отлага първо върху катода. В този случай се образува хидрат на алуминиев оксид и не се отделя чист алуминий. Алуминиевата електролиза включва 4 независими производства:
1. производство на химически чист алуминиев оксид
2. производство на флуорни соли и криолит
3. производство на карбонови блокове и електроди
4. самият процес на електролиза.
Схема на електролизна вана за производство на алуминий: 1 - корпус; 2 - шамот; 3 - въглищен блок; 4 - печка на въглища; 5 - алуминиев оксид; 6 - анод; 7 - тоководеща шина; 8 - окачване (токов проводник); 9 - кора от втвърден електролит; 10 - череп (втвърден електролит); 11 - токов проводник
Алуминият се получава чрез електролиза на алуминиев оксид, разтворен в разтопен електролит, чийто основен компонент е криолитът. В допълнение, някои CaF2, MgF2 и понякога NaCl се добавят към електролита, за да се намали точката на топене. При увеличаване на съдържанието на Al2O3 повече от 10% интензивността на електролита рязко се увеличава, при съдържание под 1,3% нормалният режим на електролиза се нарушава. Електролизна баня или клетка, където се извършва електролиза за получаване на алуминий, има правоъгълна форма в план. Корпус 1 от стоманени листове покрива стените на ваната, а за големи вани е направен с дъно. Вътре има слой от шамот 2 и след това стените са облицовани с въглищни плочи 4, а дъното е оформено от въглищни блокове на огнище 3. Ваната с дълбочина 0,5-0,6 m се пълни с електролит и слой от течен алуминий под него. Въглеродният анод 6 (понякога има няколко) е окачен на стоманени пръти 8, така че долният му край е потопен в електролита, токът се подава към анода през прътите 8 от гуми 7.
Създаване на ефективна химико-технологична система
производство на алуминий
ВЪВЕДЕНИЕ
Металният алуминий е получен за първи път през 1825 г. от Ерстед химичен методредукция на алуминиев хлорид с калиева амалгама. През 1856 г. този метод е подобрен и алуминият започва да се получава чрез редукция на двойна сол. натриев метал. Н.Н. Бекетов през 1865 г. предлага метод за производство на алуминий чрез редуциране на криолита с магнезий. Производството на алуминий по химичен метод продължава до 1890 г., като за 35 години от използването му са получени само около 200 тона алуминий.
През 1886 г. N. Héroux във Франция и C. Hawley в САЩ разработват метод за производство на алуминий чрез електролиза на алуминиева стопилка в криолит, който все още е единственият метод за промишлено производство на алуминий.
Теоретичната основа на производството беше изследването на местни учени ( края на XIX- началото на 20 век) P.P. Федотиев учи и се развива теоретична основаелектролиза на системата "алуминиев оксид - криолит", включително разтворимостта на алуминия в електролита, анодния ефект и други условия на процеса. През 1882-1892г. К.И. Bayer разработва "мокър" метод за производство на алуминиев оксид чрез излугване на руди, а през 1895 г. Д. Н. Пеняков предлага метод за производство на алуминиев оксид от боксит чрез синтероване с натриев сулфат в присъствието на въглища. ИИ Кузнецов и E.I. През 1915 г. Жуковски разработи метод за получаване на алуминиев оксид чрез редукционно топене на нискокачествени алуминиеви руди.
Алуминият е един от най-важните леки цветни метали. По производство и потребление се нарежда на второ място сред всички метали (след желязото) и на първо място сред цветните метали. Поради това в цветната металургия производството на този метал е отделено в отделен специализиран подотрасъл „Алуминиева промишленост“, който включва добив на суровини за алуминиевата промишленост, производство на алуминий, алуминиев оксид и флуорни соли.
Алуминият е твърд, сребристосив метал. Лесно се поддава на коване, валцоване, изтегляне и рязане. Пластичността на алуминия се увеличава с увеличаване на чистотата. Плътност на алуминия, точка на топене 660,2°C, точка на кипене 2520°C. В разтопено състояние той е течен и лесен за леене.
Алуминият има висока топло- и електрическа проводимост, която зависи от неговата чистота. За алуминий висока чистотаелектрическата проводимост е 65% от електрическата проводимост на медта.
Алуминият е химически активен, лесно се окислява от атмосферния кислород, образувайки здрав оксиден повърхностен филм, който причинява високото му устойчивост на корозия. Във фино раздробено състояние при нагряване на въздух се запалва и гори. Алуминият реагира със сяра и халогени. При нагряване образува карбид с въглерод и нитрид с азот. Като амфотерен метал алуминият се разтваря в силни киселини и основи. нормално електроден потенциалалуминият е 1,66 V при pH< 7 и 3,25 при рН>7.
Поради комплекс от ценни свойства (ниска плътност, пластичност, висока топло- и електрическа проводимост, нетоксичност, немагнетизъм, устойчивост на корозия в атмосферата), както и липсата на недостиг на суровини и относително ниска цена. Алуминият в чиста форма и в сплави се използва широко в различни отрасли на техниката и националната икономика.
Алуминият с висока чистота се използва в ядрената енергетика, полупроводниковата електроника, радарите, за производството на отразяващи повърхности на рефлектори и огледала. В металургичната промишленост алуминият се използва като редуциращ агент при производството на редица метали, деоксидирането на стомана и за заваряване на части.
Алуминият се използва главно за производство на алуминиеви сплави. Алуминиеви покрития се нанасят върху стоманени продукти, за да се подобри тяхната устойчивост на корозия.
Алуминий - под формата на прах и гранули - дезоксидатор на чугун и стомана, редуциращ агент на оксиди при производството на метали и сплави чрез алуминотермия, компонент на твърди ракетни горива, пиротехнически състави. Алуминиев прах и паста - пигменти на бои и лакове; прахът се използва и като разпенващ агент при производството на клетъчен бетон.
Приблизително 24% се изразходват в строителството и транспорта чист алуминийи неговите сплави, в производството на опаковъчни материали и консервни кутии - около 17%, в електротехниката - около 10%, в производството на потребителски стоки - около 8%.
1. ОБОСНОВКА НА СЪЗДАВАНЕТО НА ЕФЕКТИВНА CTS
1.1 СУРОВИНИ ЗА ПРОИЗВОДСТВО НА АЛУМИНИЙ
Алуминият е съставна част на много метали, но само боксити, нефелини, алунити и каолини се използват като алуминиеви руди. Те се различават по състава и концентрацията на алуминий. Най-важната алуминиева руда е бокситът, съдържащ хидратиран алуминиев оксид. В зависимост от степента на хидратация алуминиевият компонент в бокситите може да бъде под формата на диаспора (или ) или под формата на хидроаргелит (или ). В допълнение към алуминиевия оксид, бокситът съдържа силициев оксид и различни връзкижелязо, калций и магнезий. Основната характеристика на боксита, от която зависи изборът на метода на тяхната обработка, е съотношението на съдържанието на алуминиев оксид в тях към съдържанието на силициев оксид. За боксити, използвани в алуминиевата промишленост, модулът трябва да бъде най-малко 2,6; за боксит със средно качество е 5-7, което съответства на съдържанието на алуминиев оксид 46-48%.
Нефелините са сложна тройна сол на състава и влизат като съставна част в апатито-нефелиновата руда, която съдържа освен нефелин и апатит ![]() . За производството на алуминий се използва нефелинов кондензат със съдържание на алуминиев оксид 20-30%.
. За производството на алуминий се използва нефелинов кондензат със съдържание на алуминиев оксид 20-30%.
Алунитите са двойноосновни сулфатни соли с алуминиев и калиев състав. Съдържанието на алуминиев оксид в алунитите не надвишава 20%.
1.2 ОБЩА СХЕМА НА ПРОИЗВОДСТВОТО НА АЛУМИНИЙ
Технология на производство метал алуминийот руди е много сложен и се състои от четири индустрии, свързани помежду си с технологична верига и производни продукти. Включва:
Производство на алуминий;
Производство на флуорни соли и криолит;
Производство на въглищни продукти (електроди и облицовъчни блокове);
Производство на електролитен алуминий.
Основните индустрии, които изграждат технологичната верига
Алуминиева руда Алуминий,
са производството на алуминий и алуминий. Те обикновено са географски разделени. Поради високата енергийна интензивност на процеса на електролитна редукция на алуминий, алуминиевите топилни предприятия са разположени в райони с евтина водноелектрическа енергия. Производството на алуминиев оксид, напротив, е базирано на местата, където се добиват алуминиеви руди, за да се спестят разходите за транспортиране на суровини.
Производството на флуоридни соли и криолит има за цел да получи разтворител за алуминиев оксид и добавки, които намаляват точката на топене на електролита.
Организирането на отделно производство на въглищни продукти се дължи на факта, че в процеса на електролиза въглеродните аноди и облицовката на електролизарите се изразходват и изискват непрекъснато попълване.

Ориз. 4.1. Принципна схема на производството на алуминий.
1.3 ПРОИЗВОДСТВО НА АЛУМИНИЕВ оксид
Изходният материал за електролитното производство на алуминий е чистият алуминиев оксид - алуминиев оксид. За да се изолира алуминиевият оксид от алуминиеви руди, той се превръща в разтворима сол (натриев алуминат), която се отделя от останалите компоненти на руда, алуминиевият хидроксид се утаява от неговия разтвор и алуминиевият оксид се получава чрез калциниране на последния.
Методът за извличане на алуминиев оксид от рудата зависи от нейния състав. Тези методи се делят на химико-термични (пирометалургични), киселинни и алкални (хидрометалургични). Пирометалургичните методи включват метода на синтероване; към хидрометалургичните методи - алкалният метод на Байер.
МЕТОДЪТ НА БАЙЕР (мокър метод, метод на излугване) е най-разпространеният метод за производство на алуминиев оксид. Методът се основава на обратим процес на взаимодействие на хидратиран двуалуминиев оксид с воден разтворнатриев хидроксид до образуване на натриев алуминат. Методът се използва за изолиране на двуалуминиев оксид от боксит с ниско (по-малко от 5%) съдържание на силициев оксид. При по-високо съдържание методът става икономически неизгоден поради високата консумация на скъпи основи за взаимодействие със силициев оксид.
МЕТОД ЗА СПИТОЧАНЕ. Основава се на процеса на образуване на натриеви алуминати в резултат на взаимодействие при висока температура на алуминиев оксид с метални карбонати, последвано от излугване на алуминати с вода и тяхното разлагане с въглероден оксид (IV).
Процесът на производство на алуминиев оксид чрез синтероване е универсален и подходящ за обработка на всички видове алуминиеви суровини. На практика се използва за нефелини и боксити с високо (над 5%) съдържание на силициев оксид.
При разглеждането на тези методи за производство на алуминиев оксид е избран методът на Байер, тъй като той е основният и най-разпространен метод за производство на алуминиев оксид.
Процесът на извличане на алуминиев оксид по метода на Байер се състои от следните операции:
1. Натрошаване на боксит и мокро смилане в среда на рециклиран алкален разтвор с образуване на пулп.
2. Излугване на алуминиев оксид с циркулиращ разтвор на натриев хидроксид съгласно реакциите:
(диаспора)
(хидроаргелит)
В същото време протича реакцията на образуване на натриев силикат, за която се изразходва част от реакционната основа:
Излужването е хетерогенен процес на насищане на воден алкален разтвор с алуминиев оксид, чиято скорост зависи от дисперсността на твърдата фаза, концентрацията на разтвора на натриев хидроксид и температурата. Режимът на процеса на излугване се определя от степента на хидратация на алуминиевия оксид в боксита: диаспорите се излугват при 240°C и p=3MPa; хидроаргелит - при 100°C и p=0,1 MPa. Степента на извличане на алуминиевия оксид достига 0,92% за три часа и след това практически не се променя; концентрацията на натриев хидроксид в алкалния разтвор намалява.
3. Разреждане-самопречистване, когато към пулпата се добави вода за образуване на неразтворим хидратиран натриев алуминат:
В резултат на тази реакция част от алуминиевия компонент се губи и повече, колкото по-високо е съдържанието на силициев оксид в боксита. Утайката от алумосиликат, оцветена с железен (III) оксид в червено-кафяв цвят, се нарича червена кал.
4. Филтриране на разтвор на натриев алуминат, отделяне и промиване на червена кал.
5. Разлагане на разтвор на натриев алуминат с понижаване на температурата и интензивно смесване на целулозата:
Разлагането е спонтанен продължаващ процес на хидролиза на натриев алуминат. Ускорява се чрез въвеждането на кристален алуминиев хидроксид, който едновременно насърчава образуването на големи кристали от алуминиев хидроксид поради създаването на кристализационни центрове в системата.
6. Сгъстяване на пулпа, последвано от отделяне на алуминиев хидроксид върху вакуум филтър и класифициране на получения продукт с изолиране на основната фракция.
7. Изпаряване на матерната луга за образуване на рециклирана луга и нейното подсилване с натриев хидроксид.
8. Каустификация на образувания натриев карбонат с калциев хидроксид и връщане на образувания бял кал в технологичния процес:
9. Калциниране на алуминиев хидроксид при 1200°C:
Полученият по метода на Байер алуминиев оксид е смес от - модификация (корунд) и - модификация на алуминиев оксид. Техническият продукт е бяло кристално вещество и се предлага в няколко различни степени на чистота. Най-вредните примеси в двуалуминиевия оксид са силициевият оксид, железният оксид (III) и титановият оксид (IV).
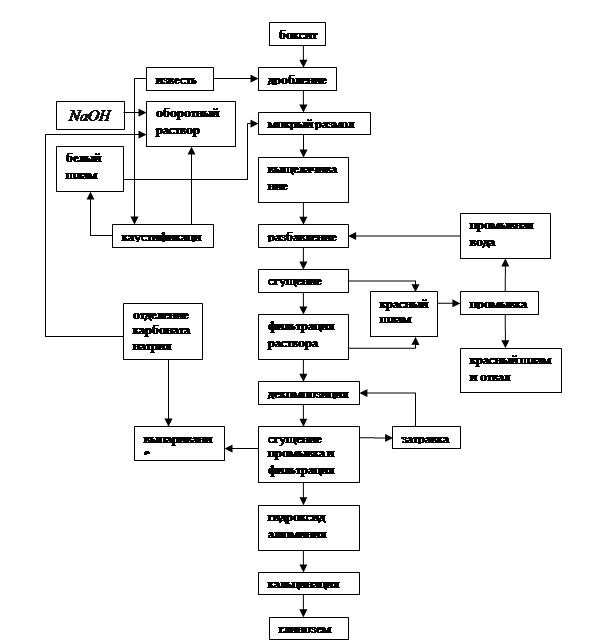
Ориз. 4.2. Схематична диаграма на производството на алуминиев оксид по метода на Байер
От принципната схема на процеса следва, че методът на излугване на Bayer използва затворен технологичен цикъл на основа. Алкалът, изразходван за излугване на алуминиев оксид от боксит, се регенерира на етапите на разлагане и каустика и се връща в процеса за обработка на нови порции боксит. По този начин методът на Байер прилага принципа за организиране на нискоотпадъчно производство.
1.4 ЕЛЕКТРОЛИТНО ПРОИЗВОДСТВО НА АЛУМИНИЙ
Единственият промишлен метод за получаване на метален алуминий от неговия оксид е електролизата на неговата стопилка.
Точката на топене на чистия двуалуминиев оксид в неговата α-модификация, която е стабилна над 900°C, е 2053°C. Електролизата на неговата стопилка е свързана с много висока консумация на енергия за топене и поддържане на висока температура на банята и води до ниска енергийна ефективност. Следователно при производството на алуминий не се използва чист алуминиев оксид, а система, състояща се от алуминиев оксид и криолит, т.е. стопилка от криолит-алуминий.
Криолитът се топи при 1100°C. Образува се с алуминиев оксид, когато съдържанието на последния е около 15% тегл. евтектика с точка на топене 938°C. По-нататъшното увеличаване на съдържанието на алуминиев оксид в стопилката води до рязко повишаване на температурата на топене на системата.
За да се намали температурата на топене на електролита, да се увеличи неговата електропроводимост, да се подобри омокряемостта на анода, в стопилката се въвеждат добавки от алуминий, магнезий, литий и калциев флуорид. Промишленият електролит има състав:
В резултат на дисоциацията на основните компоненти на системата
както и добавки от флуоридни соли, стопеният електролит е сложна многокомпонентна система, съдържаща йони:
Таблица 4.1. Първични процеси при електролиза
Следователно, по време на електролизата на стопилка от криолит-алуминиев оксид се отделят йони.
Вторичните процеси при електролизата на криолитно-алуминиева стопилка протичат както в анодното, така и в катодното пространство.
В анодното пространство при температурата на електролиза протича непрекъснато окисление на въглеродните аноди с образуването на смес от въглероден оксид (II) и въглероден оксид (IV):
Обобщавайки реакциите на първичните и вторичните процеси, получаваме общите уравнения за реакциите на електролиза:
![]()
Основният апарат в процеса електролитно производствоалуминият е електролизатор или алуминиева вана.
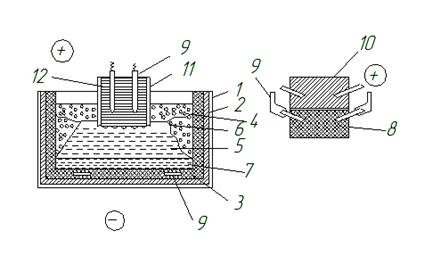
Ориз. 4.3. Схема на електролитната клетка: а - баня със самоизпичащи се аноди, б - блок с предварително изпечен аноден алуминий, 8 работен блок на изпечения електрод, 9 токопровода, 10 подреждащ се блок, 11 корпус на анодна маса, 12 анодна маса .
Електролизерът се състои от катодно и анодно устройство. Катодното устройство е правоъгълен метален корпус с огнеупорна изолация, облицован отвътре с въглищни плочи и блокове. Долните блокове са същевременно токопроводи за разтопен алуминий, който играе ролята на катод. Електролизерът е оборудван със система за рекуперация на газ и доизгаряне на въглероден окис (II), устройство за непрекъснато подаване на алуминиев оксид и система за изпомпване на метален алуминий.
Анодното устройство се състои от въглеродни аноди, частично потопени в разтопения електролит, и токопроводи, пресовани в тях. Използват се непрекъснати аноди с различни конструкции. В съвременните електролизери се използват два вида непрекъснати аноди: самозапичащи се и предварително изпечени. Самозапичащият се анод се състои от алуминиев корпус, в който е поставена брикетирана анодна маса с пресовани в нея токопроводи.
В съвременните електролизатори с висока мощност се използват предварително изпечени аноди, които се състоят от блокове, изградени отгоре, докато се изгарят. Токопроводите се притискат в готовите блокове отстрани.
Поради разликата в плътността течният алуминий се отделя от криолитно-алуминиевата стопилка и се събира на дъното на ваната. В процеса на електролиза, в резултат на охлаждане на ваната с външен въздух, върху повърхността на стопилката се образува твърд електролитен слой (олово), който изолира ваната и намалява консумацията на енергия. За извличане на разтопен алуминий от ваната се използват вакуумни черпаци или сифони, чиято смукателна тръба се въвежда в течен алуминий през слоя на черепа.
Двуалуминиевият оксид се подава непрекъснато в електролизера с помощта на пневматично прътово устройство, което позволява пробиване на кората на черепа и дозиране на алуминиевия оксид.
Системата за възстановяване на газ на електролизера е проектирана да събира газовете, отделени по време на електролизата, и да ги отвежда в системата за почистване на газ.
2. ПОЧИСТВАНЕ И РАФИНИРАНЕ НА АЛУМИНИЙ
Примесите значително влошават механичните, електрическите и леярските свойства на алуминия и намаляват неговата устойчивост на корозия. За отстраняване на механични примеси и разтворени газове алуминият, изпомпван от ваната, се хлорира във вакуумни кофи. В същото време водородът и някои метали се хлорират, а получените хлориди и механични примеси изплуват на повърхността на метала и се отстраняват:
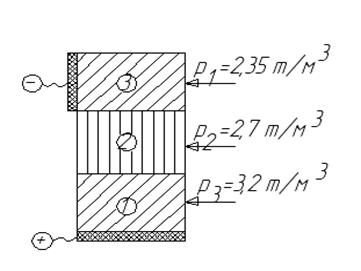
Ориз. 4.4. Схема на електролитно рафиниране на алуминий: 1 слой рафиниран (горен слой) - пречистен алуминий, съдържащ мед, 2 слой електролит, 3 слой чист алуминий.
След хлорирането алуминият се съхранява в електрически пещи за отстраняване на остатъчните примеси и хомогенизиране на състава, след което се отлива в блокове. След такова пречистване се получава алуминий клас А85, който съдържа най-малко 99,85% от метала. За да се получи алуминий с висока и специална чистота, той се подлага на допълнително рафиниране. В промишлеността се използват два метода за рафиниране: електролитно и с използване на алуминиеви подсъединения.
Електролитният трислоен метод на рафиниране се основава на процеса на анодно окисление и последваща катодна редукция на алуминий. Анодът на електролизера е рафиниран алуминий, съдържащ да увеличи
Между катода и анода се намира разтопен електролит, състоящ се от смес от бариев и натриев хлорид и алуминиев и натриев флуорид.По време на процеса на рафиниране алуминият се разтваря върху анода:
неговите йони, поради разликата в плътността между слоевете замърсен алуминий и електролита, преминават през слоя на последния и се редуцират на катода:
В същото време примесите с висок потенциал остават в слоя на рафинирания метал и се натрупват в слоя електролит. Тъй като примесите се натрупват, анодната сплав и електролитът периодично се сменят. Алуминият, получен чрез този метод на рафиниране, е с чистота 99,99%.
Рафинирането с подсъединения се основава на сублимация на силно летливи едновалентни алуминиеви подсъединения, образувани по време на високотемпературна обработка на рафиниран алуминий с алуминиев (III) хлорид. Примесите не се дестилират и остават в остатъка от рафинирането.
Чистотата на алуминия, получен чрез суб-съединения, е 99,9995%.
Алуминий със свръхвисока чистота (99,9999%) може да бъде получен чрез зоново топене.
3. ОПРЕДЕЛЯНЕ НА ТЕХНОЛОГИЧНАТА ТОПОЛОГИЯ НА КТС
Определяне на видовете комуникация между устройствата в технологична схемапроизводство на алуминиев оксид по метода на Байер.
В тази схема се използва главно серийният тип свързване на устройства.
Смесителят за целулоза, нагревателят за целулоза, нагревателните автоклави и реакционните автоклави са свързани последователно, така че бокситната пулпа преминава през тези апарати последователно, където се раздробява, мокро смила и излугва. Реакционните автоклави са свързани към сепаратора за пара и течност и към разредителя чрез последователно байпасна връзка. Парният сепаратор е свързан към нагревателя обратна връзка, тъй като парата, образувана в сепаратора, се връща към нагревателя, за да го загрее. Пулпата от сепаратора се подава последователно към разредителя, след това към сгъстителя на утайките и след това към отделянето на червена кал във вакуумния филтър. Вакуумният филтър е свързан паралелно с устройство за измиване на утайки и разлагател, тъй като утайката, отделена на филтъра, се изпраща за промиване, а разтворът на натриев алуминат влиза в разлагателя, където се смесва с въздух. Освен това разлагателят, сепараторът на алуминиев оксид, бункерът, тръбната пещ и тръбният охладител са свързани последователно.
Тъй като във веригата има технологична връзка с обратна връзка, веригата е затворена.
При метода на излугване на Байер се осъществява затворен технологичен цикъл за алкали. В резултат на това се прилага принципът за организиране на нискоотпадъчно производство.
4. УСТАНОВЯВАНЕ НА ТЕХНОЛОГИЧНИ И СТРУКТУРНИ ПАРАМЕТРИ НА CTS, ТЕХНИЧЕСКИ ПАРАМЕТРИ НА РЕЖИМА И ПОТОЦИ
Реакционният автоклав за излугване на боксит е вертикално разположен заварен съд с диаметър до 2,5 м и височина 14–18 м. Степента на разлагане на суровините е до 0,9 фракции от единица.
Най-модерният въздушно смесен декомпозитор е стоманен резервоар с конично дъно с диаметър 9 m и височина до 35 m.
Таблица 4.2. Разходни коефициенти за 1 тон алуминиев оксид.
Таблица 4.3. Характеристики на клетки за производство на алуминий с непрекъснати предварително изпечени аноди.
Производителността на такива електролизатори варира от 0,5 до 1,2 тона алуминий на ден и може да се изчисли по формулата:
![]()
където P е производителността на клетката, t/ден;
J - сила на тока, A;
Време на електролиза, h;
Текущ изход, дял
Таблица 4.4. Разходни съотношения за 1 тон алуминий.
5. ИЗОБРАЖЕНИЕ НА ГРАФИЧНИ МОДЕЛИ НА XTS
Химична схема
Функционална схема

Структурна схема
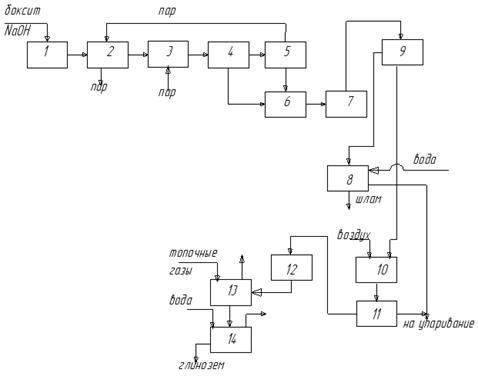
1 - миксер за целулоза
2 - нагревател за целулоза
3 - нагревателни автоклави
4 - реакционни автоклави
5 - сепаратор на пара и течност
6 - разредител
7 - сгъстител на утайки
8 - миене на утайки
9 - вакуумен филтър
11 - алуминиев сепаратор
12 - бункер
13 - тръбна пещ
14 - тръбен охладител
Технологична система
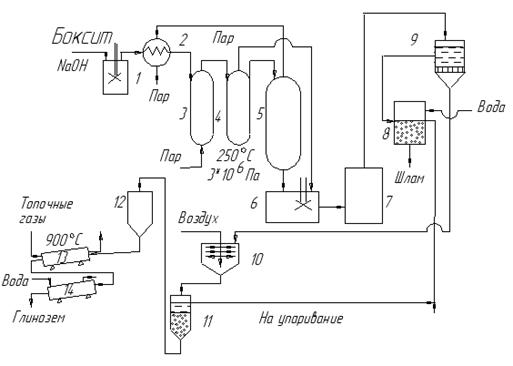
1 смесител за целулоза,
2-пулп нагревател,
3-нагревателни автоклави (два),
4-реакционни автоклави (6),
5-парен и течен сепаратор,
6-тънък,
7-сгъстител на утайки,
8-миячка,
9-вакуумен филтър,
11-алуминиев сепаратор,
12-бункер,
13-тръбна пещ,
14-тръбен хладилник.
Технологичният процес за производство на алуминиев оксид по метода на Байер е организиран по следния начин. Бокситната пулпа от смесителя 1 се подава в нагревателя 2, загрята от пара от сепаратора 5. От нагревателя пулпата влиза в батерията на нагревателните автоклави 3 и след това в батерията на реакционните автоклави 4, където процесът на излугване отнема място, откъдето се изпраща в сепаратора 5. В сепаратора налягането намалява от 3 MPa до атмосферно, в резултат на което пулпата кипи и получената пара се изпраща към нагревателя 2. След това пулпата, състоящ се от алкален разтвор на натриев алуминат и червена кал, се разрежда в разредител 6 и влиза в сгъстителя на пулпа 7 и по-нататък за отделяне на червената кал към филтъра 9. Отделената утайка се промива с вода в шайбата 8 и разтворът на натриев алуминат влиза в разлагащия апарат 10, където се смесва с барботиращ въздух. От разлагащия апарат хидратната пулпа, състояща се от кристали на алуминиев хидроксид и матерната луга, се изпраща в кристалния сепаратор 11, където кристалите се отделят от матерната луга и след преминаване през бункера 12 влизат в 13 тръбна пещ за калциниране , след което се охлаждат в тръбен охладител 14. Отделената матерна луга се свързва с разтвора от утайката 8 и се изпраща за изпаряване.
Основни апарати: реакционен автоклав и декомпозитор.
Алуминият е един от най-разпространените елементи в природата:
Поради високата химическа активност на алуминия в природата,
чайове само в подвързана форма. Броят на минералите, съдържащи алуминий,
много големи: според академик А. Е. Ферсман има
се оказват около 250.
По-долу са най-важните от тези минерали, като се посочва съдържанието им
в тях Al2O3, %:
Корунд Al2O3 100
Диаспора, бемит Al2O3 H2O 85.0
Шпинел Al2O3 MgO 71.0
Гибзит (хидраргилит) Al2O3 3H2O 65.4
Кианит, андалузит, силиманит Al2O3 SiO2 63.0
Каолинит Al2O3 2SiO2 2H2O 39.5
Серицит, мусковит K2O 3Al2O3 6SiO2 2H2O 38,4
Алунит K 2 S0 4 Al 2 (S04) 3 4Al(OH) 3 37,0
Анортит CaO Al 2 O 3 2SiO 2 36.7
Нефелин (Na, K) 2O Al 2 O 3 2SiO 2 32,3÷35,9
Левцит K 2 O Al 2 O 3 4SiO 2 23.5
Албит Na 2 O Al 2 O 3 6SiO 2 19.3
Ортоклаз K 2 O AlO 3 6SiO 2 18.4
алумосиликати: фелдшпати (ортоклаз, албит), нефелин, минерали
силиманитни групи, левцит и др. Тези алумосиликати имат първичен
произход и са основният компонент на много вулканични
род. Химичните съединения на оксида също са от първичен произход.
алуминий с оксиди на други метали (шпинели) и корунд. Прозрачни времена
Разновидностите на корунда, оцветени с оксиди на други метали или безцветни, са скъпоценни камъни (рубин, сапфир, левкосапфир).
Под въздействието на температурни промени, киселинни и алкални разтвори
канавка, въглеродният диоксид е разрушаването на скали от първичен произход
жив. В резултат на такова унищожение множество вторични
естествени скали, които се характеризират с по-високо съдържание на окси-
да алуминий. В състава на тези вторични скали алуминият е под формата
хидроксиди (боксити), каолинит (глини, каолини, шисти), алуминий
нита (алунитни скали). От алуминиева руда, като правило, първо се получава алуминиев оксид (алуминиев оксид). Не всички скали, съдържащи алуминий, могат да се използват за производство на алуминий.
При оценката на качеството на алуминиевата руда се вземат предвид редица фактори:
химичният и минералогичен състав на рудата, възможността за извличане на алуминиев оксид от нея по известни методи, както и условията на възникване на рудата, отдалечеността на находището от комуникационните линии, наличието на източници на гориво, вода, и много други. Понастоящем като алуминиеви руди се използват боксити, нефелинови и алунитни скали, каолини и кианитни скали. Възможни суровини за получаване на алуминиев оксид са също серицит, пепел с високо съдържание на алуминий, образувана при изгарянето на въглища, металургична шлака, отпадъци от обогатяване на въглища.
Бокситът е най-важната алуминиева руда. Делът на бокситите е
голяма част от световното производство на алуминий. Алуминиевата промишленост на чужди страни почти изцяло работи само на боксити.
В нашата страна, наред с боксита за производство на алуминиев оксид, до голяма степен
В големи количества се използват нефелинови и алунитни руди.
Бокситът е сложна скала, в която има алуминий
среща се под формата на хидроксиди - диаспор и бемит (монохидратни оксиди), гибсит
или хидраргилит (трихидратен оксид). Заедно с хидроксидите, част от алуминия
миниумът може да се намери в бокситите под формата на корунд, каолинит и други минерали. В допълнение, съставът на боксит под формата на различни химични съединениявключва желязо, силиций, титан и други елементи. Желязото може да се намери в бокситите под формата на хематит Fe2O3, гьотит 2Fe 2 0 3 .H 2 O, сидерит FeCO 3, пирит FeS 2, шамозит 4FeO Al 2 O 3 3SiO 2 4H 2 O и редица други съединения. Силицият присъства в бокситите под формата на кварц, опал, халцедон (различни модификации).
катион SiO2), каолинит, шамозит и някои други минерали. Основен
титанови минерали в боксити: анатаз и рутил TiO 2 и илменит FeO·TiO 2 . AT
бокситите могат също да съдържат калциеви карбонати CaCO3 и магнезий
MgCO3, органични съединения, съединения на сярата, фосфора, хрома и др
елементи. Сярата присъства в бокситите главно под формата на пирит и неговото количество
лоидна разновидност - мелниковит, фосфор - под формата на апатит
3Ca 3 (PO 4) 2 CaF 2. В малки количества бокситите често съдържат съединения
комбинации от редки елементи: ванадий, галий, цирконий, ниобий и др.
състав на боксити под формата на различни съединения, намерени 42 химически
елемент. Химическият състав на бокситите, както и техните физични свойства, са много различни. Те съдържат Al 2 O 3 35 ÷ 70%, SiO 2 - от десети до 25%, Fe 2 O 3 2 ÷ 40%, TiO 2 - от следи до 11%. Съдържанието на редица елементи в бокситите се измерва в стотни и дори хилядни от процента, например ванадий 0,025÷0,15%, галий 0,001÷0,007%.
На външен вид бокситите често приличат на глина, цветът им е от бял до тъмночервен (най-често червен с различни нюанси). Структурата на бокситите може да бъде плътна и пореста. Плътността им е от 1,2 до 3,5 g/cm3, твърдостта е от 2 до 7 (по скалата на Моос).
Има каменисти, рохкави и глинести боксити, които се отличават с
Xia не само с физичните си свойства, но и с химически и минерални
химичен състав. Каменистите боксити обикновено са с високо съдържание на желязо; съдържанието на силициев оксид в тях обикновено е ниско. Разхлабена кутия
Различавате се от каменистите предимно по по-високото съдържание на каолинит с намалено количество алуминиев хидроксид. Глинените боксити се характеризират с високо съдържание на каолинит и ниско съдържание на железни оксиди.
В зависимост от минералогичната форма на хидроксидите
алуминият се намира в бокситите, те се делят на диаспор, бемит,
гибзитови и смесени. Смесените боксити съдържат едновременно две форми на алуминиев хидроксид (диаспор-бемит, гибзит-бомит
боксити). Съдържанието на боксити оказва най-голямо влияние върху качеството на бокситите.
оксиди на алуминий и силиций. Съотношението на съдържанието на Al2O3 в боксит към ко-
съдържащ SiO2 (по маса) се нарича кремъчен модул на боксит. как
колкото по-голям е модулът на кремъка, толкова по-високо е качеството на боксита.
Съгласно GOST 972−84, в зависимост от вида на потреблението, боксит
разделени на 7 марки:
ЕВ-1 и ЕВ-2 - Производство на електрокорунд
ЦБ-1 – Производство на алуминиев цимент
CB-2 – Производство на цимент
OB – Производство на огнеупори
GB - Производство на алуминий
MB - Мартеновско производство на стомана
Изчерпателен показател за качеството на боксита, преработен в глина
zem (клас GB), зависи от технологичната схема на преработката му и от съдържанието в него на A12O3, SiO2 и други компоненти, които влияят върху ефективността на преработката. Повечето отсветовните запаси от боксит са концентрирани в остатъчни
депозити. Това са основните находища на Африка, полуостров Хиндустан, Централна и Южна Америка и Австралия.
Проучените запаси от боксит у нас са сравнително малки и
качеството им като цяло е ниско. Освен това част от находищата се намират в райони, които са трудни за разработка и са неподходящи за по-ефективен открит добив.
Най-важното е Североуралското бокситно находище в
Свердловска област. Редица бокситни находища на бемит-диаспор
тип отворен на Южен Уралв района на Челябинск и Башкирската АССР.
Южноуралските боксити се характеризират с високо съдържание на
неземни и въглероден окис (IV), както и висока твърдост. Те също се добиват под земята. Добитите боксити съдържат средно, % (според
маса): Al2O3 50÷53; SiO2 5÷10 и Fe2О3 21÷22. В Северен Казахстан (в района на Тургайското корито) са известни редица находища на гиббзитни боксити: Амангелдинское, Краснооктябрское, Белинское, Аятское и др.
бокситите са предимно от тип средно желязо, имат относително високо съдържание на каолинит и нисък кремъчен модул. Тургайските боксити се добиват в открит рудник. Основната маса на боксита съдържа средно 42÷44% Al2O3, 9÷11% SiO2 и 16÷20% Fe2O3 с кремъчен модул 4÷5.
Тихвинското находище на гибсайт се намира в Ленинградска област.
боемит боксит. Химичен състав и физични свойства на Тихвин
бокситите са много разнообразни, но като цяло качеството им е ниско. В настоящето
За момента запасите от Тихвински боксити са до голяма степен изчерпани. В Архангел
област в района на Северна Онега, разработването на находището е в ход
гибзит-бьомитни боксити. Северно Онежките боксити се характеризират с
лез (6÷9%), но имат нисък среден кремъчен модул – около три. Северноонежките боксити, за разлика от бокситите от други находища, съдържат относително високо количество хром (0,5÷0,8%. Сr2O3); силициев диоксид (16÷20%) се намира в боксита главно под формата на каолинит. Бокситът се добива в открит рудник. Чуждестранната алуминиева промишленост работи главно върху висококачествени боксити от типа на гибсита. Само в определени страни
(Франция, Гърция и др.) има заводи, работещи с боксити от бемит.
Големи находища на боксит се намират в Австралия, в Африка
континент (Гвинея, Гана), в страните от Южна Америка (Суринам, Гвиана,
Ямайка, Бразилия). Азия има големи запаси от боксит
в Индия, Индонезия, Китай, Малайзия. На европейския континент големи
находища на боксит има във Франция, Унгария, Югославия и Гърция.
ция. Европейски страни като Германия, Норвегия, Швеция и Англия имат
със сравнително развита алуминиева индустрия, собствен
Те почти нямат находища на боксити и използват вносни суровини (алуминиев оксид и боксити). САЩ значителна част от обработката
Моите боксити се внасят от други страни. Канада, която има развит алуминий
индустрия, няма собствени боксити и изнася суровини
(боксит и алуминиев оксид) от много страни в Америка и Африка.
У нас се преработват и известни количества боксит,
идващи от чужди държави: Гвинея, Югославия, Гърция. Правя-
Гибзитовият боксит от Гвинея има следния състав, % (по маса):
Al 2 O 3 45÷48; Fe 2 O 3 20÷25; SiO 2 1,5÷2,5.
Наред с бокситите у нас, за производството на алуминиев оксид,
наричат нефелини и алунити. Включване в производството на нови видове суровини
позволи не само да се разшири суровинната база на алуминиевата промишленост
sti, но и по-рационално разполагане на алуминиевата индустрия.
Нефелините са част от нефелиновите сиенити, уртити и др
род. Резервати от уртити са открити на Колския полуостров - в Хи-
бобови планини. Основните компоненти на уртитите от Кола са апатитите
3Ca 3 (PO 4) 2 CaF 2 и нефелин (Na, K) 2O Al 2 O 3 2SiO 2. Съдържание на апатит в рудата
средно 43%, нефелин 38%, останалото - пироксени, сфен, ти-
таномагнетит, фелдшпат и други минерали. В естествения нефелин, мол-
съотношението на SiO 2 към Al 2 O 3 е малко повече от 2; състав на нефелин
се изразява със следната формула (Na,K)2O Al 2 O 3 (2+n) SiO 2, където n = 0÷0,5.
Рудата се подлага на флотационно обогатяване. Това води до a
титанов концентрат, който се използва за производството на фосфор
трици и нефелинови отпадъци. Опашките отново се подлагат на флотация (повторно
почистване) и получаване на нефелинов концентрат - суровина за производството на глина
Нефелиновият концентрат е натрошен материал, в
в които от 20 до 40% от фракцията е под 0,085 mm. Съдържанието на нефелин в нефе-
линия концентрат достига 95%.
Съгласно спецификации (MRTU 6-12-54-80) нефелин концентрат
17,5% (Na20+K20). Средно аритметично химичен съставследващ концентрат, %
(тегловни): Al 2 O 3 28,5; SiO2 44; Fe2O3 3,5; (Na 2 O + K 2 O) 18.
Уртитното находище Кия-Шалтирское е открито в района на Кемерово.
lusty, които се характеризират с високо качество и за разлика от други известни нефелинови руди могат да се обработват без предварително обогатяване.
Съгласно спецификациите (TU 48-0113−81), нефелиновата руда на това находище трябва да съдържа най-малко 26,5% Al 2 O 3 и 12,4% (Na 2 O + K 2 O по отношение на Na 2 O). Рудата е светлосива, средно- и едрозърнеста скала, съдържаща средно 85% нефелин. По отношение на съдържанието на алуминиев оксид рудата Kiyashaltyr се различава малко от концентрата на Кола нефелин, но съдържа по-малко алкали и повече железен оксид.
Заедно с двуалуминиевия оксид при преработката на нефелинови руди и концентрати
вземете сода и поташ. В допълнение, отпадъците от производството на алуминиев оксид - утайки от белит се използват за производството на цимент. Следователно нефелиновите руди са сложни суровини, което прави преработката им икономически целесъобразна, въпреки ниското съдържание на алуминиев оксид в сравнение с боксита. Алунитите са част от алунитни скали, чиито находища се намират в Азербайджан, Казахстан, Узбекистан и Украйна. Минералогично, алунитът е основният сулфат на алуминий и калий (или натрий) K 2 SO 4 ·A1 2 (SO 4) 3 · 4A1 (OH) 3.
Има натриеви и калиеви разновидности на алунит: натрий - с молекулно съотношение Na 2 O: K 2 O \u003d (1,76 ÷ 6): 1, калий - Na 2 O: K 2 O \u003d 1: 2. Промишлените находища обикновено съдържат изоморфна смес от тях
две разновидности с преобладаване на калий.
Включени са минерали от групата на силиманита (кианит, силиманит, андалузит).
в състава на редица скали, чиито отлагания са открити на Кол-
полуостров, в Сибир, в Урал. Най-голямото от тях е находището на кианит на Колския полуостров. Средното съдържание на кианит в рудата на това находище е 30÷40%. По време на обогатяването на рудата чрез флотация е изолиран концентрат, съдържащ до 60% Al 2 O 3. Кианитният концентрат е добра суровина за производството на алуминиево-силициеви сплави и огнеупори с високо съдържание на алуминий.
Глините и каолините са най-често срещаните алуминиеви оксиди
породи. Страната разполага с редица големи находища с високо качество
глини и каолини в Урал и Сибир. Алуминият се намира в глините под формата
воден алумосиликат - каолинит. Чисти глини с високо съдържание
се наричат каолинит и съответно ниско съдържание на примеси
каолини. Качеството на каолините като алуминийсъдържащи суровини се определя от
etsya, на първо място, съдържанието на каолинит и възможността за тяхното обогатяване.
Понастоящем каолините се използват за производство на силиций-алуминий
сплав - силикоалуминий чрез директна редукция; те също са възможни суровини за производството на алуминиев оксид чрез киселинни процеси и процеси на синтероване.
Sericite Ka 2 O 3Al 2 O 3 6SiO 2 2H 2 O - воден калиев алумосиликат съдържа
живее около 10% K 2 O и над 39% Al 2 O 3. По време на флотационното обогатяване не-
от които медни руди се получават хвостове с високо съдържание на серицит.
Повторната флотация на хвоста дава възможност да се изолира концентрат, състоящ се от почти
от чист серицит. Този концентрат може да се използва за получаване
алуминиев оксид, основи и цимент.
Суровината за производство на алуминиев оксид може да бъде въглищна пепел,
отпадъци от обогатяване черни въглищаи алуминисти шлаки, образуващи -
Xia по време на редукционното топене на някои железни руди. Съдържание на Al 2 O 3
в пепелта от изгарянето на някои въглища, както и в отпадъците от обогатяване на въглища
достига 30–40%, останалото е главно силициев диоксид.


