Stosunkowo niedawno (nieco ponad sto lat temu) aluminium było uważane za jeden z najdroższych metali. A było to spowodowane nie małymi zapasami surowców, ale złożonym procesem produkcji tego metalu. Dzisiaj aluminium stało się jednym z najtańszych metali, zarówno dzięki dużym zasobom surowcowym, jak i ulepszonej produkcji. Zajmuje wiodącą pozycję w produkcji metali nieżelaznych i znajduje szerokie zastosowanie w wielu branżach m.in czysta forma oraz w postaci stopów. Jak dziś pozyskuje się aluminium? Rozwiążmy to.
Z czego wykonane jest aluminium?
W zależności od surowców użytych do uzyskania tego metalu aluminium dzieli się na pierwotne i wtórne.
Do produkcji aluminium pierwotnego stosuje się rudy mineralne zawierające tlenek glinu: boksyty, nefeliny, ałunity.
Boksyt jest najbardziej wzbogaconą rudą w tlenek glinu – zawiera ponad 50% tlenku glinu. Do 30% tlenku zawiera nefeliny. A ich najmniejsza zawartość (do 20%) znajduje się w ałunitach.
Również aluminium wtórne stopy aluminium otrzymywane w wyniku przetwarzania odpadów i złomu aluminiowego. Do jego produkcji przetapia się wióry aluminiowe, folię i drut, skrawki blach i rur.
Jak powstaje aluminium pierwotne?
Aluminium pierwotne otrzymuje się metodą zwaną „elektrolizą stopionego tlenku glinu w kriolicie”. Produkcja rudy aluminium jest wieloetapowa proces technologiczny, która obejmuje pozyskiwanie surowców pośrednich: tlenku glinu - soli kriolitowych i fluorkowych - produktów węglowych - aluminium elektrolitycznego.
Głównymi ogniwami tego łańcucha technologicznego są tlenek glinu i aluminium elektrolityczne. Głównym urządzeniem produkcyjnym jest elektrolizer lub wanna aluminiowa. Gęstość aluminium jest wyższa niż gęstość kriolitu. Dlatego w procesie elektrolizy jest oddzielany od stopionego kriolitu-tlenku glinu. Odseparowany metal osiada na dnie wanny, skąd jest zbierany przez kadzie próżniowe. Następnie zebrany metal jest oczyszczany przez chlorowanie i odlewane są z niego wlewki.
Jak powstaje aluminium ze złomu?
Aluminium wtórne jest produkowane przez wytapianie. W tym celu odpady są zbierane i sortowane, a następnie oczyszczane przez obróbkę na zimno. W procesie recyklingu z odpadów usuwane są wszelkie zanieczyszczenia (metale i niemetale), a następnie złom jest przetapiany w piecach paliwowych lub elektrycznych. Gotowy produkt wlewa się do specjalnych wlewków odlewniczych.
Ponieważ produkcja tego metalu wymaga dużej ilości energii, huty aluminium budowane są w pobliżu elektrowni wodnych, które dostarczają najtańszą energię elektryczną. Z tego samego powodu w pobliżu złóż rud aluminium znajdują się przedsiębiorstwa produkujące tlenek glinu.
Więcej więcej informacji na ten i inne podobne tematy znajdziesz w artykułach naszego działu.
Aluminium otrzymuje się przez elektrolizę tlenku glinu rozpuszczonego w stopionym elektrolicie, którego głównym składnikiem jest kriolit.. W czystym kriolicie Na 3 AlF 6 (3NaF AlF 3) stosunek NaF: AlF 3 wynosi 3, aby zaoszczędzić energię elektryczną, konieczne jest, aby ten stosunek był w zakresie 2,6-2,8 podczas elektrolizy, dlatego fluorek glinu AlF 3 jest dodany do kriolitu.
Ponadto do elektrolitu dodaje się trochę CaF 2 , MgF 2 i czasami NaCl w celu obniżenia temperatury topnienia. Zawartość głównych składników w elektrolicie przemysłowym mieści się w następujących granicach, %: Na 3 AlF 6 75-90; AlF3 5-12; MgF2 2-5; CaF 2 2-4; Al 2 O 3 2-10. Wraz ze wzrostem zawartości Al 2 Około 3 ponad 10% gwałtownie wzrasta nietopliwość elektrolitu, przy zawartości mniejszej niż 1,3% zaburzony jest normalny tryb elektrolizy.
Wanna lub elektrolizer, w którym przeprowadza się elektrolizę w celu uzyskania aluminium, ma w planie kształt prostokąta. Schemat przekroju wanny pokazano na ryc. 1. Obudowa 1 wykonana z blach stalowych przykrywa ściany wanny, a dla dużych wanien wykonywana jest z dnem. Wewnątrz znajduje się warstwa szamotu 2, a następnie ściany wyłożone są płytami węglowymi 4, a dno tworzą bloki węglowe paleniskowe 3. Wanna o głębokości 0,5-0,6 m wypełniona jest elektrolitem, a pod nią warstwa ciekłego aluminium.
Anoda węglowa 6 (czasami jest ich kilka) jest zawieszona na stalowych prętach 8 tak, że jej dolny koniec jest zanurzony w elektrolicie, prąd doprowadzany jest do anody przez pręty 8 z opon 7.
Moc elektrolizera (wanny), określona przez natężenie dostarczanego do niego prądu, waha się od 30 kA dla wanien małej mocy do 250 kA dla wanien duża moc. Ponieważ dopuszczalna gęstość właściwa prądu przepływającego przez anodę wynosi 0,65-1,0 A/cm2, wraz ze wzrostem mocy kąpieli zwiększa się powierzchnia anody; wymiary przekroju anody potężnych wanien sięgają 2,8x9 m, wymiary wanny (wewnątrz) - 3,8x10 m.
Istniejące wanny różnią się konstrukcją mocy i anody: wanny z jedną anodą samopiekającą i górnym doprowadzeniem prądu, z tą samą anodą i bocznym doprowadzeniem prądu oraz wanny z anodą z wypalanych bloków. Na ryc. przedstawiono wannę z anodą samopiekającą i górnym doprowadzeniem prądu. 2,a. Anoda o przekroju prostokątnym stale rośnie.
Jego obudowa wykonana jest z blachy stalowej, brykiety z masy elektrod węglowych (koksu naftowego ze smołą węglową) ładowane są od góry. W górnej części masa topi się, a w dolnej części obudowy, gdzie panują wysokie temperatury spiekają się, koksują i zamieniają w solidny blok. Wbija się w nią stalowe kołki 7 zanurzone w masie elektrodowej na różnych głębokościach, umieszczone w dwóch do czterech rzędach wzdłuż wanny.
Pręty te służą do doprowadzenia prądu do anody i utrzymania jej nad kąpielą, obudowa anody jest zamocowana oddzielnie nad kąpielą. Podczas spalania anody najgłębiej położone bolce są na przemian wyciągane z utwardzonej masy i mocowane do więcej wysoki poziom, po chwili są spiekane masą utwardzającą.
Gdy dolna część anody wypala się, opuszcza się ją za pomocą specjalnego mechanizmu, podczas gdy anoda zsuwa się do wnętrza obudowy. Do dolnej części obudowy anody przymocowany jest dzwon zbierający gaz, przeznaczony do wychwytywania gazów uwalnianych wokół anody.
Wanny elektrolityczne ze wstępnie spieczonymi anodami (rys. 2, b) mają zespół anod składający się z kilku (do 20 lub więcej) bloków węglowych lub grafitowych ułożonych w dwóch rzędach. Każdy blok ma cztery stalowe złączki 9 połączone z prętem 11; urządzenie to służy do zasilania prądem i zawieszenia bloku. Wypalone bloki zastępowane są nowymi. Nad wanną znajduje się skrzynka odzysku gazu.
Zastosowanie wypalanych anod pozwoliło na zwiększenie wydajności jednostkowej wanien i znaczne ograniczenie uwalniania szkodliwych substancji rakotwórczych, które powstają podczas koksowania smoły elektrody samopiekającej.
Wanny do elektrolizy są umieszczane w warsztacie w rzędzie po kilkadziesiąt wanien w rzędzie.. Elektrolizę przeprowadza się przy napięciu 4-4,3 V i, jak zauważono, przy gęstości prądu przepływającego przez anodę równej 0,65-1,0 A/cm2. Grubość warstwy elektrolitu w kąpieli wynosi 150-250 mm. Temperatura kąpieli utrzymywana jest w zakresie 950-970°C dzięki ciepłu wydzielającemu się podczas przechodzenia ciągłego szoku przez elektrolit. Takie temperatury występują pod anodą, a na granicy z powietrzem tworzy się skorupa zestalonego elektrolitu, a przy ściankach wanny tworzy się zakrzepła warstwa elektrolitu 10 (czaszka).
Wymagana temperatura kąpieli, tj. wytrącanie w warstwie elektrolitu wymagana ilość ciepło jest dostarczane przy pewnej rezystancji elektrycznej warstwy elektrolitu. Taki opór elektryczny uzyskuje się poprzez utrzymanie składu elektrolitu i grubości jego warstwy przewodzącej w określonych granicach, tj. odległość między anodą a warstwą ciekłego aluminium w granicach 40-60 mm (wzrost np. tej odległości, czyli rezystancji elektrycznej warstwy elektrolitu, powoduje wzrost wytwarzania ciepła podczas przepływu prądu i, odpowiednio, przegrzanie elektrolitu).
Po przyłożeniu napięcia do katody i anody składniki ciekłego elektrolitu ulegają dysocjacji elektrolitycznej, a stop składa się z licznych kationów i anionów. Skład elektrolitu dobierany jest tak, aby zgodnie z wartościami potencjałów rozładowania na elektrodach powstawały tylko kationy Al 3+ i aniony O 2 , które powstają podczas dysocjacji Al 2 O 3 w elektrolicie , może być rozładowany. W związku z tym proces elektrochemiczny na elektrodach jest opisany następującymi równaniami:
- na katodzie 2Al 3+ + 6e -> 2Al
- na anodzie 3O 2- - 6e -> 3O
Aluminium wyładowane na katodzie gromadzi się na dnie wanny pod warstwą elektrolitu. Tlen uwolniony na anodzie oddziałuje z węglem anody, tworząc gazy CO i CO 2 , tj. w tym przypadku spód anody jest utleniany, a zatem anoda jest okresowo obniżana. Gazy CO i CO 2 wychodzą spod anod wzdłuż ich bocznych powierzchni, zawierają toksyczne związki fluoru uwalniane z elektrolitu i pyłu tlenku glinu (dostają się do nich również szkodliwe opary żywiczne z anod samospiekających się); gazy te są wychwytywane i oczyszczane z kurzu i związków fluoru.
Podczas procesu w wannie okresowo ładuj tlenek glinu; kontrolować skład elektrolitu poprzez wprowadzanie dodatków korygujących; za pomocą regulatorów utrzymujemy optymalną odległość pomiędzy anodami a ciekłym aluminium (w granicach 40-50 mm). Tlenek glinu jest ładowany do wanien od góry, przebijając w tym celu skorupę spiekanego elektrolitu za pomocą maszyn poruszających się wzdłuż wanien.
Płynne aluminium usuwa się z kąpieli raz dziennie lub po 2-3 dniach za pomocą wiader próżniowych. Wiadro próżniowe (rys. 3) zawiera 1,5-5 ton aluminium
pojemnik wyłożony szamotem, w którym powstaje próżnia ~70 kPa. Rura wlotowa połączona z gniazdem 6 kadzi jest zanurzona od góry w warstwie ciekłego aluminium znajdującej się w kąpieli i z powodu rozrzedzenia aluminium jest zasysane do kadzi.
Uwolnione gazy anodowe kierowane są najpierw do palników, gdzie spalany jest CO i smoła, a następnie do oczyszczania gazu, gdzie wychwytywane są pyły i związki fluoru.
Wydajność nowoczesnych kąpieli elektrolitycznych to 500-1200 kg aluminium dziennie. Aby uzyskać 1 tonę aluminium zużywa się:
- ~ 1,95 tony tlenku glinu,
- ~25 kg kriolitu,
- 25 kg fluorku glinu,
- 0,5-0,6 tony masy anodowej,
- 14-16 MWh energii elektrycznej.
 Najczęściej spotykane jest aluminium pierwiastek chemiczny na ziemi. Zajmuje trzecie miejsce po tlenie i krzemie. Jego zawartość to 8,8 procent wszystkich zasobów naturalnych.
Najczęściej spotykane jest aluminium pierwiastek chemiczny na ziemi. Zajmuje trzecie miejsce po tlenie i krzemie. Jego zawartość to 8,8 procent wszystkich zasobów naturalnych.
Jak pozyskuje się czyste aluminium?
Ale czy wiesz, że wolne aluminium nie występuje w przyrodzie. Nie ma kopalni aluminium. Jest wydobywany z kopalń zawierających boksyt, ałunit i nefilinę. Aby uzyskać aluminium w czystej postaci, trzeba przejść długą drogę w oddzieleniu metalu od innych pierwiastków chemicznych.
Proces technologiczny otrzymywania aluminiumskłada się z dwóch etapów:
1 Ruda boksytu jest kruszona, uzyskuje się tlenek glinu.
2 .Ekstrakcja aluminium z tlenku glinu.
Tlenek glinu nazywany jest krystalicznym tlenkiem glinu.
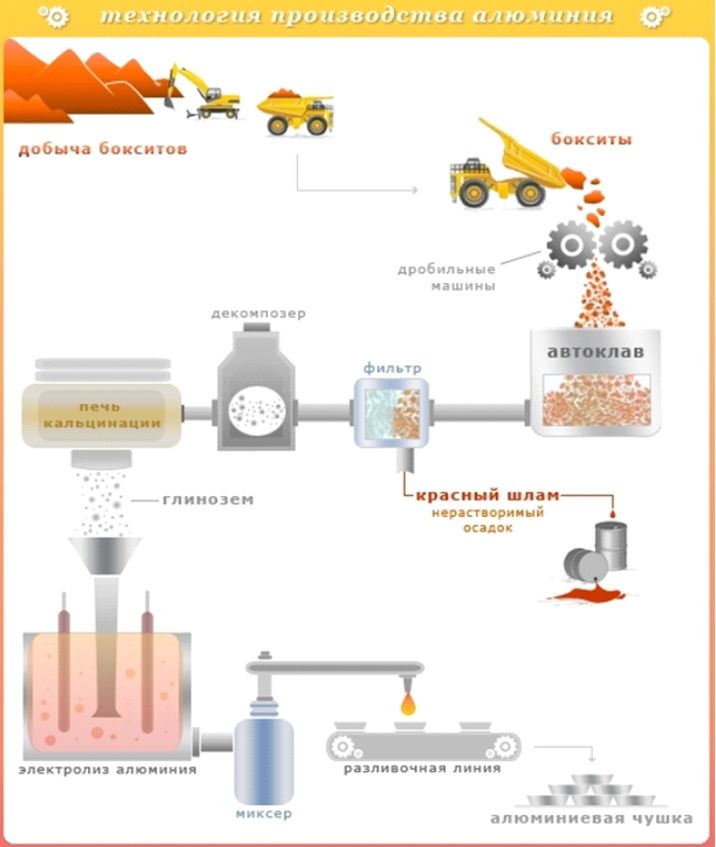
Tlenek glinu poddawany jest procedurze elektrolizy w kriolicie. W temperaturze 960-970 0 C w specjalnych kąpielach aktywuje się niskie napięcie 4,5 V, ale przy bardzo wysoka wytrzymałość obecne 250 tysięcy amperów. W rezultacie ciekłe aluminium jest skoncentrowane na dnie kąpieli wokół katody, podczas gdy tlen gromadzi się wokół anody. Aluminium jest następnie rafinowane i wlewane do form. Następnie powstają różne produkty.
Produkcja aluminium to pracochłonny proces, w którym zużywa się lwią część energii elektrycznej. Dlatego też zakłady produkujące aluminium najczęściej można znaleźć w pobliżu dużych elektrowni wodnych, aby pozyskać tanią energię elektryczną.

Jaka jest przyszłość aluminium?
W przeszłości: Na zamówienie Napoleona III sztućce zostały wykonane z aluminium. Podawano je na uroczystościach dla cesarza i najbardziej honorowych gości, reszta zadowalała się złotymi i srebrnymi naczyniami.
W połowie XIX wieku paryscy fashionistki musiały mieć w swoich strojach przynajmniej jeden kawałek aluminium.
Dziś: Co nie jest wykonane z aluminium; samoloty, paliwo rakietowe, profile szklarniowe, produkty elektroniczne. Produkcja aluminium w hutnictwie stanowi 2% produkcji metali, w przyszłości według prognoz wzrośnie do 4-5%.
W przyszłości: producenci już tworzą tkaniny pokryte cienką warstwą tego metalu. Nazywa się to „tkaniną aluminiowaną”. Na przykład, jeśli tkanina zostanie użyta jako zasłona w upalny dzień, tkanina sprawdzi się na dwa sposoby: ciepło zostanie odbite, a światło z łatwością dostanie się do pomieszczenia. Dzięki temu mieszkanie będzie lekkie i jednocześnie chłodne.
Przez dwa stulecia lekki metal był w stanie podbić świat. A XXI wiek, pod każdym względem, zapowiada się na wiek aluminium.
Pierwszy metaliczne aluminium został otrzymany chemicznie przez niemieckiego chemika F. Wöhlera w 1821 roku (redukcja z chlorku glinu metalicznym potasem po podgrzaniu). W 1854 roku francuski naukowiec Saint-Clair Deville zaproponował elektrochemiczną metodę wytwarzania aluminium poprzez redukcję podwójnego chlorku glinowo-sodowego sodem.
Produkcja i produkcja aluminium
Aluminium metaliczne pozyskiwane jest w trzech etapach:
- Otrzymywanie tlenku glinu (Al 2 O 3) z rud aluminium;
- Otrzymywanie aluminium z tlenku glinu;
- rafinacja aluminium.
Uzyskiwanie tlenku glinu
Około 95% całego tlenku glinu uzyskuje się z rud boksytu.
Boksyt(Francuski boksyt) (od nazwy obszaru Baux na południu Francji) - ruda glinu, składająca się z wodorotlenków glinu, tlenków żelaza i krzemu, surowców do produkcji tlenku glinu i materiałów ogniotrwałych zawierających tlenek glinu. Zawartość tlenku glinu w komercyjnych boksytach waha się od 40% do 60% i więcej. Jest również stosowany jako topnik w metalurgii żelaza.
Zdjęcie 1 - Ruda boksytu
Zazwyczaj boksyt jest ziemistą, podobną do gliny masą, która może mieć teksturę wstęgową, pisolityczną (podobną do grochu) lub jednolitą. W normalnych warunkach atmosferycznych skalenie (minerały, które tworzą) bardzo skorupa Ziemska i będąc glinokrzemianami) rozkładają się z utworzeniem iłów, ale w gorącym klimacie i wysokiej wilgotności końcowym produktem ich rozkładu może okazać się boksyt, gdyż takie środowisko sprzyja usuwaniu zasad i krzemionki, zwłaszcza z syenitów lub gabro. Boksyty są przetwarzane na aluminium etapami: najpierw otrzymuje się tlenek glinu (tlenek glinu), a następnie aluminium metaliczne ( elektrolitycznie w obecności kriolitu).
Głównymi zanieczyszczeniami boksytów są Fe 2 O 3 , SiO 2 , TiO 2 . Drobne zanieczyszczenia boksytów to: Na 2 O, K 2 O, CaO, MgO, pierwiastki ziem rzadkich, Cr, P, V, F, związki organiczne.
Zazwyczaj boksyty są klasyfikowane:
- według koloru;
- przez główny minerał (częściej są mieszane);
- według wieku.
Główne kryteria cechy rudy aluminium są:
- Moduł krzemowy (Msi = Al 2 O 3 /SiO 2 (% wag.)). Im większy moduł krzemowy, tym lepsza jakość(Msi = 7);
- Zawartość żelaza w przeliczeniu na Fe 2 O 3 . Jeśli zawartość Fe2O3 wynosi około 18% wag., wówczas boksyt jest uważany za bogaty w żelazo. Im większa zawartość żelaza, tym trudniej wydobywać boksyty;
- Zawartość siarki. Obecność dużej ilości siarki komplikuje przetwarzanie boksytu;
- Zawartość węglanów w przeliczeniu na CO 3 (2-) . Obecność dużej ilości węglanów komplikuje przetwarzanie boksytu.
Stosowane są boksyty:
- w produkcji tlenku glinu;
- w produkcji materiałów ściernych;
- w produkcji materiałów ogniotrwałych;
- jako topnik do wytapiania stali martenowskich;
- do suszenia gazów i oczyszczania oleju z siarki;
- jako barwnik.
Do chwili obecnej głównymi dostawcami boksytu są:
- Australia - są też ogromne złoża Fe, Au, U, Ni, Co, Cu itp. Bardziej opłaca się kupować surowce z Australii niż przerabiać własne.
- Gwinea - Rosja ma kilka zakupionych miejsc.
- Ameryka Środkowa: Gujana, Jamajka, Suriman.
- Brazylia.
W Europie wszystkie złoża są wyczerpane. Boksyty sprowadzane są z Grecji, ale surowiec ten jest kiepskiej jakości.
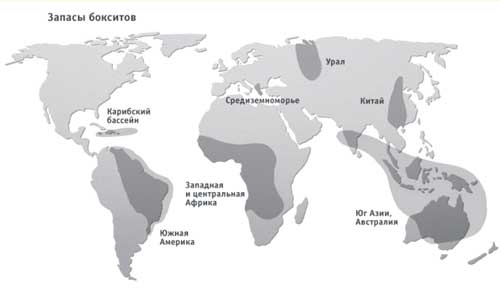
Rysunek 2 - Rezerwy boksytu na świecie
Poniżej znajdują się główne złoża rud aluminium w Rosji.
- Pierwsze złoże odkryto w 1914 r. pod Petersburgiem, w pobliżu miasta Tichwin. Na tym polu wybudowano 6 zakładów. Największa z nich to fabryka aluminium Volkhov. Do tej pory złoże Tichwinskoje jest wyczerpane i działa głównie na importowanych surowcach.
- W 1931 r. odkryto unikalne złoże boksytu wysokiej jakości Severo-Uralskoye (SUBR). Służył jako podstawa do budowy w 1939 r. Uralskiej fabryki aluminium (UAZ). A na bazie kopalni boksytu Południowego Uralu (YUBR) zbudowano hutę aluminium Bogosłowski (BAZ).
- Pole Severoonezhskoye znajduje się na drodze na Półwysep Kolski. Jest w planie, ale data budowy nie jest znana.
- Złoże Vislovskoe jest złożem czystej gliny typu kaolitu. Nie używany do tlenku glinu.
- Pole Timanskoye (Republika Komi, Varkuta). Kanadyjczycy są zainteresowani tą dziedziną, więc planują budowę fabryk (Komi Sual jest spółką holdingową).
Otrzymywanie tlenku glinu z rud boksytu
Ponieważ aluminium jest amfoteryczne, tlenek glinu jest produkowany na trzy sposoby:
- alkaliczny,
- kwas;
- elektrolityczny.
Najbardziej rozpowszechniona jest metoda alkaliczna (metoda K. I. Bayera, opracowana w Rosji pod koniec ubiegłego wieku i stosowana do przetwarzania wysokogatunkowych boksytów z niewielką ilością (do 5–6%) krzemionki). Odkąd wdrożenie techniczne został znacznie ulepszony. Schemat produkcji tlenku glinu metodą Bayera pokazano na rysunku 3.
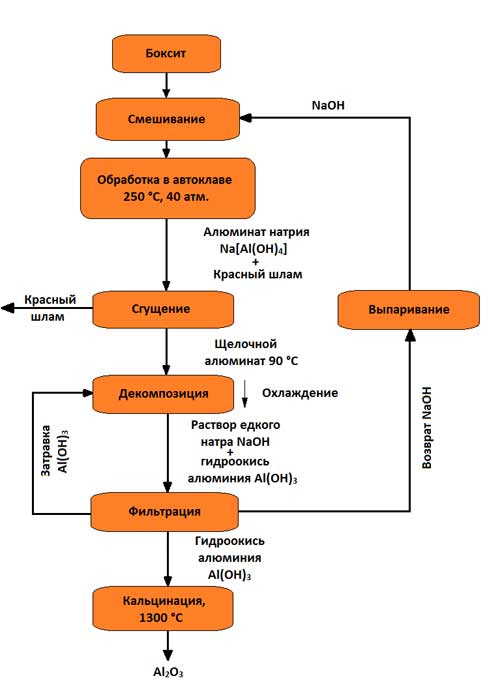
Rysunek 3 - Schemat otrzymywania tlenku glinu metodą Bayera
Istota metody polega na tym, że roztwory glinu ulegają szybkiemu rozkładowi po wprowadzeniu do nich wodorotlenku glinu, a roztwór pozostały z rozkładu po jego odparowaniu w warunkach intensywnego mieszania w temperaturze 169–170 °C może ponownie rozpuszczać tlenek glinu zawarty w boksytach. Ta metoda składa się z następujących głównych operacji:
1. Przygotowanie boksytu polegające na jego kruszeniu i mieleniu w młynach; młyny są dostarczane z boksytem, kaustycznymi alkaliami i nie duża liczba wapno, które poprawia przydział Al 2 O 3 ; uzyskana miazga jest podawana do ługowania;
2. Ługowanie boksytu (w ostatnie czasy dotychczas stosowane okrągłe bloki autoklawowe zostały częściowo zastąpione autoklawami rurowymi, w których ługowanie następuje w temperaturze 230–250 °C (500–520 K), co polega na jego chemicznym rozkładzie w wyniku oddziaływania z roztwór wodny zasady; hydraty tlenku glinu podczas interakcji z alkaliami przechodzą do roztworu w postaci glinianu sodu:
AlOOH+NaOH→NaAlO2 +H2O
Al(OH)3 +NaOH→NaAlO2+2H2O;
SiO2 +2NaOH→Na2SiO3 +H2O;
w roztworze glinian sodu i krzemian sodu tworzą nierozpuszczalny glinokrzemian sodu; tlenki tytanu i żelaza przechodzą do nierozpuszczalnej pozostałości, nadając pozostałości czerwony kolor; ta pozostałość nazywana jest czerwonym błotem. Po zakończeniu rozpuszczania powstały glinian sodu rozcieńcza się wodnym roztworem zasady, obniżając temperaturę o 100 ° C;
3. Oddzielanie roztworu glinianu od czerwonego szlamu, zwykle przeprowadzane przez płukanie w specjalnych zagęszczaczach; w wyniku tego czerwone błoto osiada, a roztwór glinianu jest spuszczany, a następnie filtrowany (klarowany). W ograniczonych ilościach szlam stosuje się np. jako dodatek do cementu. W zależności od gatunku boksytu na 1 tonę wyprodukowanego tlenku glinu przypada 0,6 - 1,0 tony czerwonego błota (suchej pozostałości);
4. Rozkład roztworu glinianu. Jest filtrowany i pompowany do dużych pojemników z mieszadłami (rozkładnikami). Wodorotlenek glinu Al(OH) 3 ekstrahuje się z przesyconego roztworu po ochłodzeniu do 60°C (330 K) i ciągłym mieszaniu. Ponieważ proces ten przebiega powoli i nierównomiernie, a tworzenie i wzrost kryształów wodorotlenku glinu mają bardzo ważne podczas jego dalszej obróbki do rozkładników dodaje się dużą ilość wodorotlenku stałego - nasiona:
Na2O Al2O3 + 4H2O→Al(OH)3 + 2NaOH;
5. Przydział wodorotlenku glinu i jego klasyfikacja; dzieje się tak w hydrocyklonach i filtrach próżniowych, gdzie od roztworu glinianu oddziela się osad zawierający 50 - 60% cząstek Al(OH) 3 . Znaczna część wodorotlenku wraca do procesu rozkładu jako materiał siewny, który pozostaje w obiegu w niezmienionych ilościach. Pozostałość po przemyciu wodą przechodzi do kalcynacji; filtrat jest również zawracany do obiegu (po zatężeniu w wyparkach - w celu wypłukania nowych boksytów);
6. Odwodnienie wodorotlenku glinu (kalcynacja); jest to ostatnia operacja produkcji tlenku glinu; odbywa się w rurowych piecach obrotowych, a od niedawna także w piecach z turbulentnym ruchem materiału w temperaturze 1150 - 1300 °C; surowy wodorotlenek glinu przechodzący przez piec obrotowy, suszony i odwadniany; po podgrzaniu następują kolejno następujące przekształcenia strukturalne:
Al(OH) 3 → AlOOH → γ-Al 2 O 3 → α-Al 2 O 3
200 °C - 950 °C - 1200 °C.
Końcowy kalcynowany tlenek glinu zawiera 30 - 50% α-Al2O3 (korund), reszta to γ-Al2O2.
Ta metoda ekstrahuje 85 - 87% całego wyprodukowanego tlenku glinu. Powstały tlenek glinu jest mocny związek chemiczny o temperaturze topnienia 2050 ° C
Otrzymywanie aluminium przez elektrolizę
Elektrolityczna redukcja tlenku glinu rozpuszczonego w stopie na bazie kriolitu jest przeprowadzana w temperaturze 950-970 °C w elektrolizerze. Elektrolizer składa się z wanny wyłożonej blokami węglowymi, na dnie której a Elektryczność. Ciekłe aluminium uwalniane na dnie służące jako katoda jest cięższe niż stopiona sól elektrolityczna, dlatego jest gromadzone na podłożu węglowym, skąd jest okresowo wypompowywane (rys. 4). Od góry w elektrolicie zanurzone są anody węglowe, które spalają się w atmosferze tlenu uwalnianego z tlenku glinu, uwalniając tlenek węgla (CO) lub dwutlenek węgla (CO2). W praktyce stosuje się dwa rodzaje anod:
- samopieczelne anody Zederberg, składające się z brykietów, tzw. „chlebów” masy Zederberg (węgiel niskopopiołowy z 25-35% pakem smoły węglowej), nadziewanych w osłonę aluminiową; pod działaniem wysokiej temperatury masa anodowa jest wypalana (spiekana);
- wypalane lub „ciągłe” anody wykonane z dużych bloków węglowych (na przykład 1900 × 600 × 500 mm, ważące około 1,1 tony).

Rysunek 4 - Schemat elektrolizera
Natężenie prądu na elektrolizerach wynosi 150 000 A. Są one połączone szeregowo z siecią, to znaczy uzyskuje się układ (serię) - długi rząd elektrolizerów.
Napięcie robocze na kąpieli, które wynosi 4-5 V, jest znacznie wyższe niż napięcie, przy którym rozkłada się tlenek glinu, ponieważ straty napięcia w procesie są nieuniknione. różne części systemy. Bilans surowców i energii po otrzymaniu 1 tony aluminium przedstawiono na rysunku 5.
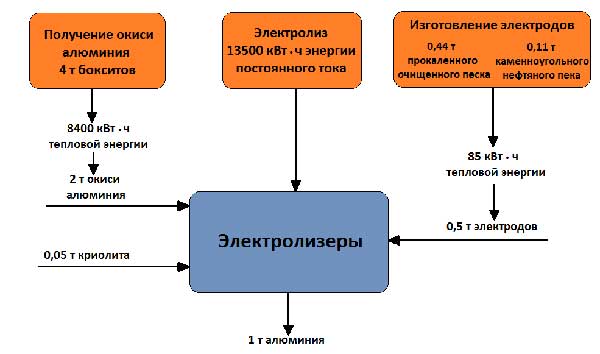
Rysunek 5 - Bilans surowców i energii przy produkcji 1 tony aluminium
W naczyniu reakcyjnym tlenek glinu jest najpierw przekształcany w chlorek glinu. Następnie w szczelnie izolowanej kąpieli zachodzi elektroliza AlCl3 rozpuszczonego w stopionych solach KCl, NaCl. Uwolniony w tym procesie chlor jest odsysany i kierowany do recyklingu; aluminium osadza się na katodzie.
Zaletami tej metody w stosunku do istniejącej elektrolizy ciekłego stopionego kriolit-tlenek glinu (Al 2 O 3 , Na 3 AlF 6 rozpuszczony w kriolicie) są: oszczędność do 30% energii; możliwość zastosowania tlenku glinu, który nie nadaje się do tradycyjnej elektrolizy (np. Al 2 O 3 o wysokiej zawartości krzemu); zastąpienie drogiego kriolitu tańszymi solami; eliminacja niebezpieczeństwa emisji fluorków.
Uzyskanie rafinowanego aluminium
W przypadku aluminium rafinacja elektrolizy z rozkładem wodnych roztworów soli nie jest możliwa. Ponieważ dla niektórych celów stopień oczyszczenia aluminium przemysłowego (Al 99,5 - Al 99,8), otrzymanego przez elektrolizę stopionego kriolit-tlenku glinu, jest niewystarczający, nawet czystsze aluminium (Al 99,99 R) otrzymuje się z przemysłowych odpadów aluminiowych lub metalowych przez rafinację . Najbardziej znaną metodą rafinacji jest elektroliza trójwarstwowa.
Rafinacja przez trójwarstwową elektrolizę
Pokryta blachą stalową, działającą na prąd stały (rys. 6), kąpiel rafinacyjna składa się z paleniska węglowego z przewodami prądowymi i termoizolacyjnej wykładziny magnezytowej. W przeciwieństwie do elektrolizy stopionego kriolit-tlenek glinu, anoda jest tutaj z reguły roztopionym metalem rafinowanym (dolna warstwa anody). Elektrolit składa się z czystych fluorków lub mieszaniny chlorku baru i fluorków glinu i sodu (warstwa środkowa). Aluminium rozpuszczające się z warstwy anodowej w elektrolicie uwalnia się nad elektrolitem (górna warstwa katodowa). Czysty metal służy jako katoda. Prąd dostarczany jest do warstwy katodowej przez elektrodę grafitową.

Rysunek 6 - Schemat ogniwa elektrolitycznego z przednim paleniskiem do rafinacji aluminium (według Fuldy - Ginsberga)
1 - stop aluminium; 2 – elektrolit; 3 - aluminium rafinowane wysokiej częstotliwości; 4 – katoda grafitowa; 5 - ściana magnezytowa; 6 - przedni klakson; 7 - warstwa izolacyjna; 8 - izolacja boczna; 9 - palenisko węglowe; 10 – przewód anodowy; 11 - izolacja paleniska; 12 - żelazne pudełko; 13 - okładka
Kąpiel pracuje w temperaturze 750 - 800 ° C, zużycie energii to 20 kWh na 1 kg czyste aluminium, tj. nieco wyższy niż w konwencjonalnej elektrolizie aluminium.
Metal anodowy zawiera 25-35% Cu; 7 – 12% Zn; 6 – 9% Si; do 5% Fe i niewielka ilość manganu, niklu, ołowiu i cyny, reszta (40 - 55%) to aluminium. Wszystkie metale ciężkie i krzem pozostają w warstwie anodowej podczas rafinacji. Obecność magnezu w elektrolicie prowadzi do niepożądanych zmian w składzie elektrolitu lub do jego silnego żużlowania. Aby usunąć magnez, żużle zawierające magnez poddaje się działaniu topników lub gazowego chloru.
W wyniku rafinacji otrzymuje się czyste aluminium (99,99%) oraz produkty segregacji (produkt Zigera), które zawierają metale ciężkie i krzem i są izolowane w postaci roztworu alkalicznego oraz krystalicznej pozostałości. Roztwór alkaliczny jest odpadem, a stałą pozostałość wykorzystuje się do odkwaszania.
Rafinowane aluminium ma zwykle następujący skład, %: Fe 0,0005 - 0,002; Si 0,002 - 0,005; Cu 0,0005 - 0,002; Zn 0,0005 - 0,002; ślady magnezu; Odpocznij.
Rafinowane aluminium jest przetwarzane na półprodukt o określonym składzie lub stapiany z magnezem (tabela 1).
Tabela 1 - Skład chemiczny aluminium o wysokiej czystości i aluminium pierwotne wg DIN 1712 arkusz 1
|
Dopuszczalne zanieczyszczenia*, % |
||||||||
|
włącznie z |
||||||||
* O ile to możliwe do ustalenia konwencjonalne metody Badania.
** Czyste aluminium dla elektrotechniki (przewody aluminiowe) dostarczane jest w postaci aluminium pierwotnego 99,5 zawierającego nie więcej niż 0,03% (Ti + Cr + V + Mn); oznaczony w tym przypadku jako E-A1, numer materiału 3.0256. Poza tym jest zgodny z VDE-0202.
Rafinacja za pomocą kompleksowych związków glinoorganicznych i topienie stref
Aluminium o wyższej klasie czystości A1 99,99 R można otrzymać przez rafinację elektrolizy czystego lub komercyjnie czystego aluminium przy użyciu złożonych związków glinoorganicznych aluminium jako elektrolitu. Elektroliza odbywa się w temperaturze około 1000°C pomiędzy stałymi elektrodami aluminiowymi i jest zasadniczo podobna do elektrolizy rafinacji miedzi. Charakter elektrolitu dyktuje potrzebę pracy bez powietrza i przy niskiej gęstości prądu.
Ten rodzaj elektrolizy rafinacyjnej, stosowany początkowo tylko w skali laboratoryjnej, jest już przeprowadzany na małą skalę przemysłową – produkuje się kilka ton metalu rocznie. Nominalny stopień oczyszczenia powstałego metalu wynosi 99,999 -99,9999%. Potencjalne obszary zastosowań metalu o tej czystości to kriogeniczna elektrotechnika i elektronika.
Możliwe jest zastosowanie rozważanej metody rafinacji w galwanotechnice.
Nawet więcej wysoka czystość- nominalnie do A1 99,99999 - można uzyskać przez kolejne strefowe topienie metalu. Przetwarzając aluminium o wysokiej czystości w półprodukt, blachę lub drut, należy, biorąc pod uwagę niską temperaturę rekrystalizacji metalu, podjąć szczególne środki ostrożności. Niezwykłą właściwością rafinowanego metalu jest jego wysoka przewodność elektryczna w zakresie temperatur kriogenicznych.
Po raz pierwszy metaliczny glin został otrzymany chemicznie przez niemieckiego chemika F. Wöhlera w 1821 roku (przez redukcję z chlorku glinu metalicznym potasem po podgrzaniu). W 1854 roku francuski naukowiec Saint-Clair Deville zaproponował elektrochemiczną metodę wytwarzania aluminium poprzez redukcję podwójnego chlorku glinowo-sodowego sodem.
Produkcja i produkcja aluminium
Aluminium metaliczne pozyskiwane jest w trzech etapach:
- Otrzymywanie tlenku glinu (Al 2 O 3) z rud aluminium;
- Otrzymywanie aluminium z tlenku glinu;
- rafinacja aluminium.
Uzyskiwanie tlenku glinu
Około 95% całego tlenku glinu uzyskuje się z rud boksytu.
Boksyt(Francuski boksyt) (od nazwy obszaru Baux na południu Francji) - ruda glinu, składająca się z wodorotlenków glinu, tlenków żelaza i krzemu, surowców do produkcji tlenku glinu i materiałów ogniotrwałych zawierających tlenek glinu. Zawartość tlenku glinu w komercyjnych boksytach waha się od 40% do 60% i więcej. Jest również stosowany jako topnik w metalurgii żelaza.
Zdjęcie 1 - Ruda boksytu
Zazwyczaj boksyt jest ziemistą, podobną do gliny masą, która może mieć teksturę wstęgową, pisolityczną (podobną do grochu) lub jednolitą. W normalnych warunkach atmosferycznych skalenie (minerały, które stanowią większość skorupy ziemskiej i są glinokrzemianami) rozkładają się na gliny, ale w gorącym klimacie i dużej wilgotności końcowym produktem ich rozkładu może być boksyt, gdyż takie środowisko sprzyja ich usuwaniu zasad i krzemionki, zwłaszcza z syenitów lub gabro. Boksyty są przetwarzane na aluminium etapami: najpierw otrzymuje się tlenek glinu (tlenek glinu), a następnie aluminium metaliczne (elektrolitycznie w obecności kriolitu).
Głównymi zanieczyszczeniami boksytów są Fe 2 O 3 , SiO 2 , TiO 2 . Drobne zanieczyszczenia boksytów to: Na 2 O, K 2 O, CaO, MgO, pierwiastki ziem rzadkich, Cr, P, V, F, związki organiczne.
Zazwyczaj boksyty są klasyfikowane:
- według koloru;
- przez główny minerał (częściej są mieszane);
- według wieku.
Główne kryteria cechy rudy aluminium są:
- Moduł krzemowy (Msi = Al 2 O 3 /SiO 2 (% wag.)). Im większy moduł krzemowy, tym lepsza jakość (Msi = 7);
- Zawartość żelaza w przeliczeniu na Fe 2 O 3 . Jeśli zawartość Fe2O3 wynosi około 18% wag., wówczas boksyt jest uważany za bogaty w żelazo. Im większa zawartość żelaza, tym trudniej wydobywać boksyty;
- Zawartość siarki. Obecność dużej ilości siarki komplikuje przetwarzanie boksytu;
- Zawartość węglanów w przeliczeniu na CO 3 (2-) . Obecność dużej ilości węglanów komplikuje przetwarzanie boksytu.
Stosowane są boksyty:
- w produkcji tlenku glinu;
- w produkcji materiałów ściernych;
- w produkcji materiałów ogniotrwałych;
- jako topnik do wytapiania stali martenowskich;
- do suszenia gazów i oczyszczania oleju z siarki;
- jako barwnik.
Do chwili obecnej głównymi dostawcami boksytu są:
- Australia - są też ogromne złoża Fe, Au, U, Ni, Co, Cu itp. Bardziej opłaca się kupować surowce z Australii niż przerabiać własne.
- Gwinea - Rosja ma kilka zakupionych miejsc.
- Ameryka Środkowa: Gujana, Jamajka, Suriman.
- Brazylia.
W Europie wszystkie złoża są wyczerpane. Boksyty sprowadzane są z Grecji, ale surowiec ten jest kiepskiej jakości.

Rysunek 2 - Rezerwy boksytu na świecie
Poniżej znajdują się główne złoża rud aluminium w Rosji.
- Pierwsze złoże odkryto w 1914 r. pod Petersburgiem, w pobliżu miasta Tichwin. Na tym polu wybudowano 6 zakładów. Największa z nich to fabryka aluminium Volkhov. Do tej pory złoże Tichwinskoje jest wyczerpane i działa głównie na importowanych surowcach.
- W 1931 r. odkryto unikalne złoże boksytu wysokiej jakości Severo-Uralskoye (SUBR). Służył jako podstawa do budowy w 1939 r. Uralskiej fabryki aluminium (UAZ). A na bazie kopalni boksytu Południowego Uralu (YUBR) zbudowano hutę aluminium Bogosłowski (BAZ).
- Pole Severoonezhskoye znajduje się na drodze na Półwysep Kolski. Jest w planie, ale data budowy nie jest znana.
- Złoże Vislovskoe jest złożem czystej gliny typu kaolitu. Nie używany do tlenku glinu.
- Pole Timanskoye (Republika Komi, Varkuta). Kanadyjczycy są zainteresowani tą dziedziną, więc planują budowę fabryk (Komi Sual jest spółką holdingową).
Otrzymywanie tlenku glinu z rud boksytu
Ponieważ aluminium jest amfoteryczne, tlenek glinu jest produkowany na trzy sposoby:
- alkaliczny,
- kwas;
- elektrolityczny.
Najbardziej rozpowszechniona jest metoda alkaliczna (metoda K. I. Bayera, opracowana w Rosji pod koniec ubiegłego wieku i stosowana do przetwarzania wysokogatunkowych boksytów z niewielką ilością (do 5–6%) krzemionki). Od tego czasu jego parametry techniczne uległy znacznej poprawie. Schemat produkcji tlenku glinu metodą Bayera pokazano na rysunku 3.

Rysunek 3 - Schemat otrzymywania tlenku glinu metodą Bayera
Istota metody polega na tym, że roztwory glinu ulegają szybkiemu rozkładowi po wprowadzeniu do nich wodorotlenku glinu, a roztwór pozostały z rozkładu po jego odparowaniu w warunkach intensywnego mieszania w temperaturze 169–170 °C może ponownie rozpuszczać tlenek glinu zawarty w boksytach. Ta metoda składa się z następujących głównych operacji:
1. Przygotowanie boksytu polegające na jego kruszeniu i mieleniu w młynach; młyny są zasilane boksytem, ługiem kaustycznym i niewielką ilością wapna, co poprawia uwalnianie Al 2 O 3 ; uzyskana miazga jest podawana do ługowania;
2. Ługowanie boksytu (ostatnio dotychczas stosowane okrągłe bloki autoklawowe zostały częściowo zastąpione autoklawami rurowymi, w których ługowanie następuje w temperaturze 230–250 °C (500–520 K), co polega na jego chemicznym rozkładzie z interakcja z wodnym roztworem zasad; hydraty tlenku glinu podczas interakcji z alkaliami przechodzą do roztworu w postaci glinianu sodu:
AlOOH+NaOH→NaAlO2 +H2O
Al(OH)3 +NaOH→NaAlO2+2H2O;
SiO2 +2NaOH→Na2SiO3 +H2O;
w roztworze glinian sodu i krzemian sodu tworzą nierozpuszczalny glinokrzemian sodu; tlenki tytanu i żelaza przechodzą do nierozpuszczalnej pozostałości, nadając pozostałości czerwony kolor; ta pozostałość nazywana jest czerwonym błotem. Po zakończeniu rozpuszczania powstały glinian sodu rozcieńcza się wodnym roztworem zasady, obniżając temperaturę o 100 ° C;
3. Oddzielanie roztworu glinianu od czerwonego szlamu, zwykle przeprowadzane przez płukanie w specjalnych zagęszczaczach; w wyniku tego czerwone błoto osiada, a roztwór glinianu jest spuszczany, a następnie filtrowany (klarowany). W ograniczonych ilościach szlam stosuje się np. jako dodatek do cementu. W zależności od gatunku boksytu na 1 tonę wyprodukowanego tlenku glinu przypada 0,6 - 1,0 tony czerwonego błota (suchej pozostałości);
4. Rozkład roztworu glinianu. Jest filtrowany i pompowany do dużych pojemników z mieszadłami (rozkładnikami). Wodorotlenek glinu Al(OH) 3 ekstrahuje się z przesyconego roztworu po ochłodzeniu do 60°C (330 K) i ciągłym mieszaniu. Ponieważ proces ten przebiega powoli i nierównomiernie, a powstawanie i wzrost kryształów wodorotlenku glinu ma ogromne znaczenie podczas jego dalszej obróbki, do rozkładników dodaje się dużą ilość wodorotlenku stałego - nasiona:
Na2O Al2O3 + 4H2O→Al(OH)3 + 2NaOH;
5. Przydział wodorotlenku glinu i jego klasyfikacja; dzieje się tak w hydrocyklonach i filtrach próżniowych, gdzie od roztworu glinianu oddziela się osad zawierający 50 - 60% cząstek Al(OH) 3 . Znaczna część wodorotlenku wraca do procesu rozkładu jako materiał siewny, który pozostaje w obiegu w niezmienionych ilościach. Pozostałość po przemyciu wodą przechodzi do kalcynacji; filtrat jest również zawracany do obiegu (po zatężeniu w wyparkach - w celu wypłukania nowych boksytów);
6. Odwodnienie wodorotlenku glinu (kalcynacja); jest to ostatnia operacja produkcji tlenku glinu; odbywa się w rurowych piecach obrotowych, a od niedawna także w piecach z turbulentnym ruchem materiału w temperaturze 1150 - 1300 °C; surowy wodorotlenek glinu przechodzący przez piec obrotowy, suszony i odwadniany; po podgrzaniu następują kolejno następujące przekształcenia strukturalne:
Al(OH) 3 → AlOOH → γ-Al 2 O 3 → α-Al 2 O 3
200 °C - 950 °C - 1200 °C.
Końcowy kalcynowany tlenek glinu zawiera 30 - 50% α-Al2O3 (korund), reszta to γ-Al2O2.
Ta metoda ekstrahuje 85 - 87% całego wyprodukowanego tlenku glinu. Powstały tlenek glinu jest silnym związkiem chemicznym o temperaturze topnienia 2050 ° C.
Otrzymywanie aluminium przez elektrolizę
Elektrolityczna redukcja tlenku glinu rozpuszczonego w stopie na bazie kriolitu jest przeprowadzana w temperaturze 950-970 °C w elektrolizerze. Ogniwo składa się z wanny wyłożonej blokami węglowymi, do której dna doprowadzany jest prąd elektryczny. Ciekłe aluminium uwalniane na dnie służące jako katoda jest cięższe niż stopiona sól elektrolityczna, dlatego jest gromadzone na podłożu węglowym, skąd jest okresowo wypompowywane (rys. 4). Od góry w elektrolicie zanurzone są anody węglowe, które spalają się w atmosferze tlenu uwalnianego z tlenku glinu, uwalniając tlenek węgla (CO) lub dwutlenek węgla (CO2). W praktyce stosuje się dwa rodzaje anod:
- samopieczelne anody Zederberg, składające się z brykietów, tzw. „chlebów” masy Zederberg (węgiel niskopopiołowy z 25-35% pakem smoły węglowej), nadziewanych w osłonę aluminiową; pod działaniem wysokiej temperatury masa anodowa jest wypalana (spiekana);
- wypalane lub „ciągłe” anody wykonane z dużych bloków węglowych (na przykład 1900 × 600 × 500 mm, ważące około 1,1 tony).

Rysunek 4 - Schemat elektrolizera
Natężenie prądu na elektrolizerach wynosi 150 000 A. Są one połączone szeregowo z siecią, to znaczy uzyskuje się układ (serię) - długi rząd elektrolizerów.
Napięcie robocze na kąpieli, które wynosi 4-5 V, jest znacznie wyższe niż napięcie, przy którym rozkłada się tlenek glinu, ponieważ straty napięcia w różnych częściach układu są nieuniknione podczas pracy. Bilans surowców i energii po otrzymaniu 1 tony aluminium przedstawiono na rysunku 5.

Rysunek 5 - Bilans surowców i energii przy produkcji 1 tony aluminium
W naczyniu reakcyjnym tlenek glinu jest najpierw przekształcany w chlorek glinu. Następnie w szczelnie izolowanej kąpieli zachodzi elektroliza AlCl3 rozpuszczonego w stopionych solach KCl, NaCl. Uwolniony w tym procesie chlor jest odsysany i kierowany do recyklingu; aluminium osadza się na katodzie.
Zaletami tej metody w stosunku do istniejącej elektrolizy ciekłego stopionego kriolit-tlenek glinu (Al 2 O 3 , Na 3 AlF 6 rozpuszczony w kriolicie) są: oszczędność do 30% energii; możliwość zastosowania tlenku glinu, który nie nadaje się do tradycyjnej elektrolizy (np. Al 2 O 3 o wysokiej zawartości krzemu); zastąpienie drogiego kriolitu tańszymi solami; eliminacja niebezpieczeństwa emisji fluorków.
Uzyskanie rafinowanego aluminium
W przypadku aluminium rafinacja elektrolizy z rozkładem wodnych roztworów soli nie jest możliwa. Ponieważ dla niektórych celów stopień oczyszczenia aluminium przemysłowego (Al 99,5 - Al 99,8), otrzymanego przez elektrolizę stopionego kriolit-tlenku glinu, jest niewystarczający, nawet czystsze aluminium (Al 99,99 R) otrzymuje się z przemysłowych odpadów aluminiowych lub metalowych przez rafinację . Najbardziej znaną metodą rafinacji jest elektroliza trójwarstwowa.
Rafinacja przez trójwarstwową elektrolizę
Pokryta blachą stalową, działającą na prąd stały (rys. 6), kąpiel rafinacyjna składa się z paleniska węglowego z przewodami prądowymi i termoizolacyjnej wykładziny magnezytowej. W przeciwieństwie do elektrolizy stopionego kriolit-tlenek glinu, anoda jest tutaj z reguły roztopionym metalem rafinowanym (dolna warstwa anody). Elektrolit składa się z czystych fluorków lub mieszaniny chlorku baru i fluorków glinu i sodu (warstwa środkowa). Aluminium rozpuszczające się z warstwy anodowej w elektrolicie uwalnia się nad elektrolitem (górna warstwa katodowa). Czysty metal służy jako katoda. Prąd dostarczany jest do warstwy katodowej przez elektrodę grafitową.

Rysunek 6 - Schemat ogniwa elektrolitycznego z przednim paleniskiem do rafinacji aluminium (według Fuldy - Ginsberga)
1 - stop aluminium; 2 – elektrolit; 3 - aluminium rafinowane wysokiej częstotliwości; 4 – katoda grafitowa; 5 - ściana magnezytowa; 6 - przedni klakson; 7 - warstwa izolacyjna; 8 - izolacja boczna; 9 - palenisko węglowe; 10 – przewód anodowy; 11 - izolacja paleniska; 12 - żelazne pudełko; 13 - okładka
Kąpiel pracuje w temperaturze 750 - 800 ° C, zużycie energii wynosi 20 kWh na 1 kg czystego aluminium, czyli nieco więcej niż przy konwencjonalnej elektrolizie aluminium.
Metal anodowy zawiera 25-35% Cu; 7 – 12% Zn; 6 – 9% Si; do 5% Fe i niewielka ilość manganu, niklu, ołowiu i cyny, reszta (40 - 55%) to aluminium. Wszystkie metale ciężkie i krzem pozostają w warstwie anodowej podczas rafinacji. Obecność magnezu w elektrolicie prowadzi do niepożądanych zmian w składzie elektrolitu lub do jego silnego żużlowania. Aby usunąć magnez, żużle zawierające magnez poddaje się działaniu topników lub gazowego chloru.
W wyniku rafinacji otrzymuje się czyste aluminium (99,99%) oraz produkty segregacji (produkt Zigera), które zawierają metale ciężkie i krzem i są izolowane w postaci roztworu alkalicznego oraz krystalicznej pozostałości. Roztwór alkaliczny jest odpadem, a stałą pozostałość wykorzystuje się do odkwaszania.
Rafinowane aluminium ma zwykle następujący skład, %: Fe 0,0005 - 0,002; Si 0,002 - 0,005; Cu 0,0005 - 0,002; Zn 0,0005 - 0,002; ślady magnezu; Odpocznij.
Rafinowane aluminium jest przetwarzane na półprodukt o określonym składzie lub stapiany z magnezem (tabela 1).
Tabela 1 - Skład chemiczny aluminium o wysokiej czystości i aluminium pierwotnego zgodnie z DIN 1712, arkusz 1
|
Dopuszczalne zanieczyszczenia*, % |
||||||||
|
włącznie z |
||||||||
* W miarę możliwości określić konwencjonalnymi metodami badawczymi.
** Czyste aluminium dla elektrotechniki (przewody aluminiowe) dostarczane jest w postaci aluminium pierwotnego 99,5 zawierającego nie więcej niż 0,03% (Ti + Cr + V + Mn); oznaczony w tym przypadku jako E-A1, numer materiału 3.0256. Poza tym jest zgodny z VDE-0202.
Rafinacja za pomocą kompleksowych związków glinoorganicznych i topienie stref
Aluminium o wyższej klasie czystości A1 99,99 R można otrzymać przez rafinację elektrolizy czystego lub komercyjnie czystego aluminium przy użyciu złożonych związków glinoorganicznych aluminium jako elektrolitu. Elektroliza odbywa się w temperaturze około 1000°C pomiędzy stałymi elektrodami aluminiowymi i jest zasadniczo podobna do elektrolizy rafinacji miedzi. Charakter elektrolitu dyktuje potrzebę pracy bez powietrza i przy niskiej gęstości prądu.
Ten rodzaj elektrolizy rafinacyjnej, stosowany początkowo tylko w skali laboratoryjnej, jest już przeprowadzany na małą skalę przemysłową – produkuje się kilka ton metalu rocznie. Nominalny stopień oczyszczenia powstałego metalu wynosi 99,999 -99,9999%. Potencjalne obszary zastosowań metalu o tej czystości to kriogeniczna elektrotechnika i elektronika.
Możliwe jest zastosowanie rozważanej metody rafinacji w galwanotechnice.
Jeszcze wyższą czystość - nominalnie do A1 99,99999 - można uzyskać przez kolejne strefowe topienie metalu. Przetwarzając aluminium o wysokiej czystości w półprodukt, blachę lub drut, należy, biorąc pod uwagę niską temperaturę rekrystalizacji metalu, podjąć szczególne środki ostrożności. Niezwykłą właściwością rafinowanego metalu jest jego wysoka przewodność elektryczna w zakresie temperatur kriogenicznych.


