İlk kez metalik alüminyum Alman kimyager F. Wöhler tarafından 1821'de kimyasal olarak elde edildi (ısıtıldığında alüminyum klorürden metalik potasyum ile indirgeme). 1854'te Fransız bilim adamı Saint-Clair Deville, alüminyum-sodyum çift klorürü sodyum ile indirgeyerek alüminyum üretmek için elektrokimyasal bir yöntem önerdi.
Alüminyum üretimi ve üretimi
Metalik alüminyum üç aşamada elde edilir:
- Alüminyum cevherlerinden alümina (Al 2 O 3) elde edilmesi;
- Alüminadan alüminyum elde edilmesi;
- alüminyum arıtma.
alümina almak
Tüm alüminanın yaklaşık %95'i boksit cevherlerinden elde edilir.
Boksit(Fransız boksiti) (Fransa'nın güneyindeki Baux bölgesinin adından sonra) - alüminyum hidroksitler, demir ve silikon oksitleri, alümina üretimi için hammaddeler ve alümina içeren refrakterlerden oluşan alüminyum cevheri. Ticari boksitlerdeki alümina içeriği %40 ila %60 ve daha fazlası arasında değişmektedir. Ayrıca demir metalurjisinde akı olarak kullanılır.
Resim 1 - Boksit cevheri
Tipik olarak boksit, bantlı, pisolit (bezelye benzeri) veya tek tip bir dokuya sahip olabilen topraklı, kil benzeri bir kütledir. Normal hava koşulları altında, feldspatlar (bunları oluşturan mineraller) en yerkabuğu ve alüminosilikatlar) killerin oluşumu ile ayrışırlar, ancak sıcak iklimlerde ve yüksek nemde boksit, bozunmalarının nihai ürünü haline gelebilir, çünkü böyle bir ortam, özellikle siyenit veya gabrodan alkalilerin ve silisin çıkarılmasını kolaylaştırır. Boksitler aşamalar halinde alüminyuma işlenir: önce alüminyum oksit (alümina) elde edilir ve ardından metalik alüminyum (kriyolit varlığında elektrolitik olarak) elde edilir.
Boksitlerdeki ana safsızlıklar Fe 2 O 3 , SiO 2 , TiO 2'dir. Küçük boksit safsızlıkları şunları içerir: Na 2 O, K 2 O, CaO, MgO, nadir toprak elementleri, Cr, P, V, F, organikler.
Genellikle boksitler sınıflandırılır:
- renge göre;
- ana mineral tarafından (daha sık karıştırılırlar);
- yaşa göre.
Ana kriterler alüminyum cevherinin nitelikleri:
- Silikon modülü (Msi = Al 2 O 3 /SiO 2 (% ağırlık)). Silikon modül ne kadar büyükse, daha iyi kalite(Msi = 7);
- Fe 2 O 3 cinsinden demir içeriği . Fe203 içeriği ağırlıkça yaklaşık %18 ise, boksit yüksek demir olarak kabul edilir. Demir içeriği ne kadar yüksek olursa, boksit madenciliği o kadar zor olur;
- Sülfürlü içerik. Çok miktarda kükürtün varlığı, boksitin işlenmesini zorlaştırır;
- CO3 cinsinden karbonatların içeriği (2-) . Çok miktarda karbonatın varlığı, boksitin işlenmesini zorlaştırır.
Boksit kullanılır:
- alümina üretiminde;
- aşındırıcı malzemelerin üretiminde;
- refrakter malzeme üretiminde;
- açık ocak çeliğini eritmek için bir eritken olarak;
- gazları kurutmak ve yağı kükürtten temizlemek için;
- boya olarak.
Bugüne kadar, ana boksit tedarikçileri:
- Avustralya - ayrıca çok büyük Fe, Au, U, Ni, Co, Cu vb. birikintileri vardır. Avustralya'dan hammadde satın almak, kendi hammaddenizi işlemekten daha karlı.
- Gine - Rusya'nın satın aldığı birkaç koltuk var.
- Orta Amerika: Guyana, Jamaika, Suriman.
- Brezilya.
Avrupa'da tüm mevduatlar tükendi. Boksitler Yunanistan'dan tedarik ediliyor, ancak bu hammadde kalitesiz.

Şekil 2 - Dünyadaki boksit rezervleri
Aşağıda, Rusya'daki ana alüminyum cevher yatakları bulunmaktadır.
- İlk mevduat 1914 yılında Tikhvin kasabası yakınlarında, St. Petersburg yakınlarında keşfedildi. Bu sahada 6 fabrika inşa edildi. En büyüğü Volkhov alüminyum fabrikasıdır. Bugüne kadar, Tikhvinskoye alanı tükendi ve esas olarak ithal hammaddelerle çalışıyor.
- 1931'de benzersiz Severo-Uralskoye yüksek kaliteli boksit yatağı (SUBR) keşfedildi. Ural alüminyum fabrikasının (UAZ) 1939'daki inşaatının temelini oluşturdu. Ve Güney Ural boksit madeni (YUBR) temelinde, Bogoslovsky alüminyum izabe tesisi (BAZ) inşa edildi.
- Severoonezhskoye sahası, Kola Yarımadası yolunda yer almaktadır. Planda var ama yapım tarihi bilinmiyor.
- Vislovskoe yatağı, kaolit tipi saf bir kil yatağıdır. Alümina için kullanılmaz.
- Timanskoye alanı (Komi Cumhuriyeti, Varkuta). Kanadalılar bu alanla ilgileniyorlar, bu yüzden fabrikalar kurmayı planlıyorlar (Komi Sual bir holding şirketidir).
Boksit cevherlerinden alümina elde edilmesi
Alüminyum amfoterik olduğu için alümina üç şekilde üretilir:
- alkali,
- asit;
- elektrolitik.
En yaygın olanı alkalin yöntemdir (son yüzyılın sonunda Rusya'da geliştirilen ve az miktarda (% 5-6'ya kadar) silika içeren yüksek dereceli boksitlerin işlenmesi için kullanılan K. I. Bayer'in yöntemi). O zamandan beri teknik uygulamaönemli ölçüde iyileştirildi. Bayer yöntemiyle alümina üretimi için şema Şekil 3'te gösterilmektedir.
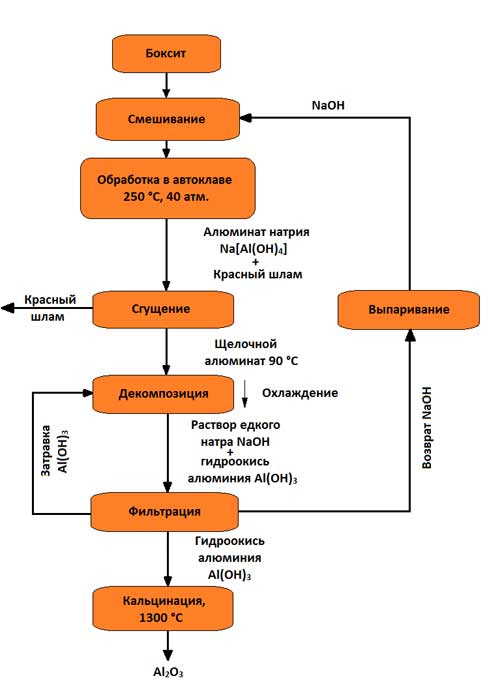
Şekil 3 - Bayer yöntemiyle alümina elde etme şeması
Yöntemin özü, alüminyum çözeltilerinin alüminyum hidroksit verildiğinde hızla bozunması ve 169-170 °C'de yoğun karıştırma koşulları altında buharlaşmasından sonra ayrışmadan kalan çözeltinin, boksitlerde bulunan alüminayı tekrar çözebilmesidir. Bu yöntem aşağıdaki ana işlemlerden oluşur:
1. Değirmenlerde kırma ve öğütme işlemlerinden oluşan boksitin hazırlanması; değirmenler boksit, kostik alkali ile sağlanır ve çok sayıda Al 2 O 3 tahsisini iyileştiren kireç; elde edilen hamur, liç için beslenir;
2. Boksit liçi (içinde son zamanlarşimdiye kadar kullanılan yuvarlak şekilli otoklav blokları, kısmen, sızıntının 230-250 ° C (500-520 K) sıcaklıklarda meydana geldiği boru şeklindeki otoklavlarla değiştirildi; sulu çözelti alkaliler; alüminyum oksit hidratlar, alkali ile etkileşime girdiğinde, sodyum alüminat formunda çözeltiye girer:
AlOOH+NaOH→NaAlO 2 +H 2 O
Al(OH)3 +NaOH→NaAlO2 +2H20;
Si02 +2NaOH→Na2SiO3 +H2O;
çözelti içinde, sodyum alüminat ve sodyum silikat, çözünmeyen bir sodyum alüminosilikat oluşturur; titanyum ve demir oksitler çözünmeyen kalıntıya geçerek kalıntıya kırmızı bir renk verir; bu kalıntıya kırmızı çamur denir. Çözünmenin tamamlanmasının ardından, elde edilen sodyum alüminat, sıcaklık 100 ° C düşürülürken sulu bir alkali çözeltisi ile seyreltilir;
3. Alüminat çözeltisinin kırmızı çamurdan ayrılması, genellikle özel koyulaştırıcılarda yıkanarak gerçekleştirilir; bunun sonucunda kırmızı çamur çökelir ve alüminat solüsyonu süzülür ve ardından süzülür (arıtılır). Sınırlı miktarlarda çamur, örneğin çimentoya katkı maddesi olarak kullanılır. Üretilen 1 ton alümina üzerine boksitin derecesine bağlı olarak 0,6 - 1,0 ton kırmızı çamur (kuru kalıntı) düşer;
4. Alüminat çözeltisinin ayrışması. Filtrelenir ve karıştırıcılar (ayrıştırıcılar) ile büyük kaplara pompalanır. Alüminyum hidroksit Al(OH)3, 60 °C'ye (330 K) soğutulduktan ve sürekli karıştırıldıktan sonra aşırı doymuş bir çözeltiden ekstrakte edilir. Bu süreç yavaş ve düzensiz ilerlediğinden ve alüminyum hidroksit kristallerinin oluşumu ve büyümesi büyük önem daha fazla işlenmesi sırasında, ayrıştırıcılara - tohumlara büyük miktarda katı hidroksit eklenir:
Na 2 O Al 2 O 3 + 4H2O→Al(OH) 3 + 2NaOH;
5. Alüminyum hidroksitin tahsisi ve sınıflandırılması; bu, %50-60 Al(OH)3 partikülü içeren bir çökeltinin alüminat çözeltisinden ayrıldığı hidrosiklonlarda ve vakum filtrelerinde olur. Hidroksitin önemli bir kısmı, değişmeyen miktarlarda dolaşımda kalan bir tohum materyali olarak bozunma işlemine geri döndürülür. Su ile yıkandıktan sonra kalıntı kalsinasyona gider; filtrat da dolaşıma geri döndürülür (buharlaştırıcılarda yoğunlaştırıldıktan sonra - yeni boksitleri süzmek için);
6. Alüminyum hidroksitin dehidrasyonu (kalsinasyon); alümina üretiminin son işlemidir; borulu döner fırınlarda ve son zamanlarda 1150 - 1300 ° C sıcaklıkta malzemenin türbülanslı hareketi olan fırınlarda gerçekleştirilir; bir döner fırından geçen, kurutulmuş ve suyu alınmış ham alüminyum hidroksit; ısıtıldığında, aşağıdaki yapısal dönüşümler sırayla gerçekleşir:
Al(OH) 3 → AlOOH → γ-Al 2 O 3 → α-Al 2 O 3
200 °C - 950 °C - 1200 °C.
Nihai kalsine edilmiş alümina %30 - 50 α-Al2O3 (korindon) içerir, geri kalanı γ-Al 2 O 2'dir.
Bu yöntem, üretilen tüm alüminanın % 85 - 87'sini çıkarır. Elde edilen alümina güçlü bir kimyasal bileşik 2050 ° C'lik bir erime noktası ile
Elektroliz ile alüminyum elde etmek
Kriyolit bazlı bir eriyikte çözünmüş alüminyum oksidin elektrolitik indirgenmesi, bir elektrolitik hücrede 950–970 °C'de gerçekleştirilir. Elektrolizör, tabanı karbon bloklarla kaplı bir banyodan oluşur. elektrik. Altta salınan katot görevi gören sıvı alüminyum, elektrolit tuzu eriyiğinden daha ağırdır, bu nedenle bir kömür bazında toplanır ve buradan periyodik olarak dışarı pompalanır (Şekil 4). Yukarıdan, karbon anotlar, alüminyum oksitten salınan oksijen atmosferinde yanan, karbon monoksit (CO) veya karbon dioksit (CO2) salan elektrolite daldırılır. Pratikte iki tip anot kullanılır:
- bir alüminyum kabuğa doldurulmuş Zederberg kütlesinin (%25 - 35 kömür katranlı düşük küllü kömür) "ekmekleri" olarak adlandırılan briketlerden oluşan kendi kendine pişirilen Zederberg anotları; yüksek sıcaklığın etkisi altında anot kütlesi ateşlenir (sinterlenir);
- büyük karbon bloklardan yapılmış ateşlenmiş veya "sürekli" anotlar (örneğin, 1900 × 600 × 500 mm, yaklaşık 1,1 ton ağırlığında).

Şekil 4 - Elektrolizörün şeması
Elektrolizörlerdeki akım gücü 150.000 A'dır. Şebekeye seri olarak bağlanırlar, yani bir sistem (seri) elde edilir - uzun bir elektrolizör sırası.
4 - 5 V olan banyodaki çalışma voltajı, proseste voltaj kayıpları kaçınılmaz olduğundan, alüminyum oksidin bozunduğu voltajdan çok daha yüksektir. çeşitli parçalar sistemler. 1 ton alüminyum alındığında hammadde ve enerji dengesi Şekil 5'te gösterilmektedir.
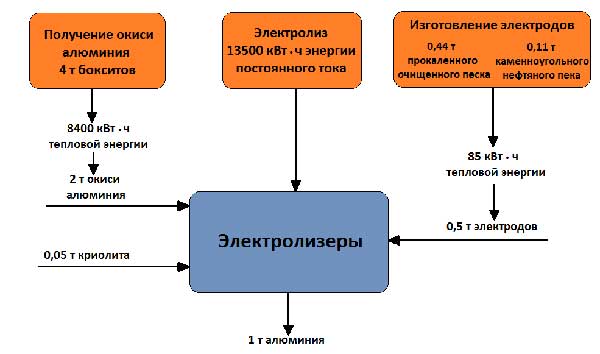
Resim 5 - 1 ton alüminyum üretiminde hammadde ve enerji dengesi
Reaksiyon kabında alüminyum oksit önce alüminyum klorüre dönüştürülür. Daha sonra, sıkıca yalıtılmış bir banyoda, KCl, NaCl'nin erimiş tuzlarında çözünen AlCl3'ün elektrolizi gerçekleşir. Bu süreçte açığa çıkan klor emilir ve geri dönüşüm için beslenir; katotta alüminyum biriktirilir.
Bu yöntemin, sıvı kriyolit-alümina eriyiğinin (kriyolit içinde çözülmüş Al 2 O 3 , Na 3 AlF6) mevcut elektrolizine göre avantajları şunlardır: %30'a kadar enerji tasarrufu; geleneksel elektroliz için uygun olmayan alüminyum oksit kullanma olasılığı (örneğin, yüksek silikon içeriğine sahip Al 2 O 3); pahalı kriyolitin daha ucuz tuzlarla değiştirilmesi; florür emisyonu tehlikesinin ortadan kaldırılması.
Rafine alüminyum elde etmek
Alüminyum için, sulu tuz çözeltilerinin ayrıştırılmasıyla elektrolizin rafine edilmesi mümkün değildir. Bazı amaçlar için, bir kriyolit-alümina eriyiğinin elektrolizi ile elde edilen endüstriyel alüminyumun (Al 99.5 - Al 99.8) saflaştırma derecesi yetersiz olduğundan, endüstriyel alüminyumdan veya metal atıklarından rafine edilerek daha saf alüminyum (Al 99.99 R) bile elde edilir. . En ünlü arıtma yöntemi üç katmanlı elektrolizdir.
Üç katmanlı elektroliz ile arıtma
Doğru akımla çalışan bir çelik sac ile kaplanmış (Şekil 6) arıtma banyosu, akım uçları olan bir kömür ocağı ve ısı yalıtımlı manyezit astardan oluşur. Bir kriyolit-alümina eriyiğinin elektrolizinin aksine, buradaki anot, kural olarak, erimiş rafine metaldir (alt anot tabakası). Elektrolit, saf florürlerden veya baryum klorür ile alüminyum ve sodyum florürlerin (orta katman) bir karışımından oluşur. Elektrolitteki anot tabakasından çözünen alüminyum, elektrolitin (üst katot tabakası) üzerine salınır. Saf metal katot görevi görür. Akım, bir grafit elektrot tarafından katot tabakasına sağlanır.

Şekil 6 - Alüminyumun rafine edilmesi için ön ocaklı bir elektrolitik hücrenin şeması (Fulda - Ginzberg'e göre)
1 - alüminyum eriyik; 2 – elektrolit; 3 - yüksek frekanslı rafine alüminyum; 4 – grafit katot; 5 - manyezit duvar; 6 - ön korna; 7 - yalıtım katmanı; 8 - yan yalıtım; 9 - kömür ocağı; 10 – anot iletkeni; 11 - ocağın izolasyonu; 12 - demir kutu; 13 - kapak
Banyo 750 - 800 ° C'de çalışır, güç tüketimi 1 kg başına 20 kWh'dir. saf alüminyum, yani geleneksel alüminyum elektrolizinden biraz daha yüksek.
Anot metali %25–35 Cu içerir; %7 – 12 Zn; %6 – 9 Si; %5'e kadar Fe ve az miktarda manganez, nikel, kurşun ve kalay, geri kalanı (%40 - 55) alüminyumdur. Rafinasyon sırasında tüm ağır metaller ve silikon anot tabakasında kalır. Elektrolitte magnezyum varlığı, elektrolit bileşiminde istenmeyen değişikliklere veya güçlü cürufuna yol açar. Magnezyumu uzaklaştırmak için magnezyum içeren cüruflar flux veya gaz klor ile işlenir.
Rafinasyon sonucunda, ağır metaller ve silikon içeren ve alkali çözelti ve kristal kalıntı şeklinde izole edilen saf alüminyum (%99,99) ve segregasyon ürünleri (Ziger ürünü) elde edilir. Alkali çözelti bir atıktır ve katı artık asitten arındırma için kullanılır.
Rafine alüminyum genellikle aşağıdaki bileşime sahiptir, %: Fe 0.0005 - 0.002; Si 0,002 - 0,005; Cu 0,0005 - 0,002; Zn 0,0005 - 0,002; Mg izleri; Dinlen.
Rafine alüminyum, belirtilen bileşimde yarı bitmiş bir ürün halinde işlenir veya magnezyum ile alaşımlanır (tablo 1).
Tablo 1 - Kimyasal bileşim DIN 1712 sayfa 1'e göre yüksek saflıkta alüminyum ve birincil alüminyum
|
İzin verilen kirlilik*, % |
||||||||
|
dahil olmak üzere |
||||||||
* Mümkün olduğunca belirlemek geleneksel yöntemler Araştırma.
** Elektrik mühendisliği için saf alüminyum (alüminyum iletkenler), %0.03'ten fazla olmayan (Ti + Cr + V + Mn) birincil alüminyum 99.5 formunda sağlanır; bu durumda E-A1, malzeme numarası 3.0256 olarak belirlenmiştir. Aksi takdirde VDE-0202 ile uyumludur.
Organoalüminyum kompleks bileşikleri ve bölge eritme ile arıtma
Daha yüksek saflık derecesi A1 99.99 R olan alüminyum, elektrolit olarak karmaşık organoalüminyum alüminyum bileşikleri kullanılarak saf veya ticari olarak saf alüminyumun elektrolizinin rafine edilmesiyle elde edilebilir. Elektroliz, katı alüminyum elektrotlar arasında yaklaşık 1000°C'lik bir sıcaklıkta gerçekleşir ve prensip olarak bakırın rafine elektrolizine benzer. Elektrolitin doğası, havasız ve düşük akım yoğunluğunda çalışma ihtiyacını belirler.
İlk başta sadece laboratuvar ölçeğinde kullanılan bu tür arıtma elektrolizi, halihazırda küçük bir endüstriyel ölçekte gerçekleştirilmektedir - yılda birkaç ton metal üretilmektedir. Elde edilen metalin nominal saflaştırma derecesi %99,999 -99,9999'dur. Bu saflıkta bir metal için potansiyel uygulama alanları, kriyojenik elektrik mühendisliği ve elektroniktir.
Ele alınan arıtma yöntemini galvanik kaplamada kullanmak mümkündür.
Hatta daha fazla yüksek saflık- nominal olarak A1 99.99999'a kadar - metalin müteakip bölge eritilmesiyle elde edilebilir. Yüksek saflıkta alüminyumu yarı bitmiş bir ürün, levha veya tel halinde işlerken, metalin düşük yeniden kristalleşme sıcaklığı dikkate alındığında özel önlemler almak gerekir. Rafine edilmiş metalin dikkate değer bir özelliği, kriyojenik sıcaklıklar bölgesindeki yüksek elektrik iletkenliğidir.
Tanıtım
Alüminyum en önemli metaldir, üretim hacmi diğer tüm demir dışı metallerin çıktısını çok geride bırakır ve yalnızca çelik üretiminden sonra ikinci sıradadır. Alüminyum üretiminin yüksek büyüme oranları, benzersiz özelliklerinden kaynaklanmaktadır. fiziksel ve kimyasal özellikler elektrik mühendisliği, uçak ve otomotiv endüstrisi, ulaşım, ev aletleri, inşaat, paketleme alanlarında geniş uygulama alanı bulması sayesinde Gıda Ürünleri vb.
Rusya'nın alüminyum endüstrisi, Sovyet zamanı, demir dışı metallerin üretiminde ülkede hakim durumda ve metal üretiminde dünyada ikinci sırada yer alıyor. AT son yıllar sayesinde bilinen nedenler, alüminyum üretimi için ekipman pratik olarak modernize edilmedi, elektroliz teknolojisi geliştirilmedi, bilimsel araştırma hacmi kabul edilemez derecede azaldı ve gelişmiş ülkelerin belirgin şekilde gerisinde kaldı. Aynı zamanda, ekipman yurtdışında kapsamlı bir şekilde modernize ediliyor, teknoloji geliştiriliyor ve bu da keskin bir şekilde artmasını mümkün kılıyor. ekonomik verim ve alüminyum üretiminin çevre güvenliği.
Son zamanlarda, makine mühendisliği, özellikle uçak endüstrisi ve demiryolu taşımacılığında giderek artan şekilde hafif metallere ihtiyaç duymaktadır. Bu nedenle alüminyum elde etmek için yeni ve daha ekonomik yöntemlerin geliştirilmesi ve mevcut yöntemlerin iyileştirilmesi büyük önem taşımaktadır.
1. Alüminyum endüstrisinin gelişim tarihi
Şu anda alüminyum, demir dışı metaller arasında üretim hacmi açısından ilk sırada yer almakta ve üretimi sürekli genişlemektedir.
Tarihsel olarak, metalik alüminyumdan ilk söz, Birinci Yüzyıl Roma'sının yazılarında yer aldı. AT ünlü ansiklopedi"Historia naturalis" aşağıdaki hikayede bulunabilir. Bir gün, bir Roma kuyumcunun İmparator Tiberius'a yeni metalden yapılmış bir yemek tabağı göstermesine izin verildi. Plaka çok hafifti ve gümüş gibi parlıyordu. Kuyumcu, imparatora metali sıradan kilden çıkardığını söyledi. Ayrıca imparatora, yalnızca kendisinin ve tanrıların kilden nasıl metal elde edileceğini bildiğine dair güvence verdi. İmparator çok ilgilendi. Ancak, insanlar bu hafif metali kilden üretmeye başlarlarsa, altın ve gümüşten oluşan tüm hazinesinin çürüyeceğini hemen anladı. Bu nedenle kuyumcunun beklediği ödül yerine kafası kesildi.
Bu hikayenin ne kadar doğru olduğu bilinmemekle birlikte anlatılan olaylar, insanoğlunun alüminyum üretimi için bir yöntemin keşfinden 2000 yıl önce gerçekleşmiştir. Bu, 1825'te Danimarkalı fizikçi H. Oersted, alüminyum klorürün potasyum amalgam ile termal indirgenmesiyle birkaç miligram metalik alüminyum elde ettiğinde oldu.
Aşağıdaki faktörlerden dolayı alüminyum elde etmede önemli zorluklar ortaya çıktı:
Alüminyumun oksijene yüksek afinitesi. Alüminyum, yaklaşık 2000°C'lik bir sıcaklıkta karbon oksit ile indirgenebilir. Bununla birlikte, zaten 1200°C'de karbon, alüminyum ile etkileşime girerek karbür verir;
Alüminyumun yüksek elektrokimyasal potansiyeli (-1.67V). Sulu çözeltilerden alüminyum elde etmek imkansızdır, çünkü hidrojen oluşumu (su ayrışması) süreci pratik olarak katotta devam edecektir;
Erimiş alüminanın elektroliz olasılığını ortadan kaldıran yüksek alümina erime noktası (2050°C).
Alüminyumun endüstriyel üretimi, Fransız Henri Saint-Clair Deville'in adıyla ilişkilidir. 1827'de alüminyum tanelerini izole etmeyi başaran G. Oersted ve başka bir bilim adamı F. Wehler'in deneylerinin çok iyi farkındaydı. F. Wöhler'in başarısız olmasının nedeni, havadaki bu tanelerin hemen en ince alüminyum oksit filmi ile kaplanmasıydı.
Öncelikle A.S.-K. Deville, metali elde etme sürecinde potasyumu daha ucuz sodyum ile değiştirir ve büyük ölçekte laboratuvar deneyleri yapar. Elde edilen alüminyum klorür, büyük bir çelik boruya yüklendi. sodyum metali. Isıtma sırasında, gaz fazında alüminyum klorür sodyum ile etkileşir ve alüminyum parçacıkları tüpün dibine yerleşir. Reaksiyon sonucunda oluşan taneler özenle toplanmış, eritilmiş ve metal külçeler elde edilmiştir.
Alüminyum üretmenin yeni yolunun çok emek yoğun olduğu kanıtlandı. Ek olarak, alüminyum klorür buharının sodyum ile etkileşimi genellikle bir patlama ile ilerler. Laboratuvar koşullarında bu ciddi bir tehlike oluşturmazken, fabrika koşullarında bir felakete neden olabilir. SORMAK. Deville, alüminyum klorürü bir AlCl3 ve NaCl karışımıyla değiştirdi. Şimdi reaksiyon katılımcıları erimiş durumdaydı. Patlamalar durdu, ancak en önemlisi, elle toplanması gereken küçük metal topaklar yerine önemli miktarda sıvı alüminyum aldılar.
Javel fabrikasındaki deneyler başarı ile taçlandı. 1855'te 6-8 kg ağırlığındaki ilk metal külçe elde edildi.
Alüminyum üretiminin kimyasal yöntemlerle üretimine Rus bilim adamı N. N. Beketov tarafından devam edildi. Kriyolit (Na 3 AlF 6) ve magnezyum arasında bir etkileşim reaksiyonu gerçekleştirdi. N. N. Beketov'un yöntemi, A.S.-K'nin yönteminden çok az farklıydı. Deville, ama daha kolaydı. 1885 yılında Almanya'nın Gmelingem şehrinde, N. N. Beketov yöntemi kullanılarak beş yılda 58 ton alüminyumun elde edildiği bir tesis inşa edildi - 1854'ten bu yana kimyasal yollarla tüm dünya metal üretiminin dörtte birinden fazlası. 1890'a kadar.
Alüminyumun kimyasal yollarla elde edilmesi, sanayiye ucuz metal sağlayamadı. Verimsizdi ve safsızlıklar olmadan saf alüminyum vermedi. Bu, araştırmacıları Farklı ülkeler dünya alüminyum üretmenin yeni yollarını arıyor.
Bilim adamlarının yardımına bir elektrik akımı geldi. 1808'de G. Davy, güçlü bir elektrik pili kullanarak alüminayı ayrıştırmaya çalıştı, ancak boşuna. Yaklaşık 50 yıl sonra, R. Bunsen ve A.S.-K. Deville, alüminyum ve sodyum klorür karışımının elektrolizini bağımsız olarak gerçekleştirdi. Seleflerinden daha şanslıydılar ve küçük alüminyum damlacıkları almayı başardılar. Ancak, o günlerde hala ucuz ve yeterince güçlü elektrik kaynakları yoktu. Bu nedenle, alüminyumun elektrolizi sadece teorik olarak ilgi çekiciydi.
1867'de bir dinamo icat edildi ve kısa süre sonra elektriğin uzun mesafelere nasıl iletileceğini öğrendiler. Elektrik sektörü istila etmeye başladı.
1886'da, Fransa'daki P. Héroult ve ABD'deki C. Hall, modern alüminyum üretim yönteminin temelini hemen hemen aynı anda attılar ve onu erimiş kriyolit içinde çözünmüş alüminanın elektrolizi yoluyla elde etmeyi teklif ettiler (Hall-Hérault yöntemi). Şu andan itibaren yeni yol Alüminyum üretimi, elektrik mühendisliğinin iyileştirilmesinin yanı sıra alüminyum cevherlerinden alümina çıkarmak için yöntemlerin geliştirilmesiyle kolaylaştırılan hızla gelişmeye başlar. Alümina üretiminin gelişimine önemli bir katkı Rus bilim adamları K. I. Bayer, D. A. Penyakov, A. N. Kuznetsov, E. I. Zhukovsky, A. A. Yakovkin ve diğerleri tarafından yapıldı.Çarlık Rusya'nın kendi alüminyum endüstrisi yoktu. Bununla birlikte, alüminyum elektrolizi alanındaki ilk teorik araştırma, ülkemizde demir dışı metallerin elektrometalurjisinin kurucusu olan seçkin Rus bilim adamına, prof. P.P. Fedotiev. 1912'de V.P. Ilyinsky, hemen birçok dile çevrilen "Deneysel; Alüminyum Elektrometalurjisi Üzerine Araştırma" adlı eseri yayınladı. yabancı Diller ve dünyanın her yerindeki metalürji uzmanları için bir başvuru kitabı haline geldi. P.P. Petersburg Politeknik Enstitüsü'ndeki (St. Petersburg Devlet Teknik Üniversitesi) Fedotiev ve Ilyinsky, elektrolitin optimal bileşiminin seçimi konusunda kapsamlı bir araştırma yaptı ve ayrıca alüminanın kriyolit içindeki çözünürlüğünün ve ilavenin kristalleşme sıcaklığının nasıl olduğunu öğrendi. sodyum, alüminyum ve kalsiyum florürler.
28 Mart 1929'da Leningradskaya Pravda gazetesinde, Krasny Vyborzhets fabrikasının pilot tesisinde ilk kez bir banyodan 8 kg alüminyum metal elde edildiğinin bildirildiği bir makale yayınlandı. Bu, alüminyum endüstrimizin başlangıcı oldu.
1931'de Alüminyum-Magnezyum Endüstrisi Araştırma Enstitüsü (VAMI) 1932'de kuruldu. Volkhovsky piyasaya sürüldü ve 1933'te. - Dnipro alüminyum fabrikaları. O zamandan beri alüminyum endüstrisi yurdun çeşitli yerlerinde yayılmaya başladı.
2. Kriyolit-alümina eriyiklerinin elektrolizinin temelleri
Kriyolit-alümina eriyiklerinin elektrolizi, alüminyum elde etmek için ana yöntemdir, ancak bazıları alüminyum alaşımları elektrotermal bir işlemle üretilir.
İlk endüstriyel elektrolizörler 0,6 kA'ya kadar akımlar içindi ve sonraki 100 yıl içinde 300 kA'ya yükseldi. Ancak bu, üretim sürecinin temellerinde önemli değişiklikler getirmedi.
Alüminyum üretiminin genel şeması, Şek. 2.1. Ana ünite elektrolizördür. Elektrolit, içinde alüminanın çözüldüğü hafif bir fazla alüminyum florür içeren bir kriyolit eriyiğidir. İşlem, yaklaşık %1 ila %8 (ağırlıkça) arasında değişen alümina konsantrasyonlarında gerçekleştirilir. Yukarıdan, kısmen elektrolite batırılmış banyoya bir karbon anot indirilir. İki ana tip kurban anot vardır: kendi kendine pişirilen ve önceden pişirilen. İlki, bir dolgu koku ve bir bağlayıcı, zift karışımından oluşan anot kütlesini kavurmak için elektroliz ısısını kullanır. Pişmiş anotlar, önceden pişirilmiş kok ve zift bağlayıcı karışımıdır. Anot kütlesi ve fırınlanmış anot üretimi için teknoloji literatürde ayrıntılı olarak açıklanmaktadır (örneğin bakınız).
Pirinç. 2.1. Alüminadan alüminyum üretim şeması.
Elektroliz sıcaklığında (950-960°C) erimiş alüminyum elektrolitten daha ağırdır ve elektrolizörün alt kısmında bulunur. Kriyolit-alümina eriyikleri çok agresiftir ve karbonlu ve bazı yeni malzemelerle direnç gösterilebilir. Bunlardan elektrolizörün iç astarı yapılır.
AC'yi DC'ye dönüştürmek için modern fabrikalar bir silikon dönüştürücü trafo merkezine (KPP) monte edilmiş, 850V gerilime ve %98,5 dönüşüm oranına sahip yarı iletken doğrultucular kullanılır. Bir redresör ünitesi 63 kA'ya kadar akım verir. Bu tür birimlerin sayısı, hepsi paralel bağlı olduklarından gerekli akım gücüne bağlıdır.
Elektrolizörde yer alan işlem, elektrolit içinde çözülmüş alüminanın elektrolitik bozunmasından oluşur. Alüminyum, bir vakumlu kepçe kullanılarak periyodik olarak dökülen ve dökme veya bir karıştırıcı için dökümhane departmanına gönderilen sıvı bir alüminyum katot üzerinde serbest bırakılır, burada metalin diğer amacına bağlı olarak silikon, magnezyum, manganez, bakır ile alaşımlar hazırlanır veya rafinasyon yapılır. Anotta karbon, salınan oksijen tarafından oksitlenir. Egzoz anot gazı, CO2 ve CO'nun bir karışımıdır.
Elektrolizörler genellikle egzoz gazlarını ve bir temizleme sistemini gideren barınaklar ile donatılmıştır. Bu, zararlı maddelerin atmosfere salınımını azaltır. Teknolojik süreç, fanlar kullanılarak kollektöre gazın emilmesini sağlamak için sığınağın hava geçirmez şekilde kapatılmasını gerektirir. Elektrolizörlerden çıkarılan gazlara karbondioksit (karbon monoksitin çoğu ya elektrolitin üzerinde ya da gaz toplama çanından sonra özel brülörlerde yakılır), nitrojen, oksijen, gaz ve katı florürler ve alümina tozu parçacıkları hakimdir. Bunları ortadan kaldırmak ve sürece geri döndürmek için çeşitli teknolojik şemalar kullanılır.
Modern elektrolizörler, yükleme süresi 10-30 dakika olan bir otomatik alümina besleme sistemi (AAF) ile donatılmıştır.
Elektrolizörde meydana gelen genel reaksiyon, denklem ile temsil edilebilir.
Bu nedenle, teorik olarak, elektroliz işlemi için alümina ve anot karbonunun yanı sıra sadece elektrolitik işlemin uygulanması için değil - alüminanın ayrışması için değil, aynı zamanda yüksek bir çalışma sıcaklığının korunması için gerekli elektrik gücü tüketilir. Uygulamada, buharlaşan ve astar tarafından emilen belirli bir miktarda florür tuzu da tüketilir. 1 ton alüminyum elde etmek için ihtiyacınız olan:
Alüminyum üretimi en enerji yoğun süreçlerden biridir, bu nedenle alüminyum izabe tesisleri enerji kaynaklarına yakın inşa edilir.
Elektrolize giren tüm malzemeler, asgari miktar alüminyumdan daha elektropozitif olan safsızlıklar (demir, silikon, bakır vb.), çünkü bu safsızlıklar elektroliz sırasında neredeyse tamamen metale geçer.
3. Alüminyum elde etmenin alternatif yolları
Uzun süreli kullanımına rağmen, kriyolit-alümina eriyiklerinin elektrolizi ile alüminyum üretmeye yönelik endüstriyel yöntemin bir dizi özelliği vardır. önemli eksiklikler: yüksek spesifik enerji tüketimi, düşük spesifik metal kaldırma ve elektrolizörlerin hizmet ömrü, yüksek işçilik ve sermaye maliyetleri, zararlı maddelerin atmosfere salınması ve bir dizi diğerleri. Bu bağlamda, alüminyum üretimi için başka yöntemler önerilmiştir. Bunlardan bazılarını ele alalım.
3.1. Alüminyum-silikon alaşımlarının elektrotermal üretimi.
Oksitinin doğrudan indirgenmesiyle saf alüminyum elde etmek imkansızdır. Karbotermik prosesler, alüminayı azaltmak için yüksek sıcaklıklar (yaklaşık 2000°C) gerektirir ve alaşım oluşturan bileşenlerin yokluğunda, metal karbona bağlanarak alüminyum karbür (A1 4 C 3) verir. Alüminyum karbür ve alüminyumun birbiri içinde çözünür olduğu ve çok refrakter karışımlar oluşturduğu bilinmektedir. Ayrıca A1 4 C3, A1 2 O3 içinde çözünür, bu nedenle alüminyum oksidin karbon ile indirgenmesi sonucunda yüksek erime noktalarına sahip alüminyum, karbür ve oksit karışımları elde edilir. Böyle bir kütleyi fırından çıkarmak genellikle mümkün değildir. Bu yapılsa bile, ayrılık maliyeti yüksek olacaktır.
Ülkemizde dünyada ilk kez yeterince yüksek teknik ve ekonomik göstergelere sahip endüstriyel ölçekte silikoalüminyum (alüminyum-silikon alaşımları) üretimi için bir yöntem geliştirilmiş ve uygulanmıştır.
Alüminyum-silikon alaşımlarının üretimi için genel teknolojik şema, Şek. 3.1. Hammadde olarak kaolinlere (Al 2 O 3 × 2 SiO 2 × 2H 2 O), kiyanitlere (Al 2 O 3 × SiO 2), distensilimanitlere (Al 2 O 3 × SiO 2) ve düşük demirli boksitlere ek olarak kullanılabilir.
Elektrikli eritme işleminden sonra alaşım, metalik olmayan safsızlıklardan arındırılmak üzere sağlanır. Bunu yapmak için, bu safsızlıkları ıslatan ve onları "toplayan" bir kriyolit ve sodyum klorür karışımından oluşan bir akış sağlanır. Rafine silikoalüminyum ortalama bir bileşime (%) sahiptir: A1 - 61; Si - 36; Fe - 1.7; Ti - 0.6; Zr - 0,5; Ca - 0.7. Bu alaşım silümin üretimi için uygun değildir ve demirden arındırılması gerekir. En yaygın saflaştırma yöntemi, demir ile refrakter intermetalik bileşikler oluşturan manganezdir.

Pirinç. 3.1. Alüminyum-silikon alaşımlarının üretimi için genel şema.
Elde edilen alaşım, çeşitli silüm derecelerine karşılık gelen bir bileşime teknik elektrolitik alüminyum veya ikincil alüminyum ile seyreltilir ve külçelere dökülür.
Füzyon yerine silüm elde etmenin bu yönteminin avantajları elektrolitik alüminyum kristal silikon ile aşağıdaki gibidir: tek bir ünitenin yüksek gücü - modern fırınlar, bir elektrolizörün 160 kA gücünden yaklaşık 30 kat daha yüksek olan 22.5 MB × A gücüne ve dolayısıyla yük trafiğinde bir azalmaya sahiptir. , sermaye maliyetlerinde ve işçilik maliyetlerinde azalma; rezervleri doğada oldukça büyük olan düşük silikon modüllü hammaddelerin kullanımı.
Teorik olarak, saf alüminyum, çeşitli yöntemlerle bir alüminyum-silikon alaşımından izole edilebilir. Ancak endüstrideki donanım ve teknolojik tasarımın karmaşıklığı nedeniyle bu yöntemler şu anda uygulanmamaktadır.
3.2. subhalojen süreci
Halid ve kontamine alüminyum karışımı ısıtılırsa, sıcaklık düşürüldüğünde saf alüminyumun serbest kaldığı bilinmektedir. Bu keşif, alüminyum-alüminyum halojenür sistemlerine olan ilgiyi ateşledi. Metalik alüminyumun, yüksek sıcaklıkta AlX 3 (burada X bir halojendir) ile reaksiyona girerek bir alüminyum alt halojenür oluşturduğu belirlendi:
![]()
Alüminyum subhalojenür gaz halinde bir ürün olduğundan, sıcaklık azaldıkça denge sola kayar. Örneğin, A1C1(G), nispeten yüksek sıcaklıklarda bir reaksiyon bölgesinde Al ve AlC13'ten hazırlanabilir ve daha sonra bir buhar olarak, orantısızlaştığı ve saf alüminyum ve alüminyum klorüre dönüştüğü daha soğuk bir bölgeye aktarılabilir. A1 - A1C1 3 sistemi için denge sabiti, A1 - A1F 3 sisteminden daha yüksektir ve bu nedenle klorür sistemi endüstriyel işlemler için kullanılabilir. Subklorür oluşum sıcaklığı, atmosfer basıncında yaklaşık 1300°C'dir. Alüminyum halojenür alüminyum ile reaksiyona girdiğinden ve pratik olarak diğer metallerin çoğuyla etkileşime girmediğinden, bu işlem alüminyumu alaşımlardan ayırmak için özellikle çekicidir. Zorluklar yalnızca FeCl 3 , MnCl 2 ve diğerleri gibi bazı uçucu amonyum halojenürler ile ortaya çıkar. AlCl3 ile karışımlar oluşturabilir ve oluşan alüminyumu kirletebilirler.
Alcan, beş aşamadan oluşan bir teknoloji geliştirdi:
1. Demir-silikon-alüminyum gibi bir ham alaşımın bir karbotermal indirgeme fırınında üretilmesi.
2. 1300 °C sıcaklıkta bir dönüştürücüde A1 ve AJC1 arasındaki etkileşim.
3. Damıtma kolonlarında buharlı halojenürler ve subhalojenürlerin ayrılması.
4. Klorür ve alüminyum açısından zengin sıvı alaşım arasındaki reaksiyon için AICI dönüşü.
5. A1C1'in ayrışması, alüminyum üretimi ve düzeltme için A1C1 3'ün iadesi.
Subklorür yöntemi, alüminyum alaşımlarının endüstriyel olarak rafine edilmesi için büyük ilgi görmektedir.
3.3. Bu süreç
Thoth yöntemiyle alüminyum elde etme şeması, Şek. 3.2. Alüminyum içeren hammaddeler uygun hazırlandıktan sonra kok ve SiCl4 varlığında akışkan yatakta klorlanır. İkincisi, Si02'nin klorlama reaksiyonunu bastırmak için kullanılır. Akışkan yataklı fırınlarda (BF) klorlamanın bir sonucu olarak, AlCl 3 , FeCl 3 , TiCl 4 ve SiCl 4 içeren bir gaz-buhar karışımı (VGM) elde edilir. İlk kondansatörde, katı haldeki FeCl3'ün yaklaşık %75'i PGM'den salınır ve oksitleyici reaktöre gönderilir, burada atmosferik oksijen ile etkileşime girerek Fe2O3 ve C12 oluşumuna neden olur. Klor, klorlama için iade edilir. İkinci yoğunlaştırıcıda kalan FeCl3 serbest bırakılır ve A1C1 3 yoğunlaşır. Titanyum ve silikon klorürler üçüncü kondansatörde yoğunlaştırılır. Bu klorürlerin ayrılması, bir damıtma kolonunda gerçekleştirilir.
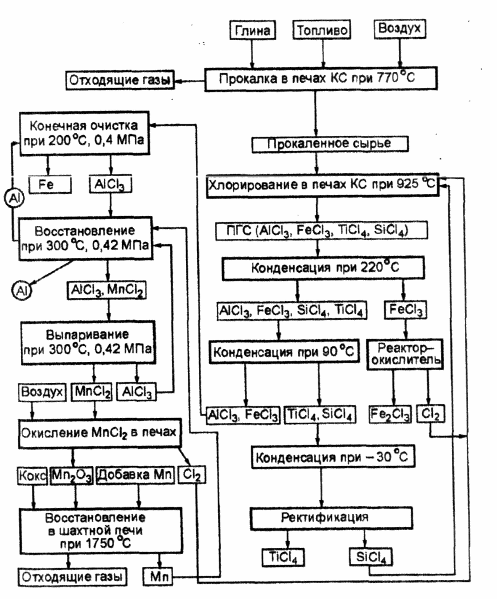
Pirinç. 3.2. Thoth yöntemiyle alüminyum elde etme şeması.
İkinci kondansatörden boşaltılan alüminyum ve demir klorürleri ısıtılır, bir kontak temizleyiciye pompalanır, burada hareketli bir katı alüminyum partikül tabakası ile ters akımda temas ederler. Reaksiyonun gerçekleştiği yer burasıdır:
Saflaştırılmış alüminyum klorür metalotermik indirgemeye beslenir. Alüminyumdan daha fazla klor afinitesine sahip teknik olarak mevcut indirgeyici maddeler sodyum, magnezyum ve manganezdir. Ancak yolun ilk iki unsuru ve bunların üretimi çok enerji yoğundur. Bu nedenle, işlemin geliştiricilerine göre, manganez kullanımının, çok daha düşük enerji tüketimi ile karbotermik yöntemle klorürden yeniden üretilebilen belirli avantajları vardır. Alüminyum klorürün manganez ile indirgenmesi sırasında aşağıdaki reaksiyonlar meydana gelir:
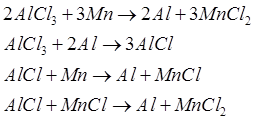
MnCl2 ile reaksiyona girmemiş AlCl3 karışımından elde edilen alüminyum, siklon ayırıcılarda ayrılırken, manganez ve alüminyum klorürler bir buharlaştırıcıda ayrılır. Alüminyum klorür, alüminyum üretmek için reaktöre geri döndürülür ve manganez klorür, katı manganez ve klor oksitleri oluşturmak için oksijenle reaksiyona girer. Manganez oksit, kok ve kireç taşının yüklendiği şaft fırınlarında karbotermik yöntemle metale indirgenir. Manganez, işlem sırasındaki kayıplarını telafi etmek için fırına eklenir.
Dezavantajlara bu süreç Diğer metalotermik yöntemlerin yanı sıra, ortaya çıkan ürünün bir indirgeyici metal ile kirlenmesini, indirgeyici maddenin yenilenmesi için üretimin organize edilmesi ihtiyacını ve sermaye maliyetlerinin artmasını içerir.
1966-1973 yıllarında laboratuvar ortamında ve büyütülmüş ölçekte manganez ile indirgenerek alüminyum üretimine yönelik araştırmalar yapılmıştır. Daha sonra, literatürde endüstriyel gelişme ile ilgili herhangi bir rapor yoktu. bu yönde görünüşe göre, bu karmaşık çok aşamalı sürecin teknik uygulamasındaki önemli zorluklardan kaynaklanmaktadır.
3.4. Klorür eriyiklerinin elektrolizi
Ocak 1973'te Alcoa, alüminyum üretimi için yeni bir yöntem geliştirdiğini duyurdu. Firma, süreç üzerinde 15 yıl çalıştı ve 23 milyon dolar harcadı.
Bu yöntem, alüminyum klorür üretimini ve müteakip elektrolizini içerir. 1976'da Alcoa şirketinin alüminyum üretimi için klorür teknolojisinin endüstriyel uygulamasına geçişi hakkında raporlar vardı. Filistin şehrinde (Teksas, ABD) bu yöntemle yılda 30 bin ton alüminyum üretim tasarım kapasiteli bir tesis faaliyet gösteriyordu.
Temel teknolojik şema, Şek. 2.4.

Pirinç. 3.3. Teknoloji sistemi klorürden alüminyum elde etmek.
Alüminyum klorür su için yüksek bir afiniteye ve oksitler ve hidrooksiklorürler oluşturma eğilimine sahiptir. Bu kapsamda alınması saf formu zor bir görevdir. Nemin varlığı korozyona neden olur ve oksijen içeren bileşiklerin varlığı anotların çökelmesine ve oksidasyonuna yol açar. "Alcoa" firması, bu sorunları kısmen çözen saflaştırılmış alüminanın klorlanmasını önerdi. Bununla birlikte, hidrojen veya nem ile ilgili olarak klorlama sırasında karbonun saflığı için artan gereksinimlere uymak gerekir.
Son zamanlarda, Toth Aluminium Corporation'ın ana bileşenin en az %99.97'sini içeren alüminyum klorürü büyük bir endüstriyel ölçekte üretmeyi başardığına dair raporlar var.
Granül veya buhar halinde elde edilen alüminyum klorür, elektrolize beslenir. Bu teknolojide kullanılan elektrolizör, şamot tuğlalarla kaplanmış çelik bir kasa ve alt kısımda ayrıca diyatomlu tuğlalardan oluşur, yani. klorür eriyikleri ile zayıf bir şekilde etkileşime giren ısı yalıtımlı iletken olmayan refrakter malzeme. Banyonun alt kısmında sıvı alüminyumun toplanması için grafit bölme bulunmaktadır. Elektrolitik hücrenin kapağı, alüminyum klorürün yüklenmesi, alüminyumun periyodik olarak emilmesi ve alüminyum klorür üretiminde kullanılan gaz halindeki klorun sürekli çıkışı için açıklıklara sahiptir. Elektrolizörün yan duvarları ve kapağı su soğutmalıdır.
Elektroliz, grafit tüketilmeyen elektrotlar kullanır. Bu avantaj (kriyolit-alümina eriyiklerinin elektrolizi ile karşılaştırıldığında), nispeten düşük bir işlem sıcaklığı (yaklaşık 700ºС) ile birlikte, elektrolizörlerin tamamen sızdırmaz hale getirilmesini mümkün kılar.
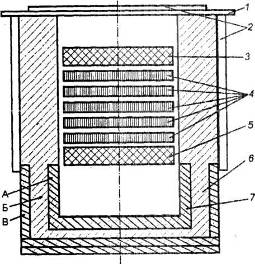
Pirinç. 2.5. Alüminyum klorürün elektrolizi için bipolar elektrotlu bir elektrolitik hücre şeması.
1 - kapak: 2 - su soğutma: 3 - anot; 4 - bipolar elektrotlar; 5 - katot; 6 - astar; 7 - alüminyum toplamak için bölme. Malzeme: A - grafit; B - havai fişek; B - diatom.
Alüminyum klorürün elektrolitik ayrışması, teorik olarak, alüminyum klorürün ayrışma voltajı çok daha yüksek olduğu için, kriyolit-alümina eriyiklerinin elektrolizinden daha yüksek bir voltaj gerektirir. Bu nedenle, işlemin dezavantajları, elektrolizöre büyük miktarda ısı tedarik etme ihtiyacını ve önemli voltaj kayıplarını içerebilir. Bununla birlikte, bir bipolar elektrot sistemi kullanıldığında yüksek omik ve termal kayıplar önemli ölçüde azalır. Hücrede, üst elektrot anottur, alt kısım katottur ve aralarında üst kısmı katot ve alt kısmı anot olan grafit elektrotlar bulunur. Aynı zamanda, hesaplama sonuçları, bipolar elektrot sayısındaki artış ve kesit alanlarındaki azalma ile kaçak akımların arttığını, yani. akımın bir kısmı, kaplamanın elektrolit emdirilmiş kısmından ve kaplama ile iki kutuplular arasındaki kanallardan, elektrokimyasal çalışma yapmadan akar. Bu kaçak akımlar, akım çıkışında bir azalmaya neden olur.
Atmosferik basınçta erime ve kaynama noktalarının yakınlığı nedeniyle, alüminyum klorür pratik olarak erimeden süblimleşir. Süblimleşme sıcaklığı 180.2°C'dir. Üçlü nokta, 192,6°C'lik bir sıcaklığa ve 0,23 MPa'lık bir mutlak basınca karşılık gelir. Bu bağlamda elektrolit olarak alüminyum klorür (%5 ± 2 (kütle)), lityum klorür (~%28 (kütle)) ve sodyum klorür (%67 (kütle)) erimiş bir karışımı kullanılır. Bu eriyiklerde A1C1 3'ün aktivitesi azalır. Bu büyük ölçüde, örneğin erimiş klorür karışımlarında A1C13'ün kompleks anyonlara bağlanmasından kaynaklanmaktadır.
Kutuplar arası mesafe 1.0 - 1.5 cm, sıcaklık 700 ± 30ºС, akım yoğunluğu -0.8 - 2.5 A / cm2'dir.
Bulgular.
Kriyolit-alümina eriyiklerinin elektrolizi ile karşılaştırıldığında, klorürünün elektrolizi yoluyla Alcoa alüminyum üretimi yönteminin Amerika Birleşik Devletleri'ndeki endüstriyel uygulaması sırasında öngörülen ve onaylanan ana avantajlar, düşük kaliteli alüminyum içeren hammaddeler kullanma olasılığıdır. elektroliz sırasında yaklaşık %30 oranında özgül güç tüketimi ve yüksek kaliteli karbon içeren elektrot malzemelerinin tüketiminin ortadan kaldırılması, florürler yerine daha az kıt ve agresif klorürlerin kullanılması, işgücü verimliliğinin artırılması, sermaye yatırımlarının azaltılması, maliyetlerin düşürülmesi, nihai ürünler ve çevreye zararlı emisyonlar.
Son zamanlarda, alüminyum üretimi için klorür yönteminin avantajları, elektrik maliyetindeki artış, mevcut endüstriyel alüminyum üretim yöntemi için hammaddeler ve artan koruma gereksinimleri nedeniyle daha somut hale geldi. çevre ve düşük kaliteli boksit olmayan hammaddelerden saf alümina elde edilmesinde şimdiye kadar olumlu sonuçların olmaması.
Böylece, en umut verici alternatif yollar alüminyum üretimi, bipolar elektrotlu elektrolizörlerde alüminyum klorürün elektrolizidir.
bibliyografya
1. Rozen B. M., Rozen Ya. B. Özel değerli metal. - M.: Metalurji, 1975. - 128 s.
2. Kolodin E.A., Sverdlin V.A., Svoboda R.V. Alüminyum elektrolizörlerin yanmış anotlarının üretimi. - M.: Metalurji, 1980, - 84 s.
3. Yankho E.A., Vorobyov D.N. Anot kütlesinin üretimi. - M.: Metalurji, 1975. - 128 s.
4. M. M. Vetkzhov, A. M. Ts’shlakov ve S. N. Shkolnikov, Elektrometalurji Alüminyum ve Magnezyum. - M.: Metalurji, 1987. - 320 s.
5. Shchenkov V.V., Litvak S.N. Yeni geliştirme teknolojik süreçler alüminyum üretimi // Tsv. metalurji: Boğa. NTI / Colormetinformation. - 1974. - No. 9. - S. 38 - 41.
6. Sandler R.A., Rapier A. Kh. Alüminyum ve magnezyumun elektrometalurjisi. - L: LGI, 1983. - 94 s.
 Alüminyum en yaygın olanıdır. kimyasal element yerde. Oksijen ve silikondan sonra üçüncü sırada yer alır. İçeriği tüm doğal kaynakların yüzde 8.8'idir.
Alüminyum en yaygın olanıdır. kimyasal element yerde. Oksijen ve silikondan sonra üçüncü sırada yer alır. İçeriği tüm doğal kaynakların yüzde 8.8'idir.
Saf alüminyum nasıl elde edilir?
Fakat serbest alüminyumun doğada bulunmadığını biliyor muydunuz? Alüminyum madenleri yok. Boksit, alunit ve nefilin içeren madenlerden çıkarılır. Saf haliyle alüminyum elde etmek için metali diğer kimyasal elementlerden ayırmada uzun bir yol kat etmek gerekir.
Alüminyum elde etmenin teknolojik süreciiki aşamadan oluşur:
1 .Boksit cevheri ezilir, alümina elde edilir.
2 .Alüminadan alüminyumun çıkarılması.
Alümina kristal alümina olarak adlandırılır.
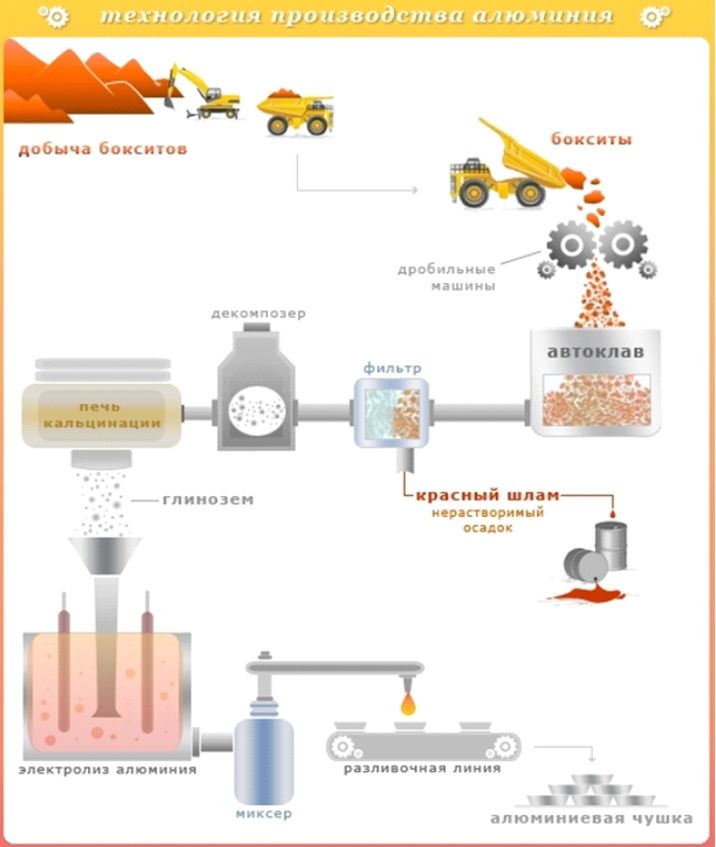
Alümina, kriyolit içinde elektroliz prosedürüne tabi tutulur. 960-970 0 C sıcaklıkta, özel banyolarda 4,5 Voltluk düşük bir voltaj etkinleştirilir, ancak çok yüksek güç mevcut 250 bin amper. Sonuç olarak, sıvı alüminyum, banyonun dibinde katot çevresinde yoğunlaşırken, oksijen anot çevresinde birikir. Alüminyum daha sonra rafine edilir ve kalıplara dökülür. Daha sonra çeşitli ürünler yapılır.
Alüminyum üretimi, elektriğin aslan payını gerektiren emek yoğun bir süreçtir. Bu nedenle, ucuz elektrik elde etmek için alüminyum tesisleri çoğunlukla büyük hidroelektrik santrallerinin yakınında bulunabilir.

Alüminyumun geleceği nedir?
Geçmişte: Napolyon III'ün emriyle çatal bıçak takımı alüminyumdan yapılmıştır. Kutlamalarda imparatora ve en onurlu konuklara servis edildi, geri kalanı altın ve gümüş kaplarla yetindi.
On dokuzuncu yüzyılın ortalarında, Parisli modacıların kıyafetlerinde en az bir parça alüminyum olması gerekiyordu.
Bugün: Alüminyumdan yapılmayan; uçak, roket yakıtı, sera profilleri, elektronik ürünler. Metalurjide alüminyum üretimi metal üretiminin %2'sini oluşturuyor, gelecekte tahminlere göre %4-5'e çıkacak.
Gelecekte:üreticiler zaten bu metalden ince bir tabaka ile kaplanmış kumaşlar yaratıyorlar. Buna "alüminize kumaş" denir. Örneğin, kumaş sıcak bir günde perde olarak kullanılırsa, kumaş iki şekilde iyi bir iş çıkaracaktır: ısı yansıtılacak ve ışık odaya kolayca girecektir. Böylece daire hafif ve aynı zamanda serin olacak.
İki yüzyıl boyunca hafif metal dünyayı fethetmeyi başardı. Ve yirmi birinci yüzyıl, tüm hesaplara göre, alüminyumun yüzyılı olmayı vaat ediyor.
1. Alüminyum oksitin hidrojen ile geri kazanımı
2. elektrolitik
3. Metal-termal
4. Pirometalurjik
5. Hidrometalurjik
181. Pik demir üretimi için başlangıç malzemeleri şunlardır:
1. Demir cevherleri
2. Hurda metal, eritkenler
3. Demir cevherleri, eritkenler, yakıt
4. Demir cevherleri, kok
5. Boksitler
182. Dökme demir şu şekilde eritilir:
1. Yüksek fırın
3. Şaft fırınları
4. Tünel fırın
5. Oda fırını
183. Bir demirli metal alaşımı:
1. Nikelin
2. Elektron
5. Gri dökme demir
184. %0,2 ila %2 karbon içeriğine sahip demir alaşımları:
5. Sementitler
185. Karbon içeriği %2'nin üzerinde olan demir alaşımlarına şunlar denir:
5. Nikelin
186. Elektroliz ile alüminyum elde edilir:
1. Kutupov
2. Kriyolit ile alüminyum oksitin erimiş karışımı
3. Mezunlar
4. Alüminyum hidroksit
5. Nefelin
187. Silikonlu alüminyum alaşımlarına şunlar denir:
1. Duralümin
3. Siluminler
188. Bakır, magnezyum, manganez içeren alüminyum alaşımlarına şunlar denir:
1. Duralümin
3. Siluminler
189. Karbonlu bir demir alaşımı (%2'ye kadar) şunlardan oluşur:
1. Östenit
2. Ostenit ve ledeburit
3. Sementit
4. Sementit ve ledeburit
5. Ledeburita
190. Karbon içeriği (%2-4) olan dökme demir şunlardan oluşur:
1. Östenit
2. Ostenit ve ledeburit
3. Sementit
4. Sementit ve ledeburit
5. Ledeburita
191. %4'ten fazla karbon içeriğine sahip dökme demir aşağıdakilerden oluşur:
1. Östenit
2. Ostenit ve ledeburit
3. Sementit
4. Sementit ve ledeburit
5. Ledeburita
192. Nikel çeliğe yapışır:
193. Manganez çelik verir:
1. Kırmızı sertlik, mukavemet, yüksek sıcaklık korozyon direnci
2. Mukavemet, süneklik, korozyon direnci
3. Normal koşullar altında mukavemet
4. Sertlik ve korozyon direnci
5. Sertlik, aşınma direnci, darbe direnci
194. Niyobyum çelik verir:
1. Artan süneklik ve viskozite
2. Dayanıklılık
3. Sertlik ve korozyon direnci
4. Asit direnci
5. Yüksek sıcaklıklarda mukavemet
195. Molibden çelik verir:
1. Kırmızı sertlik, mukavemet, yüksek sıcaklık korozyon direnci
2. Mukavemet, süneklik, korozyon direnci
3. Normal koşullar altında mukavemet
4. asit direnci
5. Sertlik, aşınma direnci, darbe direnci
Petrol kok üretimi için hammadde,
2. Ağır petrol ürünleri
Metalik alüminyum ilk kez 1821'de Alman kimyager F. Wöhler tarafından kimyasal olarak elde edildi (ısıtıldığında alüminyum klorürden metalik potasyum ile indirgenerek). 1854'te Fransız bilim adamı Saint-Clair Deville, alüminyum-sodyum çift klorürü sodyum ile indirgeyerek alüminyum üretmek için elektrokimyasal bir yöntem önerdi.
Alüminyum üretimi ve üretimi
Metalik alüminyum üç aşamada elde edilir:
- Alüminyum cevherlerinden alümina (Al 2 O 3) elde edilmesi;
- Alüminadan alüminyum elde edilmesi;
- alüminyum arıtma.
alümina almak
Tüm alüminanın yaklaşık %95'i boksit cevherlerinden elde edilir.
Boksit(Fransız boksiti) (Fransa'nın güneyindeki Baux bölgesinin adından sonra) - alüminyum hidroksitler, demir ve silikon oksitleri, alümina üretimi için hammaddeler ve alümina içeren refrakterlerden oluşan alüminyum cevheri. Ticari boksitlerdeki alümina içeriği %40 ila %60 ve daha fazlası arasında değişmektedir. Ayrıca demir metalurjisinde akı olarak kullanılır.
Resim 1 - Boksit cevheri
Tipik olarak boksit, bantlı, pisolit (bezelye benzeri) veya tek tip bir dokuya sahip olabilen topraklı, kil benzeri bir kütledir. Normal hava koşulları altında, feldspatlar (yerkabuğunun çoğunu oluşturan ve alüminosilikatlar olan mineraller) kil oluşturmak üzere ayrışırlar, ancak sıcak iklimlerde ve yüksek nemde, böyle bir ortam ayrışmayı desteklediğinden, boksit ayrışmasının son ürünü olabilir. alkaliler ve silika, özellikle siyenitlerden veya gabrodan. Boksitler aşamalar halinde alüminyuma işlenir: önce alüminyum oksit (alümina) elde edilir ve ardından metalik alüminyum (kriyolit varlığında elektrolitik olarak) elde edilir.
Boksitlerdeki ana safsızlıklar Fe 2 O 3 , SiO 2 , TiO 2'dir. Küçük boksit safsızlıkları şunları içerir: Na 2 O, K 2 O, CaO, MgO, nadir toprak elementleri, Cr, P, V, F, organikler.
Genellikle boksitler sınıflandırılır:
- renge göre;
- ana mineral tarafından (daha sık karıştırılırlar);
- yaşa göre.
Ana kriterler alüminyum cevherinin nitelikleri:
- Silikon modülü (Msi = Al 2 O 3 /SiO 2 (% ağırlık)). Silikon modül ne kadar büyük olursa kalite o kadar iyi olur (Msi = 7);
- Fe 2 O 3 cinsinden demir içeriği . Fe203 içeriği ağırlıkça yaklaşık %18 ise, boksit yüksek demir olarak kabul edilir. Demir içeriği ne kadar yüksek olursa, boksit madenciliği o kadar zor olur;
- Sülfürlü içerik. Çok miktarda kükürtün varlığı, boksitin işlenmesini zorlaştırır;
- CO3 cinsinden karbonatların içeriği (2-) . Çok miktarda karbonatın varlığı, boksitin işlenmesini zorlaştırır.
Boksit kullanılır:
- alümina üretiminde;
- aşındırıcı malzemelerin üretiminde;
- refrakter malzeme üretiminde;
- açık ocak çeliğini eritmek için bir eritken olarak;
- gazları kurutmak ve yağı kükürtten temizlemek için;
- boya olarak.
Bugüne kadar, ana boksit tedarikçileri:
- Avustralya - ayrıca çok büyük Fe, Au, U, Ni, Co, Cu vb. birikintileri vardır. Avustralya'dan hammadde satın almak, kendi hammaddenizi işlemekten daha karlı.
- Gine - Rusya'nın satın aldığı birkaç koltuk var.
- Orta Amerika: Guyana, Jamaika, Suriman.
- Brezilya.
Avrupa'da tüm mevduatlar tükendi. Boksitler Yunanistan'dan tedarik ediliyor, ancak bu hammadde kalitesiz.

Şekil 2 - Dünyadaki boksit rezervleri
Aşağıda, Rusya'daki ana alüminyum cevher yatakları bulunmaktadır.
- İlk mevduat 1914 yılında Tikhvin kasabası yakınlarında, St. Petersburg yakınlarında keşfedildi. Bu sahada 6 fabrika inşa edildi. En büyüğü Volkhov alüminyum fabrikasıdır. Bugüne kadar, Tikhvinskoye alanı tükendi ve esas olarak ithal hammaddelerle çalışıyor.
- 1931'de benzersiz Severo-Uralskoye yüksek kaliteli boksit yatağı (SUBR) keşfedildi. Ural alüminyum fabrikasının (UAZ) 1939'daki inşaatının temelini oluşturdu. Ve Güney Ural boksit madeni (YUBR) temelinde, Bogoslovsky alüminyum izabe tesisi (BAZ) inşa edildi.
- Severoonezhskoye sahası, Kola Yarımadası yolunda yer almaktadır. Planda var ama yapım tarihi bilinmiyor.
- Vislovskoe yatağı, kaolit tipi saf bir kil yatağıdır. Alümina için kullanılmaz.
- Timanskoye alanı (Komi Cumhuriyeti, Varkuta). Kanadalılar bu alanla ilgileniyorlar, bu yüzden fabrikalar kurmayı planlıyorlar (Komi Sual bir holding şirketidir).
Boksit cevherlerinden alümina elde edilmesi
Alüminyum amfoterik olduğu için alümina üç şekilde üretilir:
- alkali,
- asit;
- elektrolitik.
En yaygın olanı alkalin yöntemdir (son yüzyılın sonunda Rusya'da geliştirilen ve az miktarda (% 5-6'ya kadar) silika içeren yüksek dereceli boksitlerin işlenmesi için kullanılan K. I. Bayer'in yöntemi). O zamandan beri, teknik performansı önemli ölçüde iyileştirildi. Bayer yöntemiyle alümina üretimi için şema Şekil 3'te gösterilmektedir.

Şekil 3 - Bayer yöntemiyle alümina elde etme şeması
Yöntemin özü, alüminyum çözeltilerinin alüminyum hidroksit verildiğinde hızla bozunması ve 169-170 °C'de yoğun karıştırma koşulları altında buharlaşmasından sonra ayrışmadan kalan çözeltinin, boksitlerde bulunan alüminayı tekrar çözebilmesidir. Bu yöntem aşağıdaki ana işlemlerden oluşur:
1. Değirmenlerde kırma ve öğütme işlemlerinden oluşan boksitin hazırlanması; değirmenlere boksit, kostik alkali ve Al 2 O 3 salınımını artıran az miktarda kireç verilir; elde edilen hamur, liç için beslenir;
2. Boksit liçi (son zamanlarda, şimdiye kadar kullanılan yuvarlak şekilli otoklav blokları, kısmen, liçinin 230-250 ° C (500-520 K) sıcaklıklarda meydana geldiği boru şeklindeki otoklavlarla değiştirildi; bu, kimyasal ayrışmasından oluşur. sulu çözelti alkalileri ile etkileşim; alüminyum oksit hidratlar, alkali ile etkileşime girdiğinde, sodyum alüminat formunda çözeltiye girer:
AlOOH+NaOH→NaAlO 2 +H 2 O
Al(OH)3 +NaOH→NaAlO2 +2H20;
Si02 +2NaOH→Na2SiO3 +H2O;
çözelti içinde, sodyum alüminat ve sodyum silikat, çözünmeyen bir sodyum alüminosilikat oluşturur; titanyum ve demir oksitler çözünmeyen kalıntıya geçerek kalıntıya kırmızı bir renk verir; bu kalıntıya kırmızı çamur denir. Çözünmenin tamamlanmasının ardından, elde edilen sodyum alüminat, sıcaklık 100 ° C düşürülürken sulu bir alkali çözeltisi ile seyreltilir;
3. Alüminat çözeltisinin kırmızı çamurdan ayrılması, genellikle özel koyulaştırıcılarda yıkanarak gerçekleştirilir; bunun sonucunda kırmızı çamur çökelir ve alüminat solüsyonu süzülür ve ardından süzülür (arıtılır). Sınırlı miktarlarda çamur, örneğin çimentoya katkı maddesi olarak kullanılır. Üretilen 1 ton alümina üzerine boksitin derecesine bağlı olarak 0,6 - 1,0 ton kırmızı çamur (kuru kalıntı) düşer;
4. Alüminat çözeltisinin ayrışması. Filtrelenir ve karıştırıcılar (ayrıştırıcılar) ile büyük kaplara pompalanır. Alüminyum hidroksit Al(OH)3, 60 °C'ye (330 K) soğutulduktan ve sürekli karıştırıldıktan sonra aşırı doymuş bir çözeltiden ekstrakte edilir. Bu işlem yavaş ve düzensiz ilerlediğinden ve alüminyum hidroksit kristallerinin oluşumu ve büyümesi, daha sonraki işlemlerde büyük önem taşıdığından, ayrıştırıcılara - tohumlara büyük miktarda katı hidroksit eklenir:
Na 2 O Al 2 O 3 + 4H2O→Al(OH) 3 + 2NaOH;
5. Alüminyum hidroksitin tahsisi ve sınıflandırılması; bu, %50-60 Al(OH)3 partikülü içeren bir çökeltinin alüminat çözeltisinden ayrıldığı hidrosiklonlarda ve vakum filtrelerinde olur. Hidroksitin önemli bir kısmı, değişmeyen miktarlarda dolaşımda kalan bir tohum materyali olarak bozunma işlemine geri döndürülür. Su ile yıkandıktan sonra kalıntı kalsinasyona gider; filtrat da dolaşıma geri döndürülür (buharlaştırıcılarda yoğunlaştırıldıktan sonra - yeni boksitleri süzmek için);
6. Alüminyum hidroksitin dehidrasyonu (kalsinasyon); alümina üretiminin son işlemidir; borulu döner fırınlarda ve son zamanlarda 1150 - 1300 ° C sıcaklıkta malzemenin türbülanslı hareketi olan fırınlarda gerçekleştirilir; bir döner fırından geçen, kurutulmuş ve suyu alınmış ham alüminyum hidroksit; ısıtıldığında, aşağıdaki yapısal dönüşümler sırayla gerçekleşir:
Al(OH) 3 → AlOOH → γ-Al 2 O 3 → α-Al 2 O 3
200 °C - 950 °C - 1200 °C.
Nihai kalsine edilmiş alümina %30 - 50 α-Al2O3 (korindon) içerir, geri kalanı γ-Al 2 O 2'dir.
Bu yöntem, üretilen tüm alüminanın % 85 - 87'sini çıkarır. Elde edilen alümina, 2050 ° C erime noktasına sahip güçlü bir kimyasal bileşiktir.
Elektroliz ile alüminyum elde etmek
Kriyolit bazlı bir eriyikte çözünmüş alüminyum oksidin elektrolitik indirgenmesi, bir elektrolitik hücrede 950–970 °C'de gerçekleştirilir. Hücre, altına elektrik akımı sağlanan karbon bloklarla kaplı bir banyodan oluşur. Altta salınan katot görevi gören sıvı alüminyum, elektrolit tuzu eriyiğinden daha ağırdır, bu nedenle bir kömür bazında toplanır ve buradan periyodik olarak dışarı pompalanır (Şekil 4). Yukarıdan, karbon anotlar, alüminyum oksitten salınan oksijen atmosferinde yanan, karbon monoksit (CO) veya karbon dioksit (CO2) salan elektrolite daldırılır. Pratikte iki tip anot kullanılır:
- bir alüminyum kabuğa doldurulmuş Zederberg kütlesinin (%25 - 35 kömür katranlı düşük küllü kömür) "ekmekleri" olarak adlandırılan briketlerden oluşan kendi kendine pişirilen Zederberg anotları; yüksek sıcaklığın etkisi altında anot kütlesi ateşlenir (sinterlenir);
- büyük karbon bloklardan yapılmış ateşlenmiş veya "sürekli" anotlar (örneğin, 1900 × 600 × 500 mm, yaklaşık 1,1 ton ağırlığında).

Şekil 4 - Elektrolizörün şeması
Elektrolizörlerdeki akım gücü 150.000 A'dır. Şebekeye seri olarak bağlanırlar, yani bir sistem (seri) elde edilir - uzun bir elektrolizör sırası.
4 - 5 V olan banyodaki çalışma voltajı, çalışma sırasında sistemin çeşitli bölümlerinde voltaj kayıpları kaçınılmaz olduğundan, alüminyum oksidin bozunduğu voltajdan çok daha yüksektir. 1 ton alüminyum alındığında hammadde ve enerji dengesi Şekil 5'te gösterilmektedir.

Resim 5 - 1 ton alüminyum üretiminde hammadde ve enerji dengesi
Reaksiyon kabında alüminyum oksit önce alüminyum klorüre dönüştürülür. Daha sonra, sıkıca yalıtılmış bir banyoda, KCl, NaCl'nin erimiş tuzlarında çözünen AlCl3'ün elektrolizi gerçekleşir. Bu süreçte açığa çıkan klor emilir ve geri dönüşüm için beslenir; katotta alüminyum biriktirilir.
Bu yöntemin, sıvı kriyolit-alümina eriyiğinin (kriyolit içinde çözülmüş Al 2 O 3 , Na 3 AlF6) mevcut elektrolizine göre avantajları şunlardır: %30'a kadar enerji tasarrufu; geleneksel elektroliz için uygun olmayan alüminyum oksit kullanma olasılığı (örneğin, yüksek silikon içeriğine sahip Al 2 O 3); pahalı kriyolitin daha ucuz tuzlarla değiştirilmesi; florür emisyonu tehlikesinin ortadan kaldırılması.
Rafine alüminyum elde etmek
Alüminyum için, sulu tuz çözeltilerinin ayrıştırılmasıyla elektrolizin rafine edilmesi mümkün değildir. Bazı amaçlar için, bir kriyolit-alümina eriyiğinin elektrolizi ile elde edilen endüstriyel alüminyumun (Al 99.5 - Al 99.8) saflaştırma derecesi yetersiz olduğundan, endüstriyel alüminyumdan veya metal atıklarından rafine edilerek daha saf alüminyum (Al 99.99 R) bile elde edilir. . En ünlü arıtma yöntemi üç katmanlı elektrolizdir.
Üç katmanlı elektroliz ile arıtma
Doğru akımla çalışan bir çelik sac ile kaplanmış (Şekil 6) arıtma banyosu, akım uçları olan bir kömür ocağı ve ısı yalıtımlı manyezit astardan oluşur. Bir kriyolit-alümina eriyiğinin elektrolizinin aksine, buradaki anot, kural olarak, erimiş rafine metaldir (alt anot tabakası). Elektrolit, saf florürlerden veya baryum klorür ile alüminyum ve sodyum florürlerin (orta katman) bir karışımından oluşur. Elektrolitteki anot tabakasından çözünen alüminyum, elektrolitin (üst katot tabakası) üzerine salınır. Saf metal katot görevi görür. Akım, bir grafit elektrot tarafından katot tabakasına sağlanır.

Şekil 6 - Alüminyumun rafine edilmesi için ön ocaklı bir elektrolitik hücrenin şeması (Fulda - Ginzberg'e göre)
1 - alüminyum eriyik; 2 – elektrolit; 3 - yüksek frekanslı rafine alüminyum; 4 – grafit katot; 5 - manyezit duvar; 6 - ön korna; 7 - yalıtım katmanı; 8 - yan yalıtım; 9 - kömür ocağı; 10 – anot iletkeni; 11 - ocağın izolasyonu; 12 - demir kutu; 13 - kapak
Banyo 750 - 800 ° C'de çalışır, güç tüketimi 1 kg saf alüminyum için 20 kWh'dir, yani geleneksel alüminyum elektrolizinden biraz daha yüksektir.
Anot metali %25–35 Cu içerir; %7 – 12 Zn; %6 – 9 Si; %5'e kadar Fe ve az miktarda manganez, nikel, kurşun ve kalay, geri kalanı (%40 - 55) alüminyumdur. Rafinasyon sırasında tüm ağır metaller ve silikon anot tabakasında kalır. Elektrolitte magnezyum varlığı, elektrolit bileşiminde istenmeyen değişikliklere veya güçlü cürufuna yol açar. Magnezyumu uzaklaştırmak için magnezyum içeren cüruflar flux veya gaz klor ile işlenir.
Rafinasyon sonucunda, ağır metaller ve silikon içeren ve alkali çözelti ve kristal kalıntı şeklinde izole edilen saf alüminyum (%99,99) ve segregasyon ürünleri (Ziger ürünü) elde edilir. Alkali çözelti bir atıktır ve katı artık asitten arındırma için kullanılır.
Rafine alüminyum genellikle aşağıdaki bileşime sahiptir, %: Fe 0.0005 - 0.002; Si 0,002 - 0,005; Cu 0,0005 - 0,002; Zn 0,0005 - 0,002; Mg izleri; Dinlen.
Rafine alüminyum, belirtilen bileşimde yarı bitmiş bir ürün halinde işlenir veya magnezyum ile alaşımlanır (tablo 1).
Tablo 1 - DIN 1712, sayfa 1'e göre yüksek saflıkta alüminyum ve birincil alüminyumun kimyasal bileşimi
|
İzin verilen kirlilik*, % |
||||||||
|
dahil olmak üzere |
||||||||
* Olabildiğince geleneksel yöntemlerle araştırma yapmak.
** Elektrik mühendisliği için saf alüminyum (alüminyum iletkenler), %0.03'ten fazla olmayan (Ti + Cr + V + Mn) birincil alüminyum 99.5 formunda sağlanır; bu durumda E-A1, malzeme numarası 3.0256 olarak belirlenmiştir. Aksi takdirde VDE-0202 ile uyumludur.
Organoalüminyum kompleks bileşikleri ve bölge eritme ile arıtma
Daha yüksek saflık derecesi A1 99.99 R olan alüminyum, elektrolit olarak karmaşık organoalüminyum alüminyum bileşikleri kullanılarak saf veya ticari olarak saf alüminyumun elektrolizinin rafine edilmesiyle elde edilebilir. Elektroliz, katı alüminyum elektrotlar arasında yaklaşık 1000°C'lik bir sıcaklıkta gerçekleşir ve prensip olarak bakırın rafine elektrolizine benzer. Elektrolitin doğası, havasız ve düşük akım yoğunluğunda çalışma ihtiyacını belirler.
İlk başta sadece laboratuvar ölçeğinde kullanılan bu tür arıtma elektrolizi, halihazırda küçük bir endüstriyel ölçekte gerçekleştirilmektedir - yılda birkaç ton metal üretilmektedir. Elde edilen metalin nominal saflaştırma derecesi %99,999 -99,9999'dur. Bu saflıkta bir metal için potansiyel uygulama alanları, kriyojenik elektrik mühendisliği ve elektroniktir.
Ele alınan arıtma yöntemini galvanik kaplamada kullanmak mümkündür.
Daha da yüksek saflık - nominal olarak A1 99.99999'a kadar - metalin müteakip bölge eritilmesiyle elde edilebilir. Yüksek saflıkta alüminyumu yarı bitmiş bir ürün, levha veya tel halinde işlerken, metalin düşük yeniden kristalleşme sıcaklığı dikkate alındığında özel önlemler almak gerekir. Rafine edilmiş metalin dikkate değer bir özelliği, kriyojenik sıcaklıklar bölgesindeki yüksek elektrik iletkenliğidir.


