АЛКЕНЫ
Углеводороды, в молекуле которых помимо простых σ-связей углерод - углерод и углерод - водород имеются углерод-углеродные π-связи, называются непредельными. Так как образование π-связи формально эквивалентно потере молекулой двух атомов водорода, то непредельные углеводороды содержат на 2п атомов водорода меньше, чем предельные, где п - число π -связей:
Ряд, члены которого отличаются друг от друга на (2Н) n , называется изологическим рядом. Так, в приведенной выше схеме изологами являются гексаны, гексены, гексадиены, гексины, гексатриены и т. д.
Углеводороды, содержащие одну π-связь (т. е. двойную связь), называются алкенами (олефинами) или, по первому члену ряда - этилену, этиленовыми углеводородами. Общая формула их гомологического ряда С п Н 2л.
1. Номенклатура
В соответствии с правилами ИЮПАК при построении названий алкенов наиболее длинная углеродная цепь, содержащая двойную связь, получает название соответствующего алкана, в котором окончание -ан заменено на -ен. Эта цепь нумеруется таким образом, чтобы углеродные атомы, участвующие в образовании двойной связи, получили номера, наименьшие из возможных:

Радикалы называются и нумеруются как и в случае алканов.
Для алкенов сравнительно простого строения разрешается применять более простые названия. Так, некоторые наиболее часто встречающиеся алкены называют, добавляя суффикс -ен к названию углеводородного радикала с тем же углеродным скелетом:
Углеводородные радикалы, образованные из алкенов, получают суффикс -енил. Нумерация в радикале начинается от углеродного атома, имеющего свободную валентность. Однако для простейших алкенильных радикалов вместо систематических названий разрешается использовать тривиальные:

Водородные атомы, непосредственно связанные с ненасыщенными атомами углерода, образующими двойную связь, часто называют винилъными атомами водорода,
2. Изомерия
Помимо изомерии углеродного скелета, в ряду алкенов появляется еще и изомерия положения двойной связи. В общем виде изомерия такого типа - изомерия положения заместителя (функции) - наблюдается во всех случаях, когда в молекуле имеются какие-либо функциональные группы. Для алкана С 4 Н 10 возможны два структурных изомера:
Для алкена С 4 Н 8 (бутена) возможны три изомера:

Бутен-1 и бутен-2 являются изомерами положения функции (в данном случае ее роль выполняет двойная связь).
Пространственные изомеры различаются пространственным расположением заместителей относительно друг друга и называются цис-изомерами, если заместители расположены по одну сторону от двойной связи, и транс-изомерами, если по разные стороны:

3. Строение двойной связи
Энергия разрыва молекулы по двойной связи С=С равна 611 кДж/моль; так как энергия σ-связи С-С равна 339 кДж/моль, то энергия разрыва π -связи равна лишь 611-339 = 272 кДж/моль. π -электроны значительно легче σ -электронов поддаются влиянию, например, поляризующих растворителей или воздействию любых атакующих реагентов. Это объясняется различием в симметрии распределения электронного облака σ- и π-электронов. Максимальное перекрывание р-орбиталей и, следовательно, минимальная свободная энергия молекулы реализуются лишь при плоском строении винильного фрагмента и при укороченном расстоянии С-С, равном 0,134нм, т.е. значительно меньшем, чем расстояние между углеродными атомами, связанными простой связью (0,154 нм). С поворотом «половинок» молекулы относительно друг друга по оси двойной связи степень перекрывания орбиталей снижается, что связано с затратой энергии. Следствием этого является отсутствие свободного вращения по оси двойной связи и существование геометрических изомеров при соответствующем замещении у атомов углерода.
4. Физические свойства
Как и алканы, низшие гомологи ряда простейших алкенов при обычных условиях - газы, а начиная с С 5 - низкокипящие жидкости.

Все алкены, как и алканы, практически нерастворимы в воде и хорошо растворимы в других органических растворителях, за исключением метилового спирта; все они имеют меньшую плотность, чем вода.
5. Химические свойства
При рассмотрении реакционной способности сложных органических соединений действует общий принцип. В большинстве реакций участвует не «инертный» углеводородный радикал, а имеющиеся функциональные группы и их ближайшее окружение. Это естественно, ибо большинство связей менее прочны, чем связи С-С и С-Н, и, кроме того, связи в функциональной группе и вблизи нее наиболее поляризованы.
Естественно ожидать, что реакции алкенов будут проходить по двойной связи, которую тоже можно считать функциональной группой, а следовательно, будут реакциями присоединения, а не реакциями замещения, характерными для ранее рассмотренных алканов.
Присоединение водорода
Присоединение водорода к алкенам приводит к образованию алканов:
Присоединение водорода к этиленовым соединениям в отсутствие катализаторов происходит лишь при высоких температурах, при которых часто начинается разложение органических веществ. Значительно легче присоединение водорода идет в присутствии катализаторов. Катализаторами служат металлы платиновой группы в мелкодисперсном состоянии, сама платина и особенно палладий - уже при обычной температуре. Большое практическое значение имело открытие Сабатье, применившего специально приготовленный мелкораздробленный никель при температуре 150-300°С и в многочисленных работах показавшего универсальность этого катализатора для целого ряда реакций восстановления.
Присоединение галогенов
Галогены присоединяются к алкенам с образованием дигалогенопроизводных, содержащих атомы галогена у соседних атомов углерода:

На первой стадии этой реакции происходит взаимодействие между π-электронами двойной связи и электрофильной частицей галогена с образованием π-комплекса (I). Далее π-комплекс перегруппировывается в ониевый (бромониевый) ион (II) с ощеплением аниона галогена, находящийся в равновесии с карбкатионом (III). Затем анион атакует ониевый ион с образованием продукта присоединения (IV):

Атака анионом бромониевого иона (II) с образованием дибромида (IV) происходит в транс-положение. Так, в случае присоединения Вг 2 к циклопентену образуется только транс-1,2-дибромдикло-пентан:

Доказательством двухстадийного присоединения галогена к алкенам является тот факт, что при присоединении Вг 2 к циклогексену в присутствии МаС1 образуется не только транс-1,2-дибромциклогексан, но и транс-1-бром-2-хлорциклогексан:

Радикальное галогенирование
В жестких условиях (газовая фаза, 500°С) галогены не присоединяются по двойной связи, а происходит галогенирование α-положения:
В этом случае реакция идет по радикальному механизму.
Присоединение галогеноводородов
Галогеноводороды присоединяются к алкенам с образованием галогеналкилов. Присоединение в случае несимметричных молекул идет по правилу Марковникова, т. е. водород присоединяется к наиболее гидрогенизированному атому углерода (с наибольшим числом водородных атомов):
Эта реакция, как и присоединение брома к этилену, идет после образования π-комплекса через стадию образования протониевого иона:

В присутствии перекисей бромоводород присоединяется не по правилу Марковникова (эффект Хараша):
В присутствии перекисей реакция идет не по механизму электрофильного присоединения, как выше, а по радикальному механизму. Первой стадией является атака перекисного радикала на молекулу НВг:
Возникший радикал брома присоединяется к пропилену с образованием нового радикала:

Последний стабилизируется за счет вырывания водорода из новой молекулы НВг с регенерацией нового радикала брома и т. д.:
И в этом случае направление процесса определяется устойчивостью радикалов бромпропана: образуется преимущественно более устойчивый, приводя к 1-бромпропану.
Присоединение воды и серной кислоты
В присутствии кислот вода присоединяется по двойной связи по правилу Марковникова:
Так же идет реакция и с серной кислотой:
Окисление перманганатом калия в нейтральной или слабощелочной среде (реакция Вагнера)
На первой стадии по механизму цис-присоединения идет присоединение иона МпО 4 к кратной связи с последующим гидролитическим расщеплением неустойчивого продукта присоединения и выделения иона МпО 3 -

Реакция идет по схеме цис-присоединения:

Кислые растворы перманганата окисляют алкены с разрывом цепи по С=С-связи и образованием кислот или кетонов:
Действие озона на алкены
Эта реакция приводит к кристаллическим сильновзрывчатым озонидам, которые при гидролизе образуют альдегиды или кетоны:

Реакция часто применяется для определения положения двойной связи в молекуле, так как по образующимся карбонильным соединениям можно представить себе и строение исходного алкена.
Реакция идет путем цис-циклоприсоединения через стадию неустойчивого мольозонида, который подвергается диссоциации и последующей рекомбинации:

Полимеризация алкенов
Особо важное значение получила полимеризация этилена и пропилена в полимеры с молекулярной массой около 10 5 . До 1953 г. в основном применялась радикальная (инициируемая свободными радикалами) полимеризация, хотя в принципе использовалось и анионное, и катионное инициирование процесса.
После работ Циглера и Натта, которые получили Нобелевскую премию за эти исследования, наиболее широко стала использоваться так называемая координационная полимеризация. Простейший «циглеровский» катализатор этого типа состоит из триэтилалюминия и соединений титана (IV). При этом происходит образование полимеров с высокой степенью стереорегулярности. Например, при полимеризации пропилена образуется изотактический полипропилен - полимер, в котором все боковые СН 3 -группы занимают одинаковое пространственное положение:

Это придает полимеру большую прочность, и он может даже применяться для изготовления синтетического волокна.
Полиэтилен, получаемый этим способом, представляет собой предельный углеводород с неразветвленной цепью. Он менее эластичен, чем полиэтилен, получаемый при высоких давлениях, но обладает большей твердостью и способен выдерживать воздействие более высоких температур.
Благодаря сочетанию многих ценных свойств полиэтилен имеет очень широкое применение. Он является одним из лучших материалов для изоляции кабелей, для применения в радарной технике, радиотехнике, сельском хозяйстве и др. Из него изготавливают трубы, шланги, сосуды, тару для сельскохозяйственных продуктов и удобрений, пленки различной толщины и многие бытовые предметы. Прочные пленки из полиэтилена начали применяться даже в качестве покрытия дна искусственных каналов для придания им водонепроницаемости.
Теломеризация
Интересен имеющий промышленное применение процесс сополимеризации этилена с тетрахлоридом углерода, названный теломеризацией. Если в смесь этилена с СС1 4 внести перекись бензоила или другой инициатор, распадающийся с образованием свободных радикалов, происходит следующий процесс:
Радикалы СС1 3 " инициируют цепную полимеризацию этилена:
При встрече с другой молекулой СС1 4 рост цепи прекращается:
Радикал СС1 3 - дает начало новой цепи.
Образующиеся низкомолекулярные продукты полимеризации, содержащие на концах цепи атомы галогена, называются теломерами. Получены теломеры со значениями п =2,3, 4, ...,15.
При гидролизе продуктов теломеризации образуются ω-хлорзаме-щенные карбоновые кислоты, являющиеся ценными химическими продуктами.
Для алкенов характерны, прежде всего, реакции присоединения по двойной связи. В основном эти реакции идут по ионному механизму. Пи-связь разрывается, и образуются две новые сигма-связи. Напомню, что для алканов типичными были реакции замещения и шли они по радикальному механизму. Присоединяться к алкенам могут молекулы водорода, эти реакции называются гидрирование, молекулы воды, гидратация, галогены галогенирование, галогенводороды гидрогалогенирование. Но обо всем по порядку.
Реакции присоединения по двойной связи
Итак, первое химическое свойство способность присоединять галогеноводороды, гидрогалогенирование.
Пропен и остальные алкены реагируют с галогеноводородами по правилу Марковникова.

Атом водорода присоединяется к наиболее гидрированному, или правильнее сказать гидрогенизированному, атому углерода.
Вторым номером в нашем списке свойств будет гидратация, присоединение воды.
Реакция проходит при нагревании в присутствии кислоты обычно серной или фосфорной. Присоединение воды происходит также по правилу Марковникова, то есть первичный спирт можно получить только гидратацией этилена, остальные неразветвленные алкены дают вторичные спирты.

И для гидрогалогениерования и для гидратации существуют исключения из правила Марковникова. Во-первых, против этого правила присоединение протекает в присутствии пероксидов.
Во-вторых, для производных алкенов, в которых присуствуют электронноакцепторне группы. Например, для 3,3,3-трифторпропена-1.

Атомы фтора за счет высокой электроотрицательности оттягивают на себя электронную плотность по цепи сигма-связей. Такое явление называется отрицательным индуктивным эффектом.
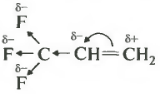
Из-за этого происходит смещение подвижных пи-электронов двойной связи и у крайнего атома углерода оказывается частичный положительный заряд, который обычно обозначается как дельта плюс. Именно к нему и пойдет отрицательно заряженный ион брома, а катион водорода присоединится к наименее гидрированному атому углерода.
Помимо трифторметильной группы отрицательным индуктивным эффектом обладает, например, трихлорметильная группа, нитрогруппа, карбоксильная группа и некоторые другие.
Этот второй случай нарушения правила Марковникова в ЕГЭ встречается очень редко, но все-таки желательно иметь его в виду, если вы планируете сдать экзамен на максимальный балл.
Третье химическое свойство присоединение молекул галогенов.

В первую очередь это касается брома, поскольку данная реакция является качественной на кратную связь. При пропускании, например, этилена через бромную воду, то есть раствор брома в воде, имеющий коричневый цвет, происходит ее обесцвечивание. Если пропускать через бромную воду смесь газов, например, этан и этен, то можно получить чистый этан без примеси этена, поскольку тот останется в реакционной колбе в виде дибромэтана, представляющего собой жидкость.
Особым образом стоит отметить реакцию алкенов в газовой фазе при сильном нагревании, например, с хлором.
При таких условиях протекает не реакция присоединения, а реакция замещения. При чем исключительно по альфа-атому углерода, то есть атому, соседствующему с двойной связью. В данном случае получается 3-хлорпропен-1. Эти реакции на экзамене встречаются нечасто, поэтому большинство учеников их не помнит и, как правило, совершает ошибки.
Четвертым номером идет реакция гидрирования, а вместе с ней и реакция дегидрирования. То есть присоединение или отщепление водорода.

Гидрирование происходит при не очень высокой температуре на никелевом катализаторе. При более высокой температуре возможно дегидрирование с получением алкинов.
Пятым свойством алкенов является способность к полимеризации, когда сотни и тысячи молекул алкена за счет разрыва пи-связи и образования сигма-свзяей друг с другом образуют очень длинные и прочные цепочки.
В данном случае получился полиэтилен. Обратите внимание, что в получившейся молекуле кратные связи отсутствуют. Такие вещества называются полимерами, исходные молекулы называются мономерами, повторяющийся фрагмент это элементарное звено полимера, а число n степень полимеризации.
Также возможны реакции получения других важных полимерных материалов, например, полипропилена.
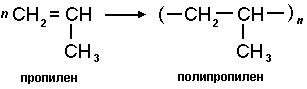
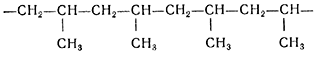
Еще один важный полимер поливинилхлорид.
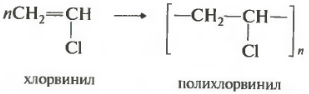
Исходным веществом для производства этого полимера является хлорэтен, тривиальное название которого винилхлорид. Поскольку этот непредельный заместитель называется винил. Часто встречающаяся аббревиатура на пластмассовых изделиях ПВХ как раз расшифровывается как поливинилхлорид.
Мы обсудили пять свойств, которые представляли собой реакции присоединения по двойной связи. Теперь обратимся к реакциям окисления .
Реакции окисления алкенов
Шестое химическое свойство в нашем общем списке это мягкое окисление или реакция Вагнера. Оно протекает при воздействии на алкен водным раствором перманганата калия на холоду, поэтому часто в экзаменационных заданиях указывают температуру ноль градусов.
В результате получается двухатомный спирт. В данном случае этиленгликоль, а в целом такие спирты носят общее название гликоли. В процессе реакции фиолетово-розовый раствор перманганата обесцвечивается, поэтому эта реакция также является качественной на двойную связь. Марганец в нейтральной среде из степени окисления +7 восстанавливается до степени окисления +4. Рассмотрим еще несколько примеров. УРАВНЕНИЕ
Здесь получился пропандиол-1,2. Однако таким же образом будут реагировать и циклические алкены. УРАВНЕНИЕ
Еще один вариант, когда двойная связь находится, например, в боковой цепи ароматических углеводородов. Регулярно в заданиях егэ встречается реакция Вагнера с участием стирола, его второе название винилбензол.
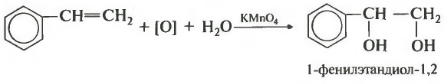
Я надеюсь, что представил вашему вниманию достаточно примеров, чтобы вы поняли, что мягкое окисление двойной связи всегда подчиняется довольно простому правилу пи-связь разрывается и к каждому атому углерода присоединяется гидроксигруппа.
Теперь, что касается жесткого окисления. Это будет наше седьмое свойство. Такое окисление происходит, когда алкен реагирует с кислотным раствором перманганата калия при нагревании.
Происходит деструкция молекулы, то есть ее разрушение по двойной связи. В случае бутена-2 получились две молекулы уксусной кислоты. В целом же, по продуктам окисления можно судить о положении кратной связи в углеродной цепи.
При окислении бутена-1 получается молекула пропионовой (пропановой) кислоты и углекислый газ.
В случае этилена получится две молекулы углекислого газа. Во всех случаях в кислой среде марганец из степени окисления +7 восстанавливается до +2.
И, наконец, восьмое свойство полное окисление или горение.
Алкены сгорают, как и другие углеводороды, до углекислого газа и воды. Запишем уравнение сгорания алкенов в общем виде.
Молекул углекислого газа будет столько же, сколько и атомов углерода в молекуле алкена, поскольку в состав молекулы CO 2 входит один атом углерода. То есть n молекул CO 2 . Молекул воды будет в два раза меньше, чем атомов водорода, то есть 2n/2, а значит просто n.
Атомов кислорода слева и справа одинаковое количество. Справа их 2n из углекислого газа плюс n из воды, итого 3n. Слева атомов кислорода столько же, а значит молекул в два раза меньше, потому как в состав молекулы входят два атома. То есть 3n/2 молекул кислорода. Можно записать 1,5n.
Мы рассмотрели восемь химических свойств алкенов.
К непредельным относят углеводороды, содержащие в молекулах кратные связи между атомами углерода. Непредельными являются алкены, алкины, алкадиены (полиены) . Непредельным характером обладают также циклические углеводороды, содержащие двойную связь в цикле (циклоалкены ), а также циклоалканы с небольшим числом атомов углерода в цикле (три или четыре атома). Свойство «непредельности» связано со способностью этих веществ вступать в реакции присоединения, прежде всего водорода, с образованием предельных, или насыщенных углеводородов - алканов.
Строение алкенов
Ациклические углеводороды, содержащие в молекуле помимо одинарных связей, одну двойную связь между атомами углерода и соответствующие общей формуле СnН2n. Свое второе название - олефины
- алкены получили по аналогии с жирными непредельными кислотами (олеиновая, линолевая), остатки которых входят в состав жидких жиров - масел.
Атомы углерода, между которыми есть двойная связь, находятся в состоянии sр 2 -гибридизации. Это означает, что в гибридизации участвуют одна s- и две р-орбитали, а одна р-орбиталь остается негибридизованной. Перекрывание гибридных орбиталей приводит к образованию σ-связи, а за счет негибридизованных р-орбиталей
соседних атомов углерода образуется вторая, π-связь. Таким образом, двойная связь состоит из одной σ- и одной π — связи. Гибридные орбитали атомов, образующих двойную связь, находятся в одной плоскости, а орбитали, образующие π -связь, располагаются перпендикулярно плоскости молекулы. Двойная связь (0,132 им) короче одинарной, а ее энергия больше, т. к. она является более прочной. Тем не менее, наличие подвижной, легко поляризуемой π -связи приводит к тому, что алкены химически более активны, чем алканы, и способны вступать в реакции присоединения.

Строение этилена

Образование двойной связи в алкенах
Гомологический ряд этена
Неразветвленные алкены составляют гомологи- ческий ряд этена (этилена ): С 2 Н 4 - этен, С 3 Н 6 - пропен, С 4 Н 8 - бутен, С 5 Н 10 - пентен, С 6 Н 12 - гексен, С 7 Н 14 - гептен и т.д.
Изомерия алкенов
Для алкенов характерна структурная изомерия. Структурные изомеры отличаются друг от друга строением углеродного скелета. Простейший алкен, для которого характерны структурные изомеры, - это бутен:

Особым видом структурной изомерии является изомерия положения двойной связи:
Алкены изомерны циклоалканам (межклассовая изомерия), например:

Вокруг одинарной углерод-углеродной связи возможно практически свободное вращение атомов углерода, поэтому молекулы алканов могут приобретать самую разнообразную форму. Вращение вокруг двойной связи невозможно, что приводит к появлению у алкенов еще одного вида изомерии - геометрической, или цис- и транс- изомерии .


Цис-изомеры
отличаются от транс-изомеров
пространственным расположением фрагментов молекулы (в данном случае метильных групп) относительно плоскости π -связи, а следовательно, и свойствами.
Номенклатура алкенов
1. Выбор главной цепи.
Образование названия углеводорода начинается с определения главной цепи - самой длинной цепочки атомов углерода в молекуле. В случае алкенов главная цепь должна содержать двойную связь.
2. Нумерация атомов главной цепи.
Нумерация атомов главной цепи начинается с того конца, к которому ближе находится двойная связь.
Например,правильное название соединения:
![]()
Если по положению двойной связи нельзя определить начало нумерации атомов в цепи, то его определяет положение заместителей так же, как для предельных углеводородов.

3. Формирование названия. В конце названия указывают номер атома углерода, у которого начинается двойная связь, и суффикс -ен , обозначающий принадлежность соединения к классу алкенов. Например:

Физические свойства алкенов
Первые три представителя гомологического ряда алкенов - газы; вещества состава С5Н10 — С16Н32 - жидкости; высшие алкены - твердые вещества.
Температуры кипения и плавления закономерно повышаются при увеличении молекулярной массы соединений.
Химические свойства алкенов
Реакции присоединения
. Напомним, что отличительной чертой представителей непредельных углеводородов - алкенов является способность вступать в реакции присоединения. Большинство этих реакций протекает по механизму электрофильного присоединения
.
1. Гидрирование алкенов.
Алкены способны присоединять водород в присутствии катализаторов гидрирования, металлов - платины, палладия, никеля:
Эта реакция протекает при атмосферном и повышенном давлении и не требует высокой температуры, т. к. является экзотермической. При повышении температуры на тех же катализаторах может пойти обратная реакция - дегидрирование.
2. Галогенирование (присоединение галогенов)
. Взаимодействие алкена с бромной водой или раствором брома в органическом растворителе (СС14) приводит к быстрому обесцвечиванию этих растворов в результате присоединения молекулы галогена к алкену и образования дигалогеналканов.
3. Гидрогалогенирование (присоединение галогеноводорода)
.
Эта реакция подчиняется
При присоединении галогеноводорода к алкену водород присоединяется к более гидрированному атому углерода, т. е. атому, при котором находится больше атомов водорода, а галоген - к менее гидрированному.


4. Гидратация (присоединение воды).
Гидратация алкенов приводит к образованию спиртов. Например, присоединение воды к этену лежит в основе одного из промышленных способов получения этилового спирта.
Обратите внимание на то, что первичный спирт (с гидроксогруппой при первичном углероде) образуется только при гидратации этена. При гидратации пропена или других алкенов образуются вторичные спирты .

Эта реакция протекает также в соответствии с правилом Марковникова - катион водорода присоединяется к более гидрированному атому углерода, а гидроксогруппа - к менее гидрированному.
5. Полимеризация.
Особым случаем присоединения является реакция полимеризации алкенов:
Эта реакция присоединения протекает по свободнорадикальному механизму.
Реакции окисления.
1. Горение.
Как и любые органические соединения, алкены горят в кислороде с образованием СО2 и Н2О:
2. Окисление в растворах. В отличие от алканов алкены легко окисляются под действием растворов перманганата калия. В нейтральных или щелочных растворах происходит окисление алкенов до диолов (двухатомных спиртов), причем гидроксильные группы присоединяются к тем атомам, между которыми до окисления существовала двойная связь:




Алкены - непредельные углеводороды, в составе которых есть одна двойная связь. Примеры алкенов:

Методы получения алкенов.
1. Крекинг алканов при 400-700°С. Реакция идет по свободнорадикальному механизму:

2. Дегидрирование алканов:
3. Реакция элиминирования (отщепление): от соседних атомов углерода отщепляются 2 атома или 2 группы атомов, и образуется двойная связь. К таким реакциям относят:
А) Дегидратацию спиртов (нагрев свыше 150°С, при участии серной кислоты , как водоотнимающего реагента):
Б) Отщепление галогенводородов при воздействии спиртового раствора щелочи:

Атом водорода отщепляется преимущественно от того атома углерода, который связан с меньшим числом атомов водорода (наименее гидрогенизированного атома) - правило Зайцева .
В) Дегалогенирование:

Химические свойства алкенов.
Свойства алкенов обуславливаются наличием кратной связи, поэтому алкены вступают в реакции электрофильного присоединения, которое протекает в несколько стадий (Н-Х - реагент):
1-я стадия:

2-я стадия:
 .
.
Ион водорода в такого типа реакциях принадлежит тому атому углерода, который имеет более отрицательный заряд. Распределение плотности такое:

Если в качестве заместителя стоит донор, который проявляется +I- эффект, то электронная плотность смещается в сторону наиболее гидрогенизированного атома углерода, создавая на нем частично отрицательный заряд. Реакции идут по правилу Марковникова : при присоединении полярных молекул типа НХ (HCl , HCN , HOH и т.д.) к несимметричным алкенам водород присоединяется преимущественно к более гидрогенизированому атому углерода при двойной связи.
А) Реакции присоединения:
1) Гидрогалогенирование:
Реакция идет по правилу Марковникова. Но если в реакции присутствует пероксид , то правило не учитывается:
2) Гидратация. Реакция идет по правилу Марковникова в присутствие фосфорной или серной кислоты :

3) Галогенирование. В результате происходит обесцвечивание бромной воды - это качественная реакция на кратную связь:
4) Гидрирование. Реакция протекает в присутствие катализаторов.
Низшие алкены (С 2 - С 5), в промышленных масштабах получают из газов, образующихся при термической переработке нефти и нефтепродуктов. Алкены можно также получить, используя лабораторные методы синтеза.
4.5.1. Дегидрогалогенирование
При обработке галогеналканов основаниями в безводных растворителях, например, спиртовым раствором едкого кали, происходит отщепление галогеноводорода.
4.5.2. Дегидратация
При нагревании спиртов с серной или фосфорной кислотами происходит внутримолекулярная дегидратация ( - элиминирование).
Преобладающее направление реакции, как и в случае дегидрогалогенирования, - образование наиболее устойчивого алкена (правило Зайцева).
Дегидратацию спиртов можно провести, пропуская пары спирта над катализатором (оксиды алюминия или тория) при 300 - 350 о С.
4.5.3. Дегалогенирование вицинальных дигалогенидов
Действием цинка в спирте дибромиды, содержащие галогены у соседних атомов (вицинальные), могут быть превращены в алкены.

4.5.4. Гидрирование алкинов
При гидрировании алкинов в присутствии платинового или никелевого катализаторов, активность которых уменьшена добавлением небольшого количества соединений свинца (каталитический яд), образуется алкен, который не подвергается дальнейшему восстановлению.
4.5.5. Восстановительное сочетание альдегидов и кетонов
При обработке алюмогидридом лития и хлоридом титана(III) из двух молекул альдегида или кетона с хорошими выходами образуются ди- или соответственно тетразамещённые алкены.

5. АЛКИНЫ
Алкинами называются углеводороды, содержащие тройную углерод-углеродную связь –СС–.
Общая формула простых алкинов С n H 2n-2 . Простейшим представителем класса алкинов является ацетилен H–СС–H, поэтому алкины называют также ацетиленовыми углеводородами.
5.1. Строение ацетилена
Атомы углерода ацетилена находятся в sp -гибридном состоянии. Изобразим орбитальную конфигурацию такого атома. При гибридизации 2s -орбитали и 2р -орбитали образуются две равноценные sp -гибридные орбитали, расположенные на одной прямой, и остаются две негибридизованные р -орбитали.

Рис. 5.1 Схема формирования sp -гибридных орбиталей атома углерода
Направленияи формы орбиталей s р -гибридизованного атома углерода: гибридизованные орбитали эквивалентны, максимально удалены друг от друга
В молекуле ацетилена простая связь ( - связь) между атомами углерода образована перекрыванием двух sp -гибридизованных орбиталей. Две взаимно перпендикулярные - связи возникают при боковом перекрывании двух пар негибридизованных 2р- орбиталей, - электронные облака охватывают скелет так, что электронное облако имеет симметрию, близкую к цилиндрической. Связи с атомами водорода образуются за счёт sp -гибридных орбиталей атома углерода и 1s -орбитали атома водорода, молекула ацетилена линейна.

Рис. 5.2 Молекула ацетилена
а - боковое перекрывание 2р орбиталей дает две -связи;
б - молекула линейна, -облако имеет цилиндрическую форму
В пропине простая связь ( - связь) С sp -С sp3 короче аналогичной связи С sp -С sp2 в алкенах, это объясняется тем, что sp- орбиталь ближе к ядру, чем sp 2 - орбиталь .
Тройная углерод-углеродная связь С С короче двойной связи, а общая энергия тройной связи приблизительно равна сумме энергий одной простой связи С–С (347 кДж/моль) и двух -связей (259·2 кДж/моль) (табл. 5.1).


